- 57-50-1
-
Saccharose
Saccharose 
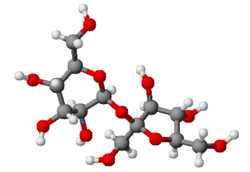
Général Nom IUPAC α-D-glucopyranosyl-(1↔2)-β-D-fructofuranoside Synonymes néohancoside D
reiniose
Fru ß(2↔1)α GlcNo CAS No EINECS PubChem SMILES InChI Apparence solide de forme variable blanc.[1] Propriétés chimiques Formule brute C12H22O11 [Isomères] Masse molaire 342,2965 g∙mol-1
C 42,11 %, H 6,48 %, O 51,42 %,pKa 12,62[2] Propriétés physiques T° fusion 185,5 °C [2] T° ébullition décomposition Solubilité 2 010 g⋅L-1 (à 25 °C)[2] Masse volumique 1.6 g/cm³[1] Précautions NFPA 704 SIMDUT[3] Produit non contrôlé Ingestion favorise l'apparition de caries, à grandes doses: vomissements, diarrhées, dyspepsies Écotoxicologie DL50 29,7 g⋅kg-1 (rats, oral)[2] LogP -3.67[1] Composés apparentés Autres composés Isomaltulose, Leucrose, Maltulose, Tréhalulose, Turanose Unités du SI & CNTP, sauf indication contraire. Le saccharose, ou sucrose, est plus simplement le sucre commercial extrait de la betterave sucrière ou de la canne à sucre. Le saccharose est une molécule organique composée de carbone, d'hydrogène et d'oxygène. Ce sucre est le constituant du sucre blanc courant.
Le saccharose est un sucre double (diholoside) formé par la condensation de 2 oses : une molécule de glucose et une molécule de fructose. Son nom officiel est le β-D-fructofuranosyl-(2↔1)-α-D-glucopyranoside. Il peut être symbolisé par Glc-Fru.
Sommaire
Propriétés
Structure
Le saccharose est un diholoside formé d'une molécule de glucose et d'une molécule de fructose reliées par une liaison osidique α(1↔2)β. Sa formule chimique non-développée est C12H22O11 et sa masse molaire est de 342,3 g.mol-1.
Le saccharose a 5 isomères naturels qui différent par la position de la liaison osidique :
- Tréhalulose ⇒ Glucose α(1→1) Fructose[4]
- Turanose ⇒ Glucose α(1→3) Fructose[5] (diholoside réducteur)
- Maltulose ⇒ Glucose α(1→4) Fructose[6]
- Leucrose ⇒ Glucose α(1→5) Fructose[4] (diholoside réducteur)
- Isomaltulose (Palatinose) ⇒ Glucose α(1→6) Fructose[7] (diholoside réducteur)
Propriétés chimiques
Le saccharose est un sucre non réducteur[8], le carbone hémiacétalique du glucose et le carbone hémiacétalique du fructose sont impliqués dans la liaison osidique. Il est non hygroscopique. Il ne peut effectuer de mutarotation et il n'est pas réducteur.
Hydrolyse
Il existe plusieurs types d'hydrolyses :
- L'hydrolyse chimique (en milieu acide)
- L'hydrolyse par résine échangeuse d'ion, cette technique permettant de contrôler le pourcentage de saccharose qui sera inverti.
- L'hydrolyse enzymatique. Elle est fonction de la température, du pH et de la concentration. Les deux enzymes entrant en jeu sont l'α-glucosidase et la β-fructosidase ou invertine.
En présence d'eau et à température modérée, soit 37 °C, le saccharose, par l'effet de l'enzyme invertase, s'hydrolyse en glucose et en fructose, ce qui permet son assimilation par l'organisme.
Le mélange produit par l'hydrolyse est un mélange équimolaire de glucose et de fructose, appelé sucre inverti. Il est néanmoins exceptionnel de trouver un sirop dans lequel la réaction a été complète et on trouvera souvent jusqu'à 30% de saccharose résiduel.
Propriétés physiques
Le sucre caramélise à 160 °C[9]. Sa solubilité est de 2,019 g.mL-1 à 25 °C[2]. Celle-ci augmente quand la température de l'eau augmente (Tableau 1).
Tableau 1 : Solubilité du saccharose Température en °C g Saccharose / g Eau 20 1,97 50 2,59 55 2,73 60 2,89 65 3,06 70 3,25 75 3,46 80 3,69 85 3,94 90 4,20 Le saccharose n'est pas soluble dans l'alcool pur.
Le taux de sucre est donné par le degré Brix.
Propriétés édulcorante
Le pouvoir sucrant du saccharose sert de référence dans l'échelle des produits sucrants, c'est-à-dire qu'il est considéré comme égal à 1. Le seuil de reconnaissance moyen du sucrose est de 0,017 mol⋅L-1[10].
Utilisations en agro-alimentaire
Physico-chimie
Lors de son utilisation dans l'industrie des boissons, le saccharose peut s'invertir tout seul lors du traitement thermique. De plus, le sucre inverti étant plus soluble que le saccharose, en sa présence, il peut jouer le rôle de rétenteur d'eau et empêcher la cristallisation de ce dernier.
Il est utilisé fréquemment, en tant qu'adjuvant de texture, pour ses qualités d'agglomérant.
Suivant l'Agence française de sécurité sanitaire des aliments (AFFSA), les sucres simples (dont le saccharose) interviennent dans la propagation des caries dentaires[11]. Elle préconise donc une diminution de la ration de saccharose, notamment pour les enfants.
Granulométrie
Les différentes tailles de cristaux suivants les besoins de l'industrie :
- sucre cristallisé,
- sucre semoule,
- sucre glace,
- sucre grain.
Notes et références
- ↑ a , b et c SUCROSE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ a , b , c , d et e (en) ChemIDplus, « Sucrose - RN: 57-50-1 » sur chem.sis.nlm.nih.gov, U.S. National Library of Medicine. Consulté le 09/009/2008.
- ↑ « Sucrose » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009
- ↑ a et b (en) (en) Peter M. Collins, Dictionary of carbohydrates, CRC Press, 2005, 1282 p. (ISBN 0849338298), p. 538
- ↑ (en) (en) Peter M. Collins, Dictionary of carbohydrates, CRC Press, 2005, 1282 p. (ISBN 0849338298), p. 948
- ↑ (en) MA Godshall, « The Expanding World of Nutritive and Non-Nutritive Sweeteners » sur http://www.sugarjournal.com, 01/2007, p. 12-20. Consulté le 7 novembre 2008 [pdf]
- ↑ (en) (en) Peter M. Collins, Dictionary of carbohydrates, CRC Press, 2005, 1282 p. (ISBN 0849338298), p. 537
- ↑ (en) (en) Shmuel Yannai, Dictionary of Food Compounds with CD-ROM: Additives, Flavors, and Ingredients, CRC Press, 2004, 1784 p. (ISBN 1584884169) [présentation en ligne], p. 1243-1244
- ↑ (en)Food-Info, caramelization
- ↑ (en) (en) Robert Shallenberger, Taste Chemistry, London, Springer, 1993, 613 pages p. (ISBN 0751401501), « Chemical nature, psychology and physiology of taste », p. 5-46
- ↑ R Ancellin, « Glucides et santé : Etat des lieux, évaluation et recommandations » sur http://www.afssa.fr, 2004, Afssa, p. 1-167. Consulté le 07/10/2008. [pdf]
Voir aussi
Articles connexes
Liens externes
- (en) Substance saccharose NCBI database
- (en) Compound: C00089 Sucrose www.Genome.net
- (en) Glycan: G00370 Neohancoside D www.Genome.net
- (en) Sucrosesur National Library of Medicine - Medical Subject Headings MeSH
- Portail de la biochimie
- Portail de la chimie
Catégories : Diholoside | Édulcorant | Sucre
Wikimedia Foundation. 2010.

