- Condensation
-
 Pour les articles homonymes, voir Condensation (homonymie).
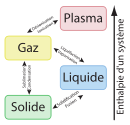
Pour les articles homonymes, voir Condensation (homonymie).En thermodynamique, la condensation désigne le passage d'un corps pur de l'état gazeux directement à l'état solide, sans passer par l'état liquide[1]. Pour la terminologie des changements d'état, voir changement d'état, ou l'image au format réduit dans le cadre « État de la matière » ici en bas de page.
Exemple : sublimation et condensation du diiode[2].
- Dans la suite de l'article, les sens du terme « condensation » sont ceux consacrés par l'usage courant ou spécialisé.
 « Condensation liquide » (de brume sur un rameau). Cette eau est dite « météoritique » ou hydrométéore
« Condensation liquide » (de brume sur un rameau). Cette eau est dite « météoritique » ou hydrométéore
 Buée sur une vitre
Buée sur une vitre
La condensation est le nom donné au phénomène physique de changement d'état de la matière qui passe d'un état dilué (gaz) à un état condensé (solide ou liquide). On peut expérimenter ce changement d'état lors d'une douche où, au contact du miroir froid, l'humidité de l'air se transforme en gouttelettes.
Dans la nature la condensation de la vapeur d'eau est naturellement présente dans l'air et est une étape importante du cycle de l'eau, à l'origine notamment de la rosée, des nuages et de la pluie, de la neige, du givre ou de certaines formes de verglas (brouillard givrant, qui est une forme de condensation solide).
Sommaire
Formulation
Il est d'usage lorsque l'état final (liquide ou solide) n'est pas indiqué, de ne l'employer que pour le passage de l'état gazeux à l'état liquide[3]. Mais pour plus de précision, il vaut mieux employer les expressions :
- condensation liquide (liquéfaction : passage de l'état gazeux à l'état liquide),
- condensation solide ou cristallisation (condensation : passage de l'état gazeux à l'état solide).
Le terme sublimation inverse est encore parfois utilisé pour désigner le changement d'état du gaz vers le solide, la sublimation désignant le changement d'état du solide au gaz, sans passer par l'état liquide.
Technique
Un dispositif de condensation est présent dans les systèmes de pompe à chaleur, utilisés notamment dans les dispositifs de climatisation et de froid industriel.
On peut retrouver pareil système de condenseur dans les chaudières à condensation. Le principe est simplement de réduire la température des gaz de combustion sous le point de rosée afin de récupérer la chaleur latente de la vapeur d'eau. Sa teneur est fonction du combustible ainsi que de l'excès d'air donné à la combustion (excès d'air indispensable afin d'assurer une bonne homogénéité combustible-air). On peut compter que sous 50 °C environ (fioul et gaz), la vapeur d'eau contenue dans les gaz de combustion a la possibilité de transmettre une énergie non négligeable, de l'ordre du dixième du pouvoir calorifique inférieur du combustible. Cette énergie est alors récupérée dans un condenseur (échangeur avec grande surface dont un côté est balayé par les gaz de combustion et l'autre par l'eau du circuit chauffage). Les gaz en sortie d'échangeur de chaleur principal (chaudière, à environ 180 °C) chutent en température (température finale minimale 60 °C) et restituent leur énergie à l'eau traversant le condenseur (souvent des tubes). Cela permet évidemment d'accroître le rendement global (plus de chaleur récupérée pour une même quantité de combustible). Il est cependant nécessaire de s'assurer que le conduit d'évacuation des gaz brûlés est prévu pour cette basse température (problème de tirage thermique, condensation d'acide sulfurique surtout pour le fioul) et qu'il a la possibilité d'évacuer l'eau produite. Les conduits en pierre, en brique et matériaux d'avant 2000 ne conviennent pas. Le tubage (mse en place d'un conduit intérieur) en PVDF (qui supporte jusqu'à 120 °C) ou en inox est impératif pour éviter ces problèmes : il faut compter environ 0,7 litre d'eau produite par litre de fioul et 1,1 litre d'eau par m3 de gaz naturel brûlé. Pour une chaudière de 20 kW, cela représente de 1,4 l/h à 2 l/h d'eau produite qu'il faut forcément canaliser. Depuis les années 1980, les fabricants de chaudière ont tous amélioré le rendement de leurs produits, ce qui implique que la température de sortie des gaz brulés a diminué et donc que la condensation de la vapeur d'eau est inévitable en fin de parcours des fumées voire avant. Tuber est donc le seul moyen d'éviter les dégâts.
Chimie
On parle de réaction de condensation chimique, lorsque deux molécules se lient pour n'en former qu'une avec généralement élimination d'une petite molécule (eau, ammoniac). On parle de polycondensation chimique, lorsque deux molécules se lient pour n'en former qu'une. Elle permet de constituer de très grandes molécules ou polymères, constitués par l'assemblage d'une succession de molécules plus petites, les monomères.
C'est le cas, par exemple, des protéines qui résultent de l'assemblage d'acides aminés par la formation du lien peptidique qui consiste en l'élimination d'une molécule d'eau entre deux acides aminés dans un milieu aqueux (condensation). La chaîne ainsi formée adopte des conformations rigides (hélices α et feuillets β), elles-mêmes asymétriques, qui jouent un rôle essentiel dans les fonctions de catalyse.
Dans le bâtiment
Souvent des signes d'humidité apparaissent sur certains murs causés par des condensations.
Le phénomène s'est amplifié avec l'élévation du coût du chauffage qui conduit d'une part à l'installation de vitrages isolants, de ventilations inappropriées, bouchées ou inexistantes et parfois de chauffage d'appoint sans évacuation (poêles à gaz ou à pétrole sans odeur, notamment) qui sont de gros producteurs de vapeur d'eau.
A chaque baisse de température dans le logement, l'excès d'eau dans l'air se dépose toujours aux endroits les plus froids, créant ainsi une zone favorable aux développement des moisissures.
Pour régler ce problème il faut chauffer (pour augmenter la capacité en eau de l'air), isoler (pour augmenter la température des points froids) et ventiler (pour évacuer l'air humide) l'habitation.
Notes et références
- Cf. par exemple les ouvrages suivants :
1. C. Chaussin, G. Hilly - Chaleur et Thermodynamique - Écoles Nationales d'Ingénieurs Arts et Métiers, Écoles d'Ingénieurs - Dunod (1962) pp. 171-172 ;
2. M. Joyal - Thermodynamique - Classes de Mathématiques Spéciales - Masson (1965) p.96 ;
3. Brénon-Audat et al. - Thermodynamique chimique - 1er Cycle - Classes préparatoires - Hachette (1993) p.206 ;
4. Dictionnaire de Physique expérimentale Quaranta - Tome II - Thermodynamique et applications - Pierron (1997) pp. 452 à 456 ;
5. en ligne : [PDF] Thermodynamique première année de Master (2008-2009) p. 85/112 (vignette 43) ; - Expérience : si on chauffe fortement des pastilles de diiode contenues dans le fond d'un tube à essai, des vapeurs violettes remplissent le tube (on peut observer qu'il n'y a pas de fusion) et des cristaux de diiode se déposent sur le haut du tube plus froid. Les vapeurs de diiode étant toxiques, il faut opérer sous hotte. Expérience extraite du Dictionnaire de Physique expérimentale Quaranta - Tome II - Thermodynamique et applications (cf. note supra) pp. 425 et 426.
- (fr) Définition de la condensation, sur le site de Météo France
Voir aussi
Articles connexes
- Condensat de Bose-Einstein.
- Distillation : la condensation s'obtient par le passage du distillat au travers d'un serpentin immergé dans un bain d'eau froide.
- Condensation - dynamique des aérosols
- Cycle de l'eau
- Ressource en eau
- Pollution de l'air
- Physique des nuages :
- forêt ombrophile (ou pluvieuse)
Bibliographie
- Dictionnaire de Physique expérimentale Quaranta - Tome II - Thermodynamique et applications - Pierron (1997) (ISBN 2 7085-0168-2)
Catégories :- Thermodynamique
- Transition de phase
- Thermodynamique atmosphérique
Wikimedia Foundation. 2010.