- Maladie d'Alzheimer
-
Maladie d'Alzheimer
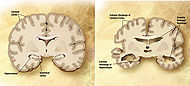
Classification et ressources externesComparaison d'un cerveau normal âgé (gauche) et du cerveau d'un patient atteint d'une maladie d'Alzheimer (droite). CIM-10 G30., F00. CIM-9 331.0, 290.1 OMIM 104300 DiseasesDB 490 MedlinePlus 000760 eMedicine neuro/13 MeSH D000544 GeneReviews alzheimer
La maladie d'Alzheimer est une maladie neurodégénérative incurable du tissu cérébral qui entraîne la perte progressive et irréversible des fonctions mentales et notamment de la mémoire. Elle fut initialement décrite par le médecin allemand Alois Alzheimer (1864-1915).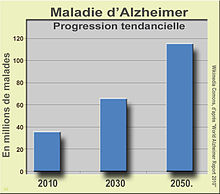 Nombre de malades attendus, selon un scenario tendanciel ("World Alzheimer Report 2010"[1])
Nombre de malades attendus, selon un scenario tendanciel ("World Alzheimer Report 2010"[1])
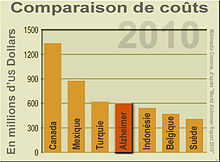 Comparaison du coût de la maladie dans le monde (2010) avec le budget de différents états ("World Alzheimer Report 2010")[1].
Comparaison du coût de la maladie dans le monde (2010) avec le budget de différents états ("World Alzheimer Report 2010")[1].
Principale cause de démence chez les personnes âgées, elle touche environ 26 millions de personnes dans le monde en 2005 et pourrait en toucher quatre fois plus en 2050 selon l'ouvrage « Global prevalence of dementia: a Delphi consensus study »[2]. Généralement diagnostiquée à partir de l'âge de 65 ans, les premiers signes de la maladie d'Alzheimer sont souvent confondus avec les aspects normaux de la sénescence ou d'autres pathologies neurologiques comme la démence vasculaire ce qui fit qu'elle fut sous-diagnostiquée jusque dans les années 1960.Aux États-Unis, elle a couté en 2008 94 milliardsUS$ à l'assurance maladie américain<refEchSour2011>Nouvelles percées concernant la maladie d’Alzheimer avec des souris transgéniques ; L'écho des souris, 2011(09-03</ref>. Et elle était en 2010 dans les pays développés l'une des maladies les plus coûteuses : 604 milliardsUS$. Selon le "World Alzheimer Report 2010", 35,6 millions de personnes vivent avec une maladie d'Alzheimer dans le monde. Elles seront 65.7 millions en 2030 et 115,4 millions en 2050.
Le diagnostic de la maladie repose essentiellement sur des tests neuropsychologiques et sur la mise en évidence d'une atrophie corticale qui touche d'abord le lobe temporal interne et notamment l'hippocampe, régions importantes pour la mémoire. Les premiers symptômes consistent en des pertes de souvenir (amnésie) qui se manifestent initialement par des distractions mineures qui s'accentuent avec la progression de la maladie, tandis que les souvenirs plus anciens sont relativement préservés. L'atteinte neurologique s'étend par la suite aux cortex associatifs frontaux et temporo-pariétaux, se traduisant par des troubles cognitifs plus sévères (confusions, troubles de l'humeur et des émotions, des fonctions exécutives et du langage) allant jusqu'à la perte des fonctions autonomes et la mort. La vitesse et l'évolution de la maladie sont variables d'un individu à l'autre rendant difficile tout pronostic précis, ainsi l'espérance de vie varie de 3 à 8 ans selon l'âge du patient au moment du diagnostic[3]. Les changements psychologiques induits par la maladie influent sur les qualités humaines essentielles et pour cette raison la maladie d'Alzheimer est quelquefois décrite comme une maladie où les victimes subissent la perte de qualités qui forment l'essence de l'existence humaine.
En 2010, il n'existe pas de traitement efficace contre la progression de la maladie. Les interventions proposées sont principalement d'ordre palliatif et n'ont qu'un effet limité sur les symptômes. Étant donné la prévalence de la maladie, un important effort est mené par l'industrie pharmaceutique pour découvrir un médicament qui permettrait de stopper le processus neurodégénératif. La principale piste de recherche vise à s'attaquer aux plaques amyloïdes qui se forment entre les neurones au cours de la maladie et aux agrégats de protéines tau formant les dégénérescences neurofibrilaires à l'intérieur des neurones.
Bien que les causes exactes de la maladie d'Alzheimer restent encore mal connues, on suppose que des facteurs génétiques et environnementaux contribuent à son apparition et à son développement. Des mutations génétiques ont été identifiées dans les cas familiaux à début précoce qui représentent moins de 5 % des patients atteints par la maladie d'Alzheimer. Pour la forme la plus courante, dite « sporadique », les allèles de plusieurs gènes (codant notamment pour l'apolipoprotéine E) augmentent le risque de développer la maladie. Alors que l'hygiène de vie joue un rôle avéré dans le risque d'apparition et de progression de la maladie, diverses études épidémiologiques et toxicologiques ont aussi mis en exergue des facteurs de risques environnementaux tels que la présence de métaux comme l'aluminium dans l'environnement, tout particulièrement sous forme hydrique (Henri Pézerat, André Picot et l'étude Paquid menée par l'Inserm dans 75 communes françaises[4]). Évoquant le doute, les autorités sanitaires et politiques (conférence de presse du ministère de la Santé, 14 octobre 1998) n'ont pas encore décidé de réduire les normes applicables aux taux d'aluminium dans l'eau de consommation. De même, ont été soulevés le problème de l'exposition à des solvants ou aux champs électromagnétiques ou encore le contact avec les métaux lourds (notamment le mercure des amalgames dentaires). Mais, à l'heure actuelle, la communauté médico-scientifique ne s'accorde pas sur l'interprétation des résultats de recherche.
Historique
Alois Alzheimer (1864-1915) est un psychiatre et un neuropathologiste allemand du début du XXe siècle qui étudia le cerveau des personnes atteintes de démence, grâce à une nouvelle technique de coloration à l'aniline et des imprégnations argentiques.
En 1907, Alois Alzheimer décrivit pour la première fois les altérations anatomiques observées sur le cerveau d'une patiente de 51 ans, Auguste D. Atteinte de démence, elle présentait également des hallucinations visuelles et des troubles de l'orientation. En 1911, Alzheimer découvrait un cas identique à celui d'Auguste D.
C'est le psychiatre Emil Kraepelin (1856-1926) qui proposa que la maladie porte le nom d'Alzheimer, du nom de son découvreur.
L'après-baby boom (ou papy boom), la maitrise de la fécondité et le progrès médical conduisent les sociétés à devoir vivre une période où les personnes âgées seront très nombreuses. Cette maladie fait donc l'objet d'une attention particulière, notamment en France avec l'observatoire national sur la recherche sur la maladie d'Alzheimer (ONRA)[5].
En 2009, la maladie d'Alzheimer explique plus de la moitié des cas de démence de la personne âgée dans les pays riches.
Épidémiologie
On distingue deux formes de la maladie d'Alzheimer : la forme « familiale », plus précoce, qui a, au moins en partie, une origine génétique, et la forme dite « sporadique » qui est la forme la plus répandue de la maladie. Le facteur de risque pour cette dernière forme augmente fortement avec l'âge, ce qui en fait, à l'échelle mondiale, la troisième cause d'invalidité pour les plus de 60 ans (après les atteintes de la moelle épinière et les cancers en phase terminale[2]) avec une prévalence de l'ordre de 4 à 6 % à cet âge[2]. Ces chiffres proviennent essentiellement des études épidémiologiques effectuées dans les pays développés, en effet bien que cette maladie s'observe sur tous les continents, elle est peu caractérisée dans les pays en voie de développement où l'espérance de vie est souvent plus courte et les enquêtes épidémiologiques plus rares. La maladie d'Alzheimer est donc considérée comme une pandémie[6].
À part l'âge, les autres facteurs de risque de la maladie sont mal connus et les chercheurs se tournent de plus en plus vers la recherche de causes environnementales[7]
En effet :
- L’incidence - aux mêmes âges - est (sauf au Japon, et moindrement en Amérique centrale et du Sud) toujours plus forte dans les pays riches qu'ailleurs.
- Ceci est vrai pour les populations urbaines supposées plus exposées aux pollutions, mais aussi pour les populations rurales (qui par exemple en Inde développent 5,4 fois moins d'Alzheimer qu'en Pennsylvanie[8]). De même les Afro-Américains vivant aux États-Unis sont-ils beaucoup plus touchés que les Yorubas du Nigeria. Des chercheurs ont comparé l'incidence de Maladie d'Alzheimer (MA) dans une population Yoruba du Nigeria et chez des Afro-Américains génétiquement proches : fréquence comparable (26 à 29 %) et élevée d'allèles APOE4[9], mais le risque de MA pour ces individus est deux fois moindre au Nigeria (1,15 %) qu'en Amérique du Nord (2,52 %) à âge égal, ce qui plaide aussi pour une cause environnementale, au moins dans 50 % des cas[10].
Cette maladie est plus rare en Asie (alors que la population chinoise connait aussi un vieillissement important suite à la politique de contrôle de la natalité soutenue par son gouvernement depuis les années 1960)[11]. Le Japon est une exception pour les pays industrialisés et riches. La prévalence de la maladie y est presque 10 fois plus faible qu'en France. - un Japonais vivant à Hawaï ou aux États-Unis voit son niveau de risque augmenter (5,4 % pour les Japonais d’Hawaii) et se rapprocher de celui d'un Américain moyen, d'un Caucasien ou Européen[11],[12].).
- De même 5,7 % des Japonais ayant émigré au Brésil ont après quelques décennies le même risque de développer la maladie qu'un Brésilien moyen[13],[14].
- Au Japon, l'Alzheimer est rare, mais la démence vasculaire est - comme aux USA - très élevée, probablement en raison d'une consommation trop importante de sel. Cette maladie diminue au Japon grâce à la prévention et à une prise en charge plus efficace de l'hypertension[15]. L'exception japonaise pourrait être expliquée par le fait que, suite à la catastrophe de Minamata et de Niigata au Japon, le mercure a été banni de nombreux usages et notamment des amalgames dentaires. Le fait que cette maladie n'ait pas progressé au Japon, alors qu'on y a aussi constaté une augmentation des caries induites par la nourriture industrielle, les sucreries et boissons gazeuses sucrées suggère que le mercure serait bien en cause, et non le sucre, ou un phénomène infectieux lié à la carie elle-même. L'espérance de vie en bonne santé y est par ailleurs parmi les meilleures au monde, ce qui n'est pas le cas en France ou en Belgique par exemple. L'espérance de vie est aussi la plus élevée au monde pour les Japonaises.
Épidémiologie prospective
Dans le monde, le nombre de cas de malades d'Alzheimer est passé de 11 millions en 1980 à 18 millions en 2000 et 25 millions en 2004[16].
En Europe, l’incidence des démences devrait croître en 50 ans de 1,9 million de nouveaux cas par an à 4,1 millions, selon les scenarii[17].
En Belgique, 5 à 10 % des plus de 65 ans sont touchés et près de 20 % des plus de 80 ans[18].
En France, l'étude « PAQUID » (1988-2001) a fait ressortir que 17,8 % des personnes de plus de 75 ans sont atteintes de la maladie d'Alzheimer ou d'un syndrome apparenté. D'après une évaluation ministérielle de 2004, environ 860 000 personnes seraient touchées par la maladie d’Alzheimer en France. Un chiffre qui pourrait atteindre 1,3 million en 2020 et 2,1 millions en 2040. Le nombre de nouveaux cas est d'environ 225 000 par an[19]. La prévalence des démences chez les plus de 75 ans atteint presque 18 % (maladie d’Alzheimer à 80 %)[20]. Ceci représente environ 900 000 malades (et dans les années 2000 environ 220 000 nouveaux cas par an), avec des tendances et projections très alarmantes : 1 200 000 malades en 2020, et plus de 2 000 000 vers 2040[21].
Facteurs de risque
- l'âge essentiellement (supérieur à 65 ans),
- antécédents familiaux de maladie d'Alzheimer, ou existence de mutations spécifiques (préséniline, APP),
- hypertension[22],[23]. Un traitement contre l'hypertension limite le risque de mourir précocément, mais aussi celui d'être admis pour une longue durée dans un centre de soins (risque diminué de 49 %), pour des raisons encore incomprises. De manière générale, l'hypertension est un facteur de risque de démence[23]. Certains se demandent même si la MA n'est pas une maladie vasculaire plutôt que neurodégénérative[24], notamment liée à une hypoperfusion cérébrale[25] et à une mauvaise irrigation du cerveau[26], comme dans d'autres formes de démence peut-être.
- maladies cardiovasculaires relativement précoces (à partir du milieu de vie) [27],[28],[29],[30]
- l'isoforme 4 de l'apolipoprotéine E (rarement recherché)
- antécédents personnels de dépression, de traumatisme crânien (coups, secousses importantes...), d'exposition au mercure en particulier dentaire.
- Cholestérolémie[31]
- Il a été question que l'exposition à l'aluminium soit aussi en cause, mais cette hypothèse est en déclin et a toujours été controversée,
- Certains indices suggèrent une relation causale entre l'exposition au mercure et la maladie d'alzheimer[32]. En revanche, les amalgames dentaires contenant du mercure ont fait l'objet de nombreuses études qui n'apportent pas la preuve de leur responsabilité au regard des maladies neurodégénératives[33],[34]
- un régime pauvre en acides gras polyinsaturés oméga-3 et riche en acides gras saturés[35],
- la consommation modérée d'alcool aurait un facteur protecteur (effet indirect controversé). L'alcoolisme (consommation chronique ou ivresses passagères même légères) est par contre un facteur de risque avéré.
- Le tabagisme augmenterait sensiblement le risque de survenue de la maladie d'Alzheimer[36].
- personnes porteuses de trisomie 21 (syndrome de Down)[37],[38],[39].
Aspects cliniques et circonstances de découverte
On distingue trois stades dans la maladie d'Alzheimer[40] : 1) le stade léger (ou premier stade) 2) le stade modéré (ou deuxième stade) 3) le stade avancé (ou troisième stade).
La maladie d'Alzheimer débute habituellement par des troubles de la mémoire. Certains patients remarquent que leur mémoire fonctionne moins bien qu'autrefois et consultent leur médecin pour cela. Chez d'autres patients, l'entourage plus que le patient lui-même remarque ses difficultés de mémoire. Les symptômes liés à la mémoire (plainte mnésique) ne sont pas spécifiques de la maladie d'Alzheimer ou d'autres démences, et peuvent être rencontrés dans diverses conditions : dépression, anxiété, surmenage, consommation de médicaments psychotropes, syndrome d'apnée du sommeil notamment.
Une étude épidémiologique française ayant porté sur 3000 sujets suivis durant 14 ans a rétrospectivement démontré l'existence de signes précurseurs 12 ans avant le diagnostic[41]. Une autre étude portant sur 10 000 personnes suivies dans 3 villes françaises doit vérifier si des signes encore plus précoces peuvent être détectés.
La maladie d'Alzheimer peut aussi se manifester par des symptômes autres que ceux liés à la mémoire. Une dépression peut être un des premiers signes. Une perte d'indépendance fonctionnelle définie par la nécessité d'une aide humaine dans les gestes de la vie quotidienne est aussi une situation qui doit faire évoquer cette maladie.
D'autres circonstances de découverte sont possibles : chutes répétées, amaigrissement, troubles du comportement.À un stade plus évolué (à partir du deuxième stade), d'autres troubles cognitifs apparaissent progressivement: altération du langage, des gestes et de la motricité, altération de la communication.
Anatomo-pathologie
Le cerveau du patient est victime d'un double processus de dégénérescence et d’inflammation, caractérisé par deux types de lésions locales participant à une lésion plus globale du cerveau :
Les plaques séniles (ou plaques amyloïdes)
Article détaillé : plaque amyloïde.Ces plaques, essentiellement localisées dans le néocortex et l'hippocampe, correspondent à l'accumulation extracellulaire d’un peptide dit « β-amyloïde » (PbA) ou « peptide Aβ42 » (42, parce que constituée de 42 acides aminés). Cette protéine est en fait la forme clivée et anormale d'une glycoprotéine membranaire dite « protéine précurseur de la protéine β-amyloïde » (ou APP). C'est une protéine pathogène (neurotoxique) et insoluble qui est aussi la forme la plus amyloïdogène du bêta-amyloïde. C'est une enzyme, la β-secretase qui provoque, pour des raisons encore mal comprises, le clivage anormal de la protéine APP (Amyloïd Protein Precursor).
En temps normal cette protéine de la membrane des neurones est clivée par des secretases en peptide p3 non neurotoxique. La responsabilité de toxiques tels que le mercure accumulé dans le cerveau sous sa forme ionisée divalente (Hg2+ ; pro-oxydant, à forte affinité pour les groupements soufrés thiols) est suspectée... voir plus bas le chapitre consacré à l'épidémiologie de la maladie).
Cette anomalie permettrait une entrée anormale de calcium dans le neurone, ce qui activerait la microglie (réaction inflammatoire), entraînant la mort inéluctable du neurone par nécrose ou par apoptose.Les dégénérescences neurofibrillaires
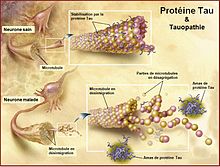
Article détaillé : protéine tau.Des lésions cellulaires semblent consécutives à une augmentation de la capacité de phosphorylation (estérification des fonctions alcool des acides aminés hydroxylés) de la protéine Tau (macromolécule essentielle à la stabilité de la tubuline (protéine constituant majoritairement l'assemblage des microtubules qui forment le cytosquelette des axones neuronaux)). Ces lésions semblent induites par l'accumulation anormale d'un dérivé de la protéine tau hyperphosphorylée, responsable de la formation de filaments appariés : quand la protéine tau est hyperphosphorylée, elle se détache des microtubules, et va se conformer en paire de filaments hélicoïdaux pathologiques, qui s'agrégent en amas de neurofibrilles causant une neurodégénérescence fibrillaire progressive. Les substances nécessaires au fonctionnement du neurone ne pouvant plus être acheminées jusqu'au corps cellulaire, le neurone finit par mourir.
L’atrophie corticale
Chez les patients atteints de la maladie d'Alzheimer, le cerveau peut perdre 8 à 10 % de son poids tous les dix ans, contre 2 % chez un sujet sain. L'atrophie corticale s'accompagne d'une dilatation des ventricules cérébraux et des sillons corticaux ainsi que d'une perte neuronale affectant particulièrement le système cholinergique (noyau basal de Meynert, septum, cortex entorhinal, amygdale et hippocampe).
Étiologie
Génétique de la maladie d'Alzheimer
Formes génétiques
Moins de 1 % [44] des malades présentent une maladie d'Alzheimer d'origine purement génétique. Cette forme se caractérise par :
- l'apparition des signes avant 30 ans ;
- une transmission autosomique dominante (la moitié de chaque génération est atteinte).
Deux mutations de gènes sont impliquées :
- une mutation du gène APP située sur le chromosome 21 qui code un précurseur de la protéine amyloïde (cinq mutations du codon 717 sont connues) ;
- une mutation du gène PSEN1 située sur le chromosome 14 (nombreuses mutations qui sont des mutations faux-sens).
Prédispositions génétiques
Les formes dites sporadiques, c'est-à-dire non-familiales, semblent souvent comporter une prédisposition génétique :
- En 1993, l' APOE4 (l'allèle 4 du gène de l'apolipoprotéine E) a été démontré significativement lié à une augmentation de risque de la maladie d'Alzheimer. Mais la présence de l' APOE4 n'est ni nécessaire ni suffisante pour développer la pathologie ;
Le gène de l'apolipoprotéine E est présent sous trois formes alléliques : l'APOE2, APOE3, et APOE4. Le premier se rencontre dans 51% de la population, le deuxième se rencontre dans 80 % de la population et le troisième se rencontre dans 15 % de la population ;
- - la présence de l' APOE4 sous la forme hétérozygote (1 allèle APOE4) multiplie par 2 le risque de maladie d'Alzheimer (par rapport aux personnes ne possédant pas cet allèle) ;
- - la présence de l' APOE4 sous la forme homozygote (2 allèles APOE4) multiplie par 11 le risque de maladie d'Alzheimer (par rapport aux personnes ne possédant pas cet allèle).
Cette apolipoprotéine E interviendrait dans les mécanismes de réparation neuronale.
- En 2009, le gène de la clusterine a été ajouté à ce début de liste[45]
- En 2009, toujours, un gène codant la protéine PICALM (phosphatidylinositol-binding clathrin assembly protein) contribuant au système immunitaire, CR1 (récepteur 1 du composant 3b/4b du complément) a aussi été ajouté fortement suspecté[46].
Le mercure comme cause possible pour les cas "non-familiaux" ?
Pour les cas n'ayant pas d'origine génétique, un nombre croissant d'indices désignent le mercure comme cause possible ;
- Ce mercure aurait pour principale origine les plombages dentaires : l’OMS considère que le mercure-vapeur émis par les amalgames dentaires est la 1re source d’exposition mercurielle des populations occidentales[47].
Les amalgames perdent environ 50 % de leur mercure (soit 1/2 gramme environ par amalgame), en 10 ans, avant stabilisation, et de nombreuses études récentes ont confirmé que le taux de mercure du cerveau est corrélé au nombre d’amalgames[48],[49],[50],[51],[52].
Une revue[53] (monographie) des connaissances et études récentes, faite par J. Mutter montre une grande cohérence des études disponibles, et une étude suédoise récente laisse penser que les dentistes et leurs assistant(e)s sont effectivement 2 à 3 fois plus touchés par un type de cancer du cerveau (gliome), rare et pouvant être ici relié au mercure. Boyd Haley et ses collègues (Université du Kentucky) ont récemment montré comment le mercure induit une neurodégénérescence caractéristique de la MA, suite à une exposition chronique à de faibles doses de mercure-vapeur[54].- Une étude (de faible puissance statistique et portant sur des vétérans de l'US Army) avait en 1993 mis en évidence un taux 7 à 8 fois plus élevé de caries racinaires chez les victimes de maladie d'Alzheimer par rapport à un groupe témoin (apparié pour l’âge et le niveau d’éducation)[55]. Par ailleurs le nombre de plombages dentaires est bien corrélé au taux de mercure mesuré dans le cerveau[56] et c'est le mercure inhalé qui passe le mieux et plus directement au travers des poumons et qu'il est facilement stocké dans le cerveau qu'il gagne aisément grâce à sa lipophilie partielle. Ce sont les cellules gliales qui le stockent durablement, pour des dizaines d'années, sous forme d'un complexe insoluble soufré de cations mercuriques (Hg2+), après qu'il y a été oxydé par le peroxyde d’hydrogène dans une réaction catalysée par une catalase (la peroxydase). Il peut alors exercer son activité bien connue de neurotoxique.
- En 2006, une étude suédoise montrait que les Suédois victimes de la maladie d'Alzheimer avaient plus souvent des problèmes dentaires que les non-malades[57].
- Chez le rat de laboratoire exposé à du mercure, on observe des processus de dégénérescence du cerveau, semblables à ceux de la maladie d'Alzheimer. Le cerveau de rats de laboratoire exposés à une dose de mercure-vapeur équivalente à celle de quelques amalgames dentaires, présente les mêmes anomalies moléculaires que celles qu'on observe à l'autopsie de 80 % des cerveaux de patients morts après une M.A. Et la gravité de l'anomalie est bien corrélée au taux de mercure mesuré dans le cerveau[58].
- On mesure un taux de mercure plus élevé dans le cerveau des malades d'Alzheimer, et tout particulièrement dans le noyau basal de Meynert au centre de l'encéphale, là où la dégénérescence neuronale est la plus forte chez les malades[59],[60].
- Les malades ont presque toujours un taux de mercure sanguin anormalement élevé (2 à 3 fois plus élevé que pour l'échantillon témoin)[61] et le taux sanguin du mercure est plus élevé chez les malades qui ont le plus de protéines β-amyloïdes se déposant dans le cerveau.
- Le mercure et d'autres métaux lourds ont une affinité pour les groupements thiols, or la tubuline possède plusieurs cystéines, un acide aminé possédant une fonction soufrée thiol (indispensable à la polycondensation de cette protéine cytosolique et c'est cette polycondensation qui forme les microtubules rigides, principaux constituants du cytosquelette des neurones, nécessaire au transport axoplasmique qui nourrit le neurone. Les fonctions thiol ont une affinité très élevée pour les cations mercuriques hydrosolubles[62], elles interviennent d'ailleurs dans les phénomènes naturels de détoxication des métaux lourds.
- In vitro, de faibles doses de mercure inorganique (Hg2+) suffisent à inhiber la production de glutathion par les neuroblastomes (cellules neuronales modifiées). Le glutathion est un tripeptide soufré normalement très présent dans le cerveau qu'il protège en tant que puissant antioxydant du milieu cellulaire. À faible dose, le mercure induit aussi (démontré expérimentalement chez le porc) une hyperphosphorylation des protéines Tau et un dépôt de protéine β-amyloïde, deux caractéristiques de la MA[63].
- la mélatonine est une hormone essentielle, produite par la glande pinéale (ou épiphyse), synchronisant les biorythmes, mais jouant aussi un rôle antioxydant et protégeant les neurones du mercure. On connaissait l'effet cytotoxique du mercure via le stress oxydatif, mais des chercheurs ont montré dans les années 2000 qu'il augmente aussi la sécrétion de bêta-amyloïde et la phosphrylation des protéines Tau dans les cellules de neuroblastome SHSY5Y. Ils ajoutent que la mélatonine protège bien les neurones contre l’action oxydante des cations mercuriques[64].
- In vitro, dans une culture de tissu cérébral humain, de très faibles doses de mercure inorganique suffisent à inhiber la phosphorylation de la tubuline par la guanosine-triphosphate (GTP), co-facteur nécessaire à la construction des microtubules, alors que d'autres métaux (même neurotoxiques connus comme le plomb, y compris sous leur forme ionisée) n'ont pas cet effet, pas plus que le fer ou le zinc ou l’aluminium, un temps suspectés[65].
- Le mercure inhibe la fixation des riboses sur l’adénosine diphosphate (ADP ; co-enzyme nucléotidique de la tubuline), ce qui inhibe la polycondensation de cette protéine (30), entraînant la formation d’amas neurofibrillaires cytotoxiques[66].
- Des neurones mis en culture dégénèrent quand ils sont exposés à de très faibles doses de mercure inorganique ionisé (Hg2+) avec, dans le même temps, formation d’amas de neurofibrilles. L'Université de médecine de Calgary a produit une vidéomicroscopie qui montre qu'une dose infime de (10-7 Mol) mercure suffit à mettre à nu une gaine de microtubules, par perte des neurofibrilles qui se dépolymérisent progressivement (Voir la vidéo). Cet effet n’est pas retrouvé avec d’autres métaux neurotoxiques : aluminium, plomb, manganèse[67].
- Des cultures de cellules souches de neurones ont été exposées à de faibles taux de mercure inorganique : celui-ci y bloque les fonctions de la tubuline, et induit la mort des cellules, par apoptose, ainsi que la formation de protéines connues pour être chaperonnes du stress thermique[68].
- Des chélateurs (molécules captant les métaux) associés à des antioxydants permettent une solubilisation de la protéine β-amyloïde (PbA). C'est un indice de plus en faveur d'une responsabilité du mercure dans l'accumulation de cette protéine pathogène[69]. Un métabolisme anormal (homéostasie cellulaire perturbée) de deux autres cations métalliques (cuivre et zinc, nécessaires au fonctionnement du cerveau) serait également associé à l'apparition des plaques amyloïdes. Débarrasser le cerveau de ses excès de certains métaux pourrait être une piste thérapeutique contre la MA[70].
- In vitro, le mercure interagit négativement avec le glutamate (neuromédiateur excitateur) dont il perturbe la synthèse et le transport[71],[72]. Or le glutamate est essentiel pour le cerveau et la mémoire, mais ne doit pas être présent en excès. Dans la fente synaptique, les cations mercuriques (à dose micromolaire, 10-6 Mol), freinent la capture du glutamate par les astrocytes, en se fixant sur les fonctions thiols des transporteurs protéiques du glutamate[73]. Le glutamate s'accumule et devient hyperexcitant, au point de tuer les cellules nerveuses.
In vivo, le liquide cérébrospinal des M.A contient toujours un taux anormalement élevé de glutamine-synthétase (GS), ce qui peut être dû au fait que le mercure inorganique freine l’activité de la GS dans les astrocytes bien plus efficacement que le cation méthylmercure (...avec une relation dose-dépendante, et même à très faible dose puisque 5 μM de mercure inorganique durant 6 heures suffisent à diminuer de 74 % l’activité de la GS)[74]. Le mercure, en augmentant le taux de glutamate excitotoxique peut entrainer la lyse d'astrocytes[75].
Le taux d'adénosine triphosphate (ATP) des cellules neuronales est en outre piloté par une enzyme (la créatine kinase, ou CK), qui est également vulnérable aux cations mercuriques car possédant un grand nombre de fonctions thiols. Or on constate aussi un taux anormalement bas de cette enzyme dans les zones du cerveau les plus affectées par la MA[76],[77].- L'effet toxique du mercure est aggravé chez les personnes génétiquement moins aptes à sa détoxication. Or, cette susceptibilité génétique au mercure (liée au polymorphisme du gène de l’apolipoprotéine E ou APOE) est corrélée à un risque beaucoup plus élevé de développer une MA, et de la développer plus jeune[78],[79]. Un trouble cognitif léger a aussi plus de valeur prédictive chez ces derniers[80]. Ce gène APOE existe sous 3 formes (allèles APOE2, APOE3 et APO4). L'APOE 2 est plutôt protecteur, alors que l'APOE4 expose au risque maximal (y compris pour l'âge)[81],[82],[83]. Par exemple, un caucasien homozygote pour APOE2 a 25 fois moins de risques de MA que son homologue homozygote pour APOE4 (OR =0,6 vs 14,9). C'est un argument de plus en faveur de la responsabilité du mercure.
Les mécanismes cellulaires à la base de la dégénérescence neuronale
Il existe deux niveaux de mécanismes : intra- et extracellulaires.
Dans les deux niveaux, il y a une accumulation de protéines qui entraîne un dysfonctionnement de la cellule. Dans les mécanismes intracellulaires, cette accumulation s'appelle neurofibrilles. Dans les mécanismes extracellulaires, elle s'appelle plaques amyloïdes.Le milieu intracellulaire
Dans les microtubules, les protéines Tau se positionnent perpendiculairement à l'axone en assurant la rigidité des microtubules et un bon transport axonal.
Normalement, des protéines Tau se détachent périodiquement des microtubules, mais sont remplacées et rapidement dégradées chez le sujet sain.
La maladie d'Alzheimer est caractérisée par des protéines Tau se détachant des microtubules, et tombant dans le milieu intracellulaire. Elles ne sont pas toutes dégradées et vont donc s'agréger. C'est cela qui va former les neurofibrilles. Trop de neurofibrilles bloquent le fonctionnement du neurone et ne permettent pas le bon transport axonal. Les neurofibrilles compriment le neurone et provoquent une mort neuronale.Il existe plusieurs explications au détachement des protéines Tau :
- La phosphorylation : c'est ce qui permet la fonctionnalité de la protéine. La protéine Tau est très peu phosphorylée et lorsqu'elle est très phosphorylée, elle ne peut pas s'attacher aux microtubules. Ce sont donc les protéines qui se détachent et s'accumulent en formant des neurofibrilles. Dans cette explication, la cause de l'augmentation de la phosphorylation est inconnue.
- Une hypothèse avance que les radicaux libres, dus à la présence de la bêta amyloïde, détériorent la paroi membranaire des axones et laissent ainsi pénétrer des ions calcium et des fragments de bêta amyloïde qui vont ainsi sur-activer les map kinases chargées de contrôler la phosphorylation des protéines Tau. Ces protéines vont donc recevoir 5 à 9 groupements de phosphates, au lieu de 2 à 3, et leur schéma de construction va changer. Les protéines Tau, qui renforcent les microtubules chargées de former le cyto-squelette des axones, vont s'agglomérer en forme hélicoïdale double (neurofibrille) et donner à l'axone la forme en spirale typique que l'on rencontre dans le cas de la dégénérescence neurofibrillaire de la MA. L'axone ne va plus fonctionner et cela va contribuer au mécanisme d'apoptose cellulaire jusqu'à la mort du neurone.
- Les coupures protéolytiques des protéines Tau, qui sembleraient intervenir de façon précoce et seraient un événement concomitant à l'hyperphosphorylation de ces protéines.
- Les facteurs génétiques : comme pour toutes les protéines, il existe un gène qui code la protéine Tau. Le gène peut avoir sept allèles différents. Ces sept allèles peuvent être classés en deux catégories :
- ceux à trois motifs R[84] ;
- ceux à quatre motifs R.
Les protéines Tau qui proviennent des allèles à trois motifs R ont une fixation moins importante que les protéines qui proviennent des allèles à quatre motifs.
Dans le corps neuronal proprement dit, la membrane étant abîmée par les radicaux libres, les ions calcium et des fragments bêta amyloïde (AB) vont également pénétrer et activer les phospho kinases a calcium (pkc) dont le rôle est d'éliminer la membrane neuronale abîmée. Le PKC suractivé va éliminer des portions de membrane saines et accélérer le processus de destruction. Les radicaux libres et les fragments d'AB vont pénétrer en surnombre dans le corps du neurone, affecter son fonctionnement et contribuer à l'apoptose (mort cellulaire programmée).
Le milieu extracellulaire
Dans le milieu extracellulaire, la protéine mise en jeu est la protéine amyloïde. C'est une protéine membranaire (située sur la membrane de la cellule). Cette protéine se détache de la membrane, et entre dans le milieu extracellulaire. Elle est ensuite récupérée puis dégradée.
Chez les patients atteints de la maladie d'Alzheimer, cette dégradation n'est pas totale et un fragment, appelé β-amyloïde, reste et ne peut être dégradé. Ces fragments finissent par s'agréger et par former des plaques amyloïdes. En s'accumulant dans le milieu extracellulaire, ces plaques compriment les neurones. C'est ce phénomène qui entraîne un dysfonctionnement, qui peut être suivi de la mort neuronale.
En outre, ces plaques séniles vont libérer un peroxyde de formule H2O2. La liaison entre les deux atomes d'oxygène étant très faible, elle va rapidement se cliver. On obtiendra alors deux molécules OH°, appelées radicaux libres. Les radicaux libres ne respectent pas la règle de l'octet, ils sont donc instables. Ils vont chercher à coupler leur électron libre. Pour ce faire, ils vont arracher un atome d'hydrogène à la membrane du neurone (composée de molécules carbonées présentant de nombreux atomes d'hydrogène). La membrane "trouée" va donc laisser pénétrer d'autres radicaux libres qui s'attaqueront à l'ADN du neurone, entraînant la destruction des fonctions de la cellule privée d'information génétique.
La cause de l'accumulation apparaît aussi avec le vieillissement normal, mais l'accumulation à la base de l'Alzheimer est peu connue.
Le seul facteur est un facteur génétique. Cela concerne une autre protéine qui agirait avec ce processus de formation des plaques amyloïdes. Elle s'appelle l’apolipoprotéine E. cette protéine dépend d’un allèle qui peut être de trois sortes : E2, E3 et E4.
Les allèles E2 et E3 sont spécifiques de l’espèce humaine. Ils proviennent d’une mutation du gène E4. L’allèle le plus répandu est l’allèle E3 (70%), suivi de l’allèle E4 (20%) puis de l’allèle E2 (10%).
L’allèle E4 est associé à la formation des plaques amyloïdes. Cet allèle permettrait l’inhibition de la croissance neuritique (formation des axones et des dendrites). Cette croissance permet la plasticité neuronale. Ce phénomène est très important pour le fonctionnement du système nerveux central. L’allèle E4 est par conséquent associé aux maladies du dysfonctionnement neuronal. L’allèle E3 favorise la plasticité neuronale, mais pas autant que l’allèle E2. C'est pour cette raison que l’allèle E2 est associé à la longévité.L'apparition de la maladie
Afin d'étudier l'apparition de la maladie, des souris transgéniques (génétiquement modifiées) sont utilisées. Chez certaines souris, le gène codant la protéine Tau est muté. Chez d'autres, c'est le gène codant la protéine amyloïde qui est muté. Certaines souris vont subir des mutations sur les deux gènes.
Les souris ayant eu une mutation sur le gène codant la protéine Tau montrent une apparition de la maladie peu prononcée. Les souris ayant eu une mutation sur le gène codant la protéine amyloïde se comportent comme des souris saines. Les souris ayant subi des mutations sur les deux gènes montrent une maladie exacerbée, bien définie.
Cela ne se passe pas obligatoirement de façon identique chez l'homme, mais cela montre que les plaques amyloïdes potentialisent l'apparition de la maladie. Les neurofibrilles apparaissent dans un premier temps, et, lorsque les plaques amyloïdes apparaissent, la maladie se déclenche. Il est certain que chez l'homme, le processus pathologique se développe bien avant que les premiers signes cliniques n'apparaissent.
Diagnostic
Il faut évoquer la possibilité d'une maladie d'Alzheimer devant une ou plusieurs circonstances de découverte : plainte concernant la mémoire, perte d'indépendance fonctionnelle, dépression, troubles du comportement, chutes répétées, amaigrissement.
Le premier temps du diagnostic consiste à rechercher l'existence d'un déficit des fonctions cognitives et doit être réalisé par le médecin généraliste. Pour cela, les médecins disposent de tests simples d'évaluation des fonctions cognitives. L'existence d'anomalies de cette première évaluation cognitive doit entraîner le recours à un médecin spécialiste qui pourra poser ou non le diagnostic de cette maladie.
Le diagnostic de la maladie d'Alzheimer en centre spécialisé est posé en 2 étapes : la première étape recherche l'existence d'un syndrome démentiel (voir critères diagnostiques ci dessous); la seconde étape, réalisée seulement en cas de démence, consiste à rechercher la cause du syndrome démentiel. Pour poser le diagnostic de démence, il est nécessaire de conduire une évaluation détaillée des fonctions cognitives qui est habituellement réalisée par un psychologue.
Aujourd'hui on ne recommande pas de recourir au dépistage de la maladie, c'est-à-dire à la recherche de la maladie chez des personnes qui n'ont aucun symptôme. En effet, en l'absence de traitement curatif, cette stratégie n'est pas pertinente au plan de la santé publique. Par contre, il est recommandé de reconnaitre la maladie chez des personnes qui ont des symptômes ou des signes évocateurs. On parle alors de détection et de diagnostic. Le terme de "diagnostic précoce" est équivoque ! Certains l'utilisent en pensant au diagnostic de maladie d'Alzheimer au stade léger, alors que d'autres pensent au diagnostic de la maladie avant le stade de démence.
L’intérêt de détecter précocement la maladie d'Alzheimer pourra permettre aux personnes atteintes de bénéficier de traitements plus précoces. Selon une équipe de chercheurs français, de nouveaux critères, provenant d’une combinaison entre tests de mémoire, données d'imagerie cérébrale et marqueurs biologiques, pourraient permettre de détecter la maladie d'Alzheimer à un stade précoce, dès les premiers symptômes, « avec un taux de certitude diagnostique supérieur à 90%. » [85]
Critères de démence du DSM-IV
Les critères de démence du DSM-IV reposent sur :
L'installation de troubles intellectuels portant de manière partielle ou complète sur :
- la mémoire : amnésie des faits récents puis anciens,
- des troubles des fonctions exécutives (c'est-à-dire d'organisation et de réalisation d'une tâche complexe, comme par exemple remplir sa feuille de déclaration de revenus),
- des troubles du langage (aphasie amnésique) caractérisés par des "oublis du mot",
- des troubles de la praxie: apraxie (c'est-à-dire de réalisation de gestes complexes : par exemple utiliser la machine à laver),
- une agnosie (troubles de reconnaissance) : par exemple de panneaux routiers, puis de visages etc.
Ces troubles ont un retentissement socio-professionnel.
Leur évolution se fait de manière progressive et irréversible (déclin continu...).
Ces signes ne s'expliquent pas par d'autres causes : ni organique (tumorale, infectieuse, toxique), ni psychique (dépression, schizophrénie), et en dehors d'une confusion aiguë.
Outils d'évaluation
Le diagnostic de maladie d'Alzheimer passe par la constatation d'un mauvais fonctionnement de plusieurs fonctions cognitives.
Outils d'évaluation en milieu non spécialisé- Le MMSE (Mini Mental State Evaluation, ou Test de Folstein), est le test le plus répandu. Il comporte 18 questions ou tâches et il est réalisable en 15 minutes environ. Il fournit un score variant de 0 à 30 points : un score inférieur à 24 sur 30 est suspect de démence ; un score de 28 ou plus est normal. Ce résultat doit cependant être interprété selon le niveau socioéconomique du patient (un haut niveau peut améliorer le score et donc fausser le test), de même qu'il faudra s'assurer de l'absence de confusion avant sa réalisation.
- le test du cadran de l'horloge : il consiste à faire dessiner à la personne le cadran d'une montre ; il est réalisable en 2 minutes environ.
- le test Codex : ce test réalisable en 3 minutes combine une épreuve de mémoire et un test de l'horloge : ces éléments forment un arbre de décision complété pour certains patients par des questions sur l'orientation spatiale.
- le test des 5 mots : ce test évalue la mémoire en distinguant les processus d'encodage et de rappel.
Outils d'évaluation cognitive en milieu spécialisé
Outre les tests précédents, on peut citer- le test de Gröber et Buschke pour explorer la mémoire
- le test Trail Making Test, pour explorer les fonctions exécutives et l'attention
- le test de Stroop pour explorer l'attention
- les test de dénomination, pour explorer le langage
- la copie de figures complexes (ex: La figure complexe de Rey)
Examens complémentaires
Le diagnostic de démence est uniquement clinique et ne nécessite pas d'examen complémentaire. Ces derniers sont utiles pour rechercher l'origine de la démence. Certains examens sont réalisés de façon courante :
- L'IRM est l'examen d'imagerie de choix pour le diagnostic étiologique des démences. Dans la maladie d'Alzheimer, elle peut montrer une atrophie corticale (particulièrement hippocampique), cependant (atrophie corticale ou sous-corticale) se voit dans d'autres maladies de la personne âgée. Cet examen permet aussi d'éliminer d'autres causes : tumeurs, accident vasculaire cérébral, hématome intra-cérébral ou sous-dural, encéphalopathie éthylique... Des indices sont cependant en cours d'évaluation pour tenter de faire un diagnostic précoce (dont la diminution de la taille de l'hippocampe).
- Le scanner cérébral est réalisé si l'IRM est contre-indiquée ou n'est pas réalisable.
- Les dosages plasmatiques de la vitamine B12 et de la vitamine B9 (folates), ainsi qu'un bilan thyroïdien (TSH) sont systématiquement réalisés, car une carence en vitamine B12 ou B9 et une hypothyroïdie peuvent être causes de démence (démence curable).
D'autres examens sont réalisés dans certaines circonstances seulement :
- La tomographie à émission monophotonique (TEMP) qui utilise aussi des marqueurs de perfusion ou du métabolisme cérébral. Cette imagerie fonctionnelle est utile pour le diagnostic étiologique des démences, lorsque les données cliniques ou d'imagerie IRM ne suffisent pas à poser le diagnostic. En particulier, le TEMP est utile pour identifier les démences fronto-temporales.La TEMP peut aussi être réalisée avec des traceurs du système dopaminergique. C'est le Dat-scan, un autre examen d'imagerie isotopique utile pour différencier la maladie d'Alzheimer de la démence à corps de Lewy, une autre démence dégénérative. Dans cette maladie, il y a une hypofixation du traceur au niveau du striatum (zone de fixation normale pour cet examen). La Dat-scan utilise un traceur fixant spécifiquement les transporteurs de la dopamine marquée à l'iode 123.
- La tomographie à émission de positons ou TEP est un examen récent, permettant l'analyse de certains traceurs radioactifs injectés dans l'organisme qui sont des marqueurs de la perfusion ou du métabolisme. On note une diminution assez nette du métabolisme de plusieurs parties du cerveau (lobe temporal, pariétal et postérieur) avec une bonne sensibilité et spécificité. La diminution de l'activité de l'hippocampe serait un indice prometteur. Cet examen n'est pas réalisé de façon courante. Il est utilisé lorsque le diagnostic étiologique de la démence est incertain, malgré l'évaluation clinique et IRM. La TEP peut aussi être utilisée avec des traceurs qui se lient aux plaques amyloides (PIB). Ce type d'examen est réalisé dans le cadre de protocoles de recherche.
- Le dosage dans le liquide céphalo-rachidien de la protéine t-tau, des protéines tau phosphorylées et du peptide amyloïde eta de 42 acides aminés est un appoint au diagnostic conséquent. Ces dosages ne sont pas réalisés en pratique courante, et ils sont pratiqués lorsque le diagnostic étiologique de la démence est incertain. Ils sont réalisés dans certains centres hospitaliers spécialisés.
Diagnostic de certitude
Seule l'autopsie permet un diagnostic de certitude de la maladie d'Alzheimer avec l'examen anatomo-pathologique du cerveau. En pratique, le diagnostic de maladie d'Alzheimer est posé chez une personne présentant des signes de démence d'apparition et d'évolution progressive et pour lesquelles les autres causes ont été éliminées. On n'a pas recours à des biopsies de tissu cérébral (ce qui est dangereux et peu utile). C'est pourquoi, sur la base du diagnotic clinique, on parle de maladie d'Alzheimer probable.
En octobre 2010, un groupe d'experts internationaux vient de proposer une nouvelle définition de cette démence[réf. nécessaire] dans laquelle sont prises en compte les avancées récentes dans ce domaine, et notamment les dosages biologiques (biomarqueurs)[Quoi ?], la clé de son diagnostic. Les patients doivent présenter des troubles épisodiques de la mémoire (des difficultés d'apprentissage d'une liste de mots, notamment) ainsi que des signes biologiques (un biomarqueur positif[Quoi ?] au moins) visibles par des examens de neuroimagerie, notamment une IRM, un PETscan, ou par l'analyse du liquide céphalorachidien (LCR).
Diagnostics différentiels
- au stade initial de la maladie, un oubli bénin lié à l'âge, un déficit cognitif léger ou mild cognitive impairment (MCI), ou encore des troubles cognitifs induits par des médicaments,
- les autres formes de démences d'origine dégénératives, notamment la démence à corps de Lewy, la démence associée à la maladie de Parkinson, les démences frontotemporales, la paralysie supranucléaire progressive, cette dernière démence rare étant une taupathie (ou tauopathie) "pure" dans la mesure où seule la protéine tau semble impliquée.
- les démences dites secondaires (à un trouble organique), dont la plus fréquente est la démence vasculaire
- des troubles anxieux, une dépression : en fait, ces troubles, notamment la dépression, sont parfois associés à la maladie d'Alzheimer. Dans certains cas, pour faire la part des choses, il faut entreprendre le traitement antidépresseur durant un temps suffisant et suivre l'évolution ; la persistance des troubles cognitifs indique qu'il s'agit bien d'une démence[réf. nécessaire].
Si ce bilan étiologique est négatif, on conclut qu'il s'agit de la maladie d'Alzheimer et on parle de maladie d'Alzheimer probable ; le diagnostic ne pourrait être certain qu'après une biopsie avec examen histologique du cerveau. Il n'existe pas de diagnostic de certitude du vivant du patient.
Certains patients ont un tableau de maladie d'Alzheimer et des signes cliniques et/ou radiologiques de lésions cérébrales d'origine vasculaire. On parle alors de démence mixte ou encore de maladie d'Alzheimer avec lésions cérébrovasculaires.
Prévention
Aucune méthode ne protège définitivement de la maladie d’Alzheimer, mais quelques facteurs de diminution du risque sont connus ;
- Les traitements contre l'hypertension [86],[87],[88], et notamment les diurétiques, et surtout ceux qui agissent sur le potassium, ont été associés à un moindre risque de MA[89] Ils diminuent le risque de n'importe quelle forme de démence.
Les antihypertenseurs visant l'angiotensine semblent également diminuer le risque de MA[90] - Conserver une activité cognitive simple pourrait diviser par 2 le risque de MA; les personnes ayant suivi de longues études, ou ayant développé leur mémoire, courent moins de risques de souffrir de la maladie s'ils entretiennent cet acquis[91] telle que lire un journal, jouer aux échecs ou aux dames, fréquenter les bibliothèques, etc. Cette diminution de risque n’est imputable qu’aux activités cognitives actuelles des personnes âgées. Celles pratiquées dans le passé n’auraient aucune influence sur le déclin cognitif lié à l’âge.
- L'exercice physique tout au long de la vie pourrait prévenir le risque de maladie d'Alzheimer chez les sujets à risque (ref), peut être en diminuant le risque d'hypertension et d'accident cardiovasculaire[92].
- Une alimentation pauvre en sel (pour limiter le risque d'hypertension [93]) et riche en vitamines C et E et riche en statines [94] et pauvre en cholestérol[95] serait également protectrice. "Le thé vert aurait une incidence directe sur les fonctions cérébrales, car il contribue à la préservation de ces fonctions et à la réparation des cellules endommagées" [96] et réduirait le risque d'être atteint de démence et d'autres maladies neuro-dégénératives comme le Parkinson et l'Alzheimer [97].
- Détecter plus tôt l'Alzheimer devient possible. Un programme d'intelligence artificielle, né d'une collaboration entre deux laboratoires français (ESPCI ParisTech, ISC-Lyon) et l'institut japonais RIKEN, a appris à distinguer les signes annonciateurs des troubles cognitifs bénins de ceux évoluant vers cette maladie (taux d'erreur : 7%).[réf. souhaitée]
- Le végétarisme : Étant donné les similitudes des symptômes (la démence) et les causes de ces pathologies graves que sont la maladie de Creutzfeldt-Jakob (équivalent humain de l'encéphalopathie spongiforme bovine) et celle d'Alzheimer (qui dont deux maladies neurodégénératives caractérisées par l'accumulation d'agrégats de protéines – quoique de types différentes[98] – formant des dégénérescences au niveau cérébral, quelques études cliniques tendent à démontrer que la consommation de viande (poissons compris[99]) en grande quantité favoriserait le développement de la maladie d'Alzheimer [100],[101],[102],[103],[104]. On invoque notamment dans certaines études le rôle de la méthionine, transformé en homocystéine par le métabolisme intermédiaire. Une hyperhomocystéinémie est un facteur augmentant le risque cardiovasculaire, et semblerait jouer un rôle dans l'apparition de la maladie d'Alzheimer. Cependant il est nécessaire de rappeler que la méthionine est un acide aminé tout à fait indispensable à la vie, qui lorsqu'il est consommé dans les quantités habituelles ne pose aucun problème de santé publique.[réf. nécessaire] Selon certaines théories, la hausse du nombre de cas développant la maladie d'Alzheimer pourrait correspondre à la hausse de la consommation de viande dans le monde[101] : ainsi, une recherche de l’American Society for nutrition, concernant des populations d'Amérique latine, de Chine et d'Inde, conclut que « la consommation de viande a été plus élevée chez ceux dont on a diagnostiqué une démence »[105]. Ce faisant, les populations indiennes pratiquant le végétarisme (depuis des générations) ont un taux d'individus touchés par la maladie d'Alzheimer qui est le plus faible enregistré de par le monde[106],[107].
Traitement
Aucun traitement ne guérit aujourd'hui la maladie d'Alzheimer, ni même ne stoppe son évolution.
Quelques médicaments (anticholinestérasiques et mémantine) freinent son évolution en atténuant les pertes de mémoire, du langage et du raisonnement. Leur efficacité a été établie par des essais en double aveugle contre placebo. Ils n'ont pas d'effet immédiat, mais après 3 à 6 mois d'utilisation, les patients qui ont reçu le traitement ont des fonctions cognitives et une autonomie meilleures que les patients ayant reçu le placebo. Ces traitements retardent le déclin fonctionnel avec des effets perceptibles dans la vie quotidienne par l'entourage des patients.
Les anticholinestérasiques ont des effets secondaires[108], surtout de type digestif (nausées et vomissement). Certains induiraient une surmortalité cardiovasculaire et des tremblements et/ou une aggravation de symptômes parkinsoniens[109] ce qui a été à l'origine de controverses portant notamment sur leur justification économique[110]. Néanmoins, les organismes d'expertise les plus sérieux reconnaissent leur intérêt[111]. Les grandes agences de santé, et en particulier, en France, la Haute Autorité de Santé, recommandent leur utilisation dans la maladie d'Alzheimer.L'approche non-médicamenteuse est une dimension importante de la prise en charge. Des approches très diverses sont proposées. Peu ont une efficacité réellement documentée par des études scientifiques.
- La rééducation / stimulation cognitive a un effet modeste, qui disparait à l'arrêt ; les thérapies occupationnelles visant à stimuler l'attention des malades ont une certaine efficacité[112]. Les interventions envers les aidants familiaux des patients semblent capables de retarder l'entrée en institution gériatrique, en particulier les interventions d'un type éducatif.
- Les aidants familiaux, par leur manière de se comporter, peuvent contrôler (via les neurones miroirs?) les troubles psychocomportementaux des malades. L'éducation des aidants, la notion de "base de sécurité" (un aidant choisi par le malade pour se sécuriser), de constellation d'aidants (autour de l'aidant principal), de tuteur de résilience pour l'aidant, sont autant d'éléments qui font de l'aidant familial un "traitement" en soi[6].
Traitements spécifiques
Il s'agit de médicaments qui sont prescrits spécifiquement dans la maladie d'Alzheimer
Inhibiteurs de l'acétylcholinestérase
Ils inhibent la dégradation de l'acétylcholine, une molécule permettant la transmission entre certains neurones du cerveau par l'intermédiaire de ses synapses. Ainsi, ils visent à corriger le déficit en acétylcholine observé dans le cerveau des personnes atteintes de cette maladie.
Plusieurs inhibiteurs ont été testés de façon rigoureuse (essais randomisés en double aveugle) et ont prouvé une certaine efficacité, dans les formes légères à modérément sévères : le donepezil[113], la rivastigmine, et la galantamine. En 2007 la Commission française de la transparence a réévalué quatre anticholinestérasiques et a conclu à une ASMR mineure[114]. D'après la revue Prescrire leurs effets sont modestes, de quelques mois, chez environ 10 % des patients[115].
Bien que modestes, leurs effets sont significativement supérieurs à ceux du placebo : ralentissement ou retard du déclin cognitif et de la perte d'autonomie.L'effet de ces traitements est stabilisateur et ils ne permettent pas de guérir la maladie, ni de récupérer le niveau de performances préexistant à sa survenue. Leurs utilisations exposent à de nombreuses interactions médicamenteuses, ainsi qu'à des effets indésirables. Ces médicaments sont indiqués dans la maladie d'Alzheimer, et les recommandations de bonne pratique française (Haute Autorité de Santé) et internationales recommandent leur prescription comme traitement de première intention. Ils doivent être introduits le plus tôt possible sans attendre des stades avancés de la maladie.
Antagonistes du NMDA
Les récepteurs neuronaux au N-methyl-D-aspartate (NMDA) jouent un rôle important dans les processus de mémorisation. Comme chez les malades atteints de sclérose latérale amyotrophique, il semble que lors de la maladie d'Alzheimer ces récepteurs soient hyperstimulés par le glutamate, ce qui serait délétère. On ne peut chercher à supprimer le glutamate (il est nécessaire à l’apprentissage et la mémorisation). Il est en outre utilisé pour la synthèse de l’acide gamma-amino-butyrique (GABA), un neurotransmetteur, et du glutathion, tripeptide soufré antioxydant indispensable à la protection cellulaire (35). La mémantine, en entrant en compétition avec le glutamate (neuromédiateur de ce récepteur) est un inhibiteur du NMDA qui a été testé avec des résultats contradictoires sur les signes de la maladie. Elle est réservée aux stades moyens ou avancés[116].
Immunothérapie et vaccin ?
Un vaccin pouvant soigner cette maladie semble envisageable d'après des études menées chez l'animal. Les premiers tests sur l'homme ont été très décevants avec des effets secondaires majeurs (décès observés, et ce sans empêcher l'évolution de la maladie d'Alzheimer). Aucun vaccin ou médicament immunogénique n'est aujourd'hui commercialisé.
- L'idée date de 1999 ; Dale Schenk, un chercheur américain, présentait dans la revue Nature une méthode semblant guérir la maladie chez des souris. En immunisant contre le peptide A bêta des souris transgéniques qui le surexpriment, il arrivait à prévenir l'apparition de dépôts chez les animaux jeunes et à limiter et même réduire leur extension chez les individus âgés.
- Un premier essai clinique de phase 1 chez l'homme conduit ensuite en Angleterre a permis l'analyse suivante : les 80 patients traités supportent bien la vaccination et le quart d'entre eux produisent bien des anticorps. Un second essai a été interrompu en raison d'effets indésirables graves (méningoencéphalites). Le suivi ultérieur des patients qui ont reçu le vaccin est plus mitigé : même si chez certains patients traités les dépôts amyloïdes intracérébraux sont moins importants, le vaccin n'a pas empêché la progression de la détérioration intellectuelle jusqu'au stade terminal[117].
- Un autre espoir, porté par le japonais Tohru Hasegawa[118] est d'utiliser l'acide homocystéique comme cible d'un vaccin. Cet acide - chez des souris 3xTg-AD (transgéniques, modifiées de manière à mimer les symptômes de la maladie humaine) - semble en effet nécessaire à la progression de la dégénérescence typique de cette affection [119],[120].
Le taux de cet acide est plus élevé dans le cerveau des souris 3xTg-AD de 4 mois que chez les souris témoins normales. Quand des souris 3xTg-AD sont soumises à une carence en vitamine B6 (ce qui augmente la quantité d'acide homocystéique dans leur cerveau, cela aggrave aussi leurs troubles mémoriels, sauf en cas d'injection d'anticorps anti-acide homocystéique. Injecter ces mêmes anticorps à des souris 3xTG-AD plus vieilles et normalement alimentées a également un effet curatif, en tous cas pour les troubles mémoriels. Les chercheurs restent prudents, car on a vu dans le passé que la souris n'était pas un modèle parfait pour cette maladie. Le vaccin devrait être testé sur des singes avant tout essai clinique sur l'homme.
Traitements non spécifiques
Ils modifient le comportement du malade sans s'attaquer à la maladie elle-même.
- La manière de se comporter est capitale: les aidants doivent pratiquer une relation théatralisée au seul but de transmettre des indices, des signes, des symboles rassurants pour le malade, ce qui ne manque pas d'améliorer son propre comportement, de limiter les réactions anxieuses qui peuvent déboucher sur de l'agressivité. Coping et resilience des aidants sont étayés par des aides, un entourage affectif et professionnel[121].
- Des psychotropes atténuent l'angoisse, l'agressivité ou les états d'agitation des patients. Les anticholinergiques, les neuroleptiques et les benzodiazépines à demi-vie longue sont à éviter en raison de leurs effets secondaires chez ces patients très fragiles. Les antidépresseurs n'ont pas prouvé d'efficacité[122].
- Des médicaments ciblant d'autres maladies sont régulièrement suspectés de protéger contre la maladie d'Alzheimer, dont certaines statines, des anti-oxydants (comme la vitamine E ou la mélatonine), des anti-inflammatoires. Mais les études observationnelles, dont le but initial n'était pas celui de traiter la démence, comportent par essence de nombreux biais et demandent à être confirmées. Les premiers résultats restent a priori décevants.
D'autres pistes sont en cours d'évaluation :
- Selon une étude[123], des souris (normales, et transgéniques présentant des troubles jugés comparables à ceux induits par la maladie d'Alzheimer) exposés plusieurs mois à certaines ondes électromagnétiques (de type téléphone portable ; 918 MHz; 0,25 W/kg) améliorent leur mémoire, perdent moins de capacité cognitive en vieillissant et produisent moins de plaques amyloïdes dans leur hippocampe (-35%) et leur cortex entorhinal (-32%). Une température cérébrale plus élevée de 1 °C et une accélération du débit sanguin cérébral sont constatés, mais le mécanisme global n'est pas compris. Si un effet similaire était constaté chez l'Homme, une piste nouvelle de traitement, non médicamenteuse et non chirurgicale s'ouvrirait.
- Café et caféine ont été proposés comme l'un des moyens d'améliorer l'état des patients[124], mais avec des effets secondaires possibles.
- L'exposition à la lumière naturelle semble améliorer certains symptômes. La prise de mélatonine, associée à une luminothérapie pourrait améliorer les troubles du sommeil, en agissant comme inducteur de sommeil mais aussi comme facteur d'allongement de la durée de celui-ci[125]. L'exposition à la lumière naturelle diminuerait aussi chez ces malades les symptômes de dépression (-19%), les limitations fonctionnelles au quotidien (- 53%), la détérioration cognitive (- 5%). Chez les malades observés, la prise de mélatonine facilitait l'endormissement. L'association lumière + mélatonine a aussi diminué les comportements agressifs (- 9%), les phases d'agitation et de réveil nocturne. Il est donc cosseillé[126] "de bien éclairer les pièces en journée (... et) à l'inverse, de diminuer les sources de lumière en soirée pour que l'organisme reçoive le signal que la nuit est là".
Conséquences sociales
La famille comprend les enfants, les frères et sœurs, nièces et neveux... En se référant au nombre estimé en 2007 de 800 000 malades en France et en considérant une moyenne de 3 cellules familiales autour d'un malade, ce sont plus de 2 400 000 personnes qui sont concernées plus ou moins directement par la maladie d'Alzheimer. C'est un problème majeur de société, la progression du nombre de malades étant d'environ 250 000 cas par an selon le rapport du prof. Ménard.
Dans les pays occidentaux, la famille a des ressources limitées en temps pour offrir à la personne malade le soutien dont elle a besoin de façon de plus en plus continue au fur et à mesure de l'évolution de la maladie. Pourtant, dans 70 % des cas, c'est la famille qui prend en charge la personne malade et lui permet de rester à domicile.
On a pris conscience de l'apport considérable de ces aidants "naturels" et les professionnels se rendent compte que l'"aide aux aidants" est probablement une des manières de répondre à cet énorme défi de santé publique.
En France, 70% des époux et 50% des enfants d'une personne souffrant de la maladie d'Alzheimer lui consacrent plus de 6 heures par jour. 24% des aidants – et 54% s’il s’agit d’enfants d'une personne atteinte de la maladie d'Alzheimer – doivent réaménager leur activité professionnelle. 20% des aidants naturels d'une personne atteinte de la maladie d'Alzheimer déclarent différer, voire renoncer à une consultation, une hospitalisation ou un soin pour eux-mêmes par manque de temps[127]. Si l'Alzheimer atteint le chiffre prévu de 1 200 000 cas, il mobilisera à lui seul et pour le simple nursing un dixième de la population active. Par ailleurs, il semblerait que la mortalité des personnes aidant soit supérieure à celle de personnes du même age ne s'occupant pas d'un malade, mais cela n'est pas clairement établi à ce jour[128].
Les aides possibles
Ce dispositif permet d’accueillir pour une période d’une demi-journée à plusieurs jours par semaine des personnes âgées atteintes de la maladie d’Alzheimer ou maladies apparentées et vivant à domicile. Ces accueils ponctuels aident les malades à maintenir un lien social, les stimulent par des activités thérapeutiques adaptées destinées à ralentir les effets de la maladie et soulagent également les proches en leur offrant des périodes de répit. L’accueil de jour permet à des personnes atteintes de troubles neuro-dégénératifs de poursuivre leur vie à domicile dans les meilleures conditions possibles grâce à des activités de stimulation. Il soulage également les proches, leur offre des périodes de répit afin d’être par la suite plus disponibles. Ces temps de prise en charge par une équipe de professionnels aident aussi les malades à maintenir un lien social.
La prise en charge financière de l’accueil de jour peut faire partie du plan d’aide proposé dans le cadre de l’Allocation Personnalisée à l'Autonomie à domicile (A.P.A.).
Les ressources humaines
Services de soins infirmiers à domicile = SSIAD
Il est possible d'avoir à domicile des soins infirmiers ou d'hygiène par un infirmier et d'autres soignants (aides-soignants, kinésithérapeute, orthophoniste...)
L’auxiliaire de vie / l’emploi d’une personne à domicile
L’aide à domicile est l’intervention d’une personne salariée qui se rend à domicile pour assurer différentes tâches.(ménage, repassage, lessive, courses, préparation du repas et/ou soins de base d’hygiène et de toilette courante...)
Ce salarié peut être toute personne, excepté le conjoint de la personne malade.
Son embauche peut se faire de diverses façons :
- directement du salarié à la personne (gré à gré),
- par l’intermédiaire d’un organisme public mandataire,
- par l'intermédiaire d'une entreprise privée prestataire de services à la personne,
- ou par une association.
L'aménagement du lieu de vie
Il ne faut pas hésiter à se faire aider par des personnes compétentes (conseillère en économie sociale et familiale, ergothérapeutes, assistants de service social...)
Lors de l'aménagement du lieu de vie, quelques mesures simples sont recommandées (liste non exhaustive) :
-
- Prévenir les accidents domestiques
- Les dangers sont nombreux : il y a bien sûr les plus courants : cuisinière , chauffage (poêle)... couteaux , etc. il faut être vigilant et prévoir car presque tout peut être un danger !
-
- ``` s'assurer que les portes extérieures soient barrées car les fugues sont possibles. Il existe des bracelets d'alerte médicale pour la maladie d'Alzheimer qui peuvent être utiles en cas de fugue ***
- La salle de bain doit être la plus fonctionnelle et sécurisée possible : maximum de température de l'eau bloqué, sol antidérapant, barres de maintien sur les murs...
- Prévenir les chutes : éviter l'encombrement inutile, les sols glissants...
- Favoriser l'autonomie dans toutes les pièces de la maison (objets usuels facilement accessibles...).
- Supprimer les sources de stress et de confusion :
- Ne pas déplacer les repères familiers du patient
- Favoriser l'orientation de la personne dans le temps
- Mettre une horloge facilement lisible dans chaque pièce
- Accrocher une éphéméride (dont la personne arrachera une page chaque jour)
- Écrire lisiblement (par exemple au-dessus du téléphone) le nom, l'adresse et le numéro de téléphone de la personne.
Des financements sont possibles, auprès de l'ANAH (Agence nationale de l'habitat), des caisses de retraites CNAVTS, ARRCO et IRCANTEC et de la PALULOS (Prime à l'Amélioration des Logements à Usage Locatif et à Occupation Sociale). Il ne faut jamais démarrer les travaux avant d'avoir soumis le dossier de demande de financement à ces organismes.
Les aides matérielles
Quelques exemples :
- portage des repas
- service de blanchisserie
- livraison de courses
- téléalarme (les mairies ou le conseil général disposent des renseignements quant à sa mise en place)
- se présente sous forme de médaillon ou de bracelet que l'on porte sur soi en continu
- en liaison avec une centrale de surveillance opérationnelle (24h/24)
- peut être couplée à un détecteur d'activité en complément du "bip" traditionnel, installé à un endroit de passage régulier de la personne
- matériel médical
Les aides financières
Plusieurs aides financières existent :
- Majoration pour tierce personne de la Sécurité Sociale si l'état de dépendance a été reconnu avant 65 ans
- Allocation compensatrice tierce personne attribuée par la MDPH (Maison Départementale de Personnes Handicapées) si la personne malade a moins de 60 ans et s'il s'agit d'un renouvellement postérieur au 1er janvier 2006. S'il s'agit d'une première demande cette allocation est remplacée par la prestation de compensation volet aide humaine ; Il existe également des volets aides techniques et aménagement du logement.
- Allocation personnalisée d'autonomie (APA):
- attribuée aux personnes âgées (de plus de 60 ans) dépendantes ayant des difficultés pour accomplir des gestes ordinaires de la vie quotidienne
- son montant varie en fonction du degré d'autonomie de la personne âgée et de ses ressources
- la perte d'autonomie est évaluée grâce à une grille nationale (la grille AGGIR) qui classe les personnes âgées en 6 groupes : du groupe GIR1, le plus dépendant, au groupe GIR6, le moins dépendant
- Allocations logement ou aide personnalisée au logement (APL) attribuées par la (Caisse d'allocations familiales)
- La prestation de garde à domicile de la CNAVTS, pour des situations d'urgence temporaires, concerne uniquement les personnes dont la caisse de retraite principale est la CNAVTS ou la CARSAT (Caisse d'assurance retraite et de la santé au travail) et sous certaines conditions.
Pour les aides matérielles :
Certains appareils ou matériel médical installés au domicile du patient peuvent être loués ou achetés et pris en charge par la Sécurité Sociale. Pour les achats et locations importants, il faut demander un avis et faire une demande d'entente préalable auprès de la Sécurité Sociale.
Pour les ressources humaines :
Pour l’emploi de personne à domicile, l’employeur peut avoir une déduction fiscale et une exonération de cotisations sociales sur le salaire de l’intervenant. L'APA peut prendre en charge les dépenses de rémunération de l'intervenant à domicile si ses interventions font partie du Plan d'aide personnalisée élaboré par l'équipe médico-sociale.
Le plan Alzheimer en France
855 000 français sont atteints par la maladie d'Alzheimer : 225 000 nouveaux cas se déclarent chaque année et un patient moyen et son aidant familial doivent débourser environ 1 000 €/mois [129].. On estime qu'1,3 millions de français pourraient être touchés en 2020. Le plan Alzheimer vise une meilleure prise en charge des troubles de la maladie d'Alzheimer en France et de ceux qui y sont liés. Après deux versions (2001-2005, puis 2004-2007) dont les objectifs ont globalement été atteints, une troisième version a été publiée en novembre 2007, entrée en vigueur le 1er janvier 2008 et couvre la période 2008-2012. Le plan vise aussi à soutenir ou augmenter le nombre de thèses traitant de ce sujet. Ce nombre est en croissance régulière et les thèses françaises ont traité (par ordre décroissant) des aspects : Biologie et neuropathologie (75 thèses) ; Neuropsychologie (près de 45 thèses) ; Modèle animaux (plus de 20 thèses) ; Pharmacologie (15 thèses environ) ; Génétique (près de 15 thèses) ; Imagerie cérébrale et autres examens (moins de 10 thèses); Épidémiologie (10 thèses); Évaluation médico-économique (2 thèses); A partir de 2011, des Maisons d'accueil et d'intégration des malades Alzheimer devraient se généraliser[130]
Le plan Alzheimer 2008-2012
- La commission chargée de la préparation du plan est présidée par Joël Ménard, ancien directeur général de la santé, professeur émérite de santé publique à l'université Paris-Descartes et Président du Conseil Scientifique International de la Fondation Plan Alzheimer (fondation de coopération adossée à l’INSERM). Elle comprend dix membres choisis pour leurs connaissances sur cette maladie. Elle s'appuie sur le travail de huit groupes d'experts, chaque groupe ayant son thème spécifique.
Les orientations du plan Alzheimer 2008-2012 (dont l'engagement financier sur 5 ans est d'un milliard six cents millions d'€) sont le renforcement de la dimension éthique de la prise en charge de la maladie (200 000 €), le développement de la recherche médicale (200 millions d'€), les soins (200 millions d'€), la simplification et l'amélioration du parcours du malade et de sa famille, dans toutes ses dimensions (un milliard deux cents millions d'€ investis dans des structures de diagnostic : 38 consultations mémoire et 3 centres mémoire de ressources et de recherche ; accompagnements à domicile ou en unités d'hébergements comme les maisons pour l’autonomie et l’intégration des malades d’Alzheimer dont 10 000 nouveaux malades, chaque année, sont âgés de moins de 60 ans)[131].
Alzheimer : tendance et ressources québécoises
La tendance au Québec : garder la personne atteinte d’Alzheimer à la maison et ce, pour le plus longtemps possible ! Pourquoi : les gouvernements fédéral et provincial estiment que le coût de l’hébergement est élevé !
Selon une étude de l’Institut de gériatrie de Sherbrooke, même quand l’institutionnalisation devient possible, peu de familles choisissent cette option; elles continuent plutôt de soigner la personne à domicile… Une autre étude montre que des aidants naturels ayant placé le malade en maison de soins éprouvent moins de plaisir à soigner que d’autres n’ayant pas eu recours à l’institutionnalisation. Seule unanimité jusqu’à maintenant chez tous les participants: les services (bain, ménage, popote roulante, infirmière, etc.) sont insuffisants[132]. Cependant, une autre vision est appliquée dans les institutions d'accueil : il s'agit de laisser les malades être autonomes dans les domaines qu'ils maîtrisent encore le plus longtemps possible.
Le traitement de la maladie d'Alzheimer en Belgique
Mars 2009 : la maladie d’Alzheimer et les affections apparentées frappent 150.000 personnes en Belgique (soit environ 1,5% de la population, qui est d'environ 10 millions d'habitants). Mal pour l'instant incurable, on estime que la démence comptera jusqu’à 200.000 victimes en Belgique en 2020, le vieillissement de la population aidant[133].
Un essor qui a incité la Fondation Roi Baudouin (FRB) à formuler des recommandations concrètes pour améliorer la qualité de vie des malades et de leurs proches. Voir l'article "Un autre regard sur la démence : des recommandations de la Fondation Roi Baudouin" sur le site Internet de la Fondation Roi Baudouin. Accès direct à l'article.
La Ligue Nationale Alzheimer Liga ASBL/vzw/VoG a son propre site Internet, trilingue (français - néerlandais - allemand). Cliquer sur "Français" dans le cercle au sommet de l'écran pour entrer dans le site de La Ligue Alzheimer a.s.b.l., qui en fait partie.
Différence entre la démence et la maladie d'Alzheimer
Le terme démence est utilisé pour exprimer une détérioration mentale générale et chronique. La démence n'est qu'une description de la façon dont le patient se présente devant le praticien, et de nombreuses maladies peuvent en être la cause. La maladie d'Alzheimer est l'une des formes de démence provoquées par une anomalie biochimique. Il existe d'autres formes de démence comme, parmi d’autres, la chorée de Huntington, la maladie de Parkinson, la paralysie supranucléaire progressive, les encéphalites[134].
Il faut noter que ce que décrivit le Dr Alois Alzheimer était la démence présénile. De nos jours, la dénomination "maladie d'Alzheimer" est couramment étendue à des cas de démence sénile. La raison majeure en est que les altérations anatomopathologiques sont similaires dans les deux cas.Néanmoins, il serait préférable de parler de maladie du type Alzheimer dans le cas des démences séniles.
Projets de calcul distribué
Le projet international neuGRID, financé par l'Union européenne, prevoit le développement d’une infrastructure numérique pour la recherche scientifique, fondée sur le système Grid et équipé d’une interface d’utilisation facile, qui permettra aux chercheurs européens de neurosciences de faire avancer la recherche pour l’étude de la maladie d'Alzheimer et d'autres maladies neurodégénératives.
La maladie d'Alzheimer dans la culture
Filmographie
- 2001 : Iris de Richard Eyre
- 2001 : Se souvenir des belles choses de Zabou Breitman
- 2002 : La Maladie de la mémoire de Richard Dindo
- 2004 : La Mémoire du tueur (De zaak Alzheimer) de Erik Van Looy
- 2004 : N'oublie jamais (The Notebook) de Nick Cassavetes
- 2004 : A Moment to Remember de John H. Lee
- 2005 : { Une grande bouffée d'amour! (Aiguemarine C°)
- 2005 : Black de Sanjay Leela Bhansali
- 2006 : Memories of Tomorrow de Yukihiko Tsutsumi
- 2007 : Loin d'elle (Away from Her) de Sarah Polley
- 2007 : La Brunante de Fernand Dansereau
- 2007 : (Ta mémoire...Mon Amour!" (Aiguemarine C°)
- 2008 : Cortex de Nicolas Boukhrief
- 2008 : U, Me Aur Hum de Ajay Devgan
- 2009 : Je me souviens mieux quand je peins, documentaire d'Eric Ellena et Berna Huebner
- 2009 : La Verticalidad del Tiempo, documentaire de Raùl Fernandez Rincon et Marianne Ruiz Luca Films, Madrid
- 2010 : The Secret Life of the American Teenager, Saison 1, épisode 8/23 (La Visite), série TV de Keith Truesdell
- 2010 : L'absence de Cyril de Gasperis
- 2011 : Je n'ai rien oublié, de Bruno Chiche, d'après le roman Small World de Martin Suter
- 2011 : La Planète des singes : Les Origines de Rupert Wyatt
Bibliographie
Il existe entre 1997 et 2007 une forte augmentation des œuvres comportant des personnages atteints de la maladie d'Alzheimer ou de maladie apparentée[135].
- Still Alice, de Lisa Genova, Pocket Books 2007
- Alzheimer, mode d'emploi, de Jean-Pierre Polydor, L'esprit du temps 2009
- Histoire de ma mère, de Yasushi Inoué, Stock 1997, 2004 et 2007
- Je ne suis pas sortie de ma nuit, de Annie Ernaux, Gallimard 1997 et Folio 1999
- Ton chapeau au vestiaire, de Nadine Trintignant, Fayard 1997 et Pocket 1999
- Small World, de Martin Suter, Christian Bourgois 1998, et Points Seuil 2000
- Quel jour sommes-nous ? de Firmin Le Bourhis, Chiron 2000
- La Cavale du géomètre, d'Arto Paasilinna, Gallimard/folio 2000
- Elégies pour Iris, de John Bailey, L’Olivier 2001
- Les jours heureux, de Laurent Graff, La Dilettante 2001 et J’ai Lu 2003
- L’Effacement de l’aube, de Ronald Nossintchouk, E-Dite 2002
- Les Corrections, de Jonathan Franzen, L’Olivier 2002 et Points Seuil 2003
- Pourquoi ma mère me rend folle, de Françoise Laborde, Ramsay 2002 et J’ai Lu 2003
- Ma mère n’est pas un philodendron, de Françoise Laborde, Fayard 2003 et J’ai Lu 2005
- L’Éclipse, de Serge Rezvani, Actes Sud 2003
- Mon vieux, de Thierry Jonquet, Seuil 2004
- Le Dernier qui part ferme la maison, de Michèle Fitoussi, Grasset 2004 et Poche 2006
- Les Cœurs décousus, de Jacqueline Girard-Frésard, Le Cherche Midi 2004
- Puzzle : journal d’une Alzheimer, de Claude Couturier, Josette Lyon 2004
- Les Quantités Négligeables (Le combat ordinaire, Tome 2), de Manu Larcenet, Dargaud 2004
- Sœurs, de Catherine Locandro, Gallimard 2005
- Mémorial, de Cécile Wajsbrot, Zulma 2005
- Le Piano désaccordé, de Christine Devars, Anne Carrière 2005
- Devant ma mère, de Pierre Pachet, Gallimard 2007
- Rides, de Paco Roca, Delcourt 2007
- Élégie : 1996-2006. La maladie d’Alzheimer vécue à deux, de Jean Sauvy, L’harmattan 2007
- Les Artistes de la mémoire, de Jeffrey Moore, Philippe Rey 2007
- Les Madones de Léningrad, de Debra Dean, Grasset, 2007
- La mémoire de ma mère Annie Girardot, de Giulia Salvatori, M. Lafon 2007
- Rainbows end, de Venor Vinge, Robert Laffont 2007
- On n’est pas là pour disparaître, de Olivia Rosenthal, Gallimard (Verticales) 2007
- La Vie sur terre, de Dorothée Janin, Denoël 2007
- La Plume du silence - Toi et moi…et Alzheimer, de Jean Witt, Presses de la Renaissance 2007
Notes et références
- "World Alzheimer Report 2010"
- (en) Cleusa P. Ferri, Martin Prince, Carol Brayne, Henry Brodaty, Laura Fratiglioni, Mary Ganguli, Kathleen Hall, Kazuo Hasegawa, Hugh Hendrie, Yueqin Huang, Anthony Jorm, Colin Mathers, Paulo R Menezes, Elizabeth Rimmer, Marcia Scazufca, for Alzheimer's Disease International, « Global prevalence of dementia: a Delphi consensus study », The Lancet, vol. 366, Issue 9503, 17 décembre 2005-6 janvier 2006, p. 2112-2117 DOI:10.1016/S0140-6736(05)67889-0 [PDF]
- http://www.caducee.net/breves/breve.asp?idb=4412&mots=all
- Étude PAQUID : Personnes Âgées Quid, recherche de 1990 à 1998 en partenariat avec le ministère de l’Environnement et l’INSERM sur 3 411 individus de 65 ans et plus. Étude du vieillissement, Pr JF Dartigues et al, université de Bordeaux (CHU de Bordeaux.)
- [PDF](fr)Document de 140 pages sur l'observatoire national sur la recherche sur la maladie d'Alzheimer, voir aussi le site de l'ONRA
- Polydor J-P, Alzheimer, mode d'emploi, le livre des aidants, préfacé par Madeleine Chapsal, prix Femina, L'esprit du temps Édition, 2009, ( ISBN, 2847951717)
- Kuller LH. Dementia epidemiology research: it is time to modify the focus of research. J Gerontol A Biol Sci Med Sci. 2006 Dec;61(12):1314-8
- Chandra V, Pandav R, Dodge HH, Johnston JM, Belle SH, DeKosky ST, Ganguli M.Incidence of Alzheimer's disease in a rural community in India: the Indo-US study ; Neurology. 2001 25 09 ; 57(6):985-9
- Hendrie HC, Hall KS, Ogunniyi A, Gao S ; Alzheimer's disease, genes, and environment: the value of international studies.;Can J Psychiatry. 2004 Feb;49(2):92-9
- Hendrie HC ; Lessons learned from international comparative crosscultural studies on dementia, Am J Geriatr Psychiatry, Juin 2006; 14(6):480-8
- Shadlen MF, Larson EB, Yukawa M. The epidemiology of Alzheimer's disease and vascular dementia in Japanese and African-American populations: the search for etiological clues. ; Department of Medicine, Harborview Medical Center, School of Pharmacy, University of Washington, Seattle, USA. Neurobiol Aging. 2000 03 21 ; (2):171-81
- Graves AB, Larson EB, Edland SD, Bowen JD, McCormick WC, McCurry SM, Rice MM, Wenzlow A, Uomoto JM. Prevalence of dementia and its subtypes in the Japanese American population of King County, Washington state. The Kame Project. Department of Epidemiology and Biostatistics, University of South Florida, Tampa, USA. Am J Epidemiol. 1996 Oct 15;144(8):760-71
- Yamada T, Kadekaru H, Matsumoto S, Inada H, Tanabe M, Moriguchi EH, Moriguchi Y, Ishikawa P, Ishikawa AG, Taira K, Yamori Y. ; Prevalence of dementia in the older Japanese-Brazilian population. ; Psychiatry Clin Neurosci. 2002 Feb;56(1):71-5 (Department of Internal Medicine and Health Care, Fukuoka University, Fukuoka, Japan)
- Lopes MA, Bottino CM. ; Prevalence of dementia in several regions of the world: analysis of epidemiologic studies from 1994 to 2000 (Instituto de Psiquiatria, Hospital das Clínicas, Faculdade de Medicina, Universidade de São Paulo, Brasil). Arq Neuropsiquiatr. Mars 2002 ;60(1):61-9
- Fujishima M, Kiyohara Y. ; Incidence and risk factors of dementia in a defined elderly Japanese population: the Hisayama study. (Department of Medicine and Clinical Sciences, Kyushu University , japon) ; Ann N Y Acad Sci. ; Novembre 2002; Nov;977:1-8
- Source : Alzheimer's Disease International
- Wancata J, Musalek M, Alexandrowicz R, Krautgartner Number of dementia sufferers in Europe between the years 2000 and 2050. M. Eur Psychiatry. 2003 Oct;18(6):306-13
- (fr)Taux de patients belges atteints de la maladie d'Alzheimer sur Le centre hospitalier chrétien (CHC). Consulté le 14 janvier 2006
- N° 2454 - Rapport sur la maladie d'Alzheimer et les maladies apparentées au nom de l'Office parlementaire d'évaluation des politiques de santé (rapporteuse : Mme Cécile Gallez)
- Ramaroson H, Helmer C, Barberger-Gateau P, Letenneur L, Dartigues JF ; Prevalence of dementia and Alzheimer's disease among subjects aged 75 years or over : Résultats mis à jour du programme PAQUID cohort] (fr) ; PAQUID. ; Unité INSERM 330, Université Victor Segalen Bordeaux II. Rev Neurol (Paris). 2003 Apr;159(4):405-11
- C, Pasquier F, Dartigues JF. Epidemiology of Alzheimer disease and related disorders Helmer Med Sci (Paris). 2006 Mar;22(3):288-96 (fr)
- Hamed A, Lee A, Ren XS, Miller DR, Cunningham F, Zhang H, et al. Use of antidepressant medications: are there differences in psychiatric visits among patient treatments in the Veterans Administration ? Med Care 2004;42:551-9.
- Nien-Chen Li, Austin Lee, Rachel A Whitmer, Miia Kivipelto, Elizabeth Lawler, Lewis E Kazis, and Benjamin Wolozin ; Use of angiotensin receptor blockers and risk of dementia in a predominantly male population: prospective cohort analysis ; BMJ 2010;340:b5465, doi:10.1136/bmj.b5465 (2010/01/12) ; résumé, publié en Creative Commons Attribution Non-commercial License, consulté 2010/04/05)
- De la Torre JC. Is Alzheimer’s disease a neurodegenerative or a vascular disorder ? Data, dogma, and dialectics. Lancet Neurol 2004;3:184-90
- Ruitenberg A, den Heijer T, Bakker SL, van Swieten JC, Koudstaal PJ, Hofman A, et al. Cerebral hypoperfusion and clinical onset of dementia: the Rotterdam Study. Ann Neurol 2005;57:789-94
- Encinas M, De Juan R, Marcos A, Gil P, Barabash A, Fernandez C, et al. Regional cerebral blood flow assessed with 99mTc-ECD SPET as a marker of progression of mild cognitive impairment to Alzheimer’s disease. Eur J Nucl Med Mol Imaging 2003;30:1473-80.
- Kivipelto M, Helkala EL, Laakso MP, Hanninen T, Hallikainen M, Alhainen K, et al. Midlife vascular risk factors and Alzheimer’s disease in later life: longitudinal, population based study. BMJ 2001;322:1447-51 (Résumé)
- Whitmer RA, Sidney S, Selby J, Johnston SC, Yaffe K. Midlife cardiovascular risk factors and risk of dementia in late life. Neurology 2005;64:277-81 (Résumé)
- Luchsinger JA, Reitz C, Honig LS, Tang MX, Shea S, Mayeux R. Aggregation of vascular risk factors and risk of incident Alzheimer disease. Neurology 2005;65:545-51 (Résumé)
- Newman AB, Fitzpatrick AL, Lopez O, Jackson S, Lyketsos C, Jagust W, et al. Dementia and Alzheimer’s disease incidence in relationship to cardiovascular disease in the Cardiovascular Health Study cohort. J Am Geriatr Soc 2005;53:1101-7
- Sjogren M, Mielke M, Gustafson D, Zandi P, Skoog I. Cholesterol and Alzheimer’s disease—is there a relation ? Mech Ageing Dev 2006;127:138-47.
- « Facteurs environnementaux impliqués dans la maladie d’Alzheimer. Le mercure dentaire, probable déterminant majeur », lire en ligne sur em-consulte.com
- M Bates et al. Health effects of dental amalgam exposure: a retrospective cohort study. Int. J. Epidemiol. (2004) 33 (4): 894-902. [1]
- J Mutter Does Inorganic Mercury Play a Role in Alzheimer’s Disease? A Systematic Review J Alzheimers Dis. 2010;22(2):357-74. [2]
- Morris MC, Evans DA, Bienias JL, Tangney CC, Bennett DA, Aggarwal N, Schneider J, Wilson RS, « Dietary fats and the risk of incident Alzheimer disease. », dans Arch Neurol., vol. 60, no (2), 2003, p. 194-200 [texte intégral]
- Rusanen M, Kivipelto M, Quesenberry Jr CP, Zhou J, Whitmer RA, Heavy smoking in midlife and long-term risk of Alzheimer disease and vascular dementia, Arch Intern Med, 2011;171:333-339
- [3]
- [4]
- [5]
- vidéo de l'association américaine Alzheimer sur l'évolution de la maladie [6]
- H. Amieva et al. Ann Neurol. 64 492, 2008
- Delacourte A, David JP, Sergeant N, et al. The biochemical pathway of neurofibrillary degeneration in aging and Alzheimer's disease. Neurology 1999 ; 52 : 1158-65.
- Delacourte A, Buée L. Normal and pathological Tau proteins as factors for microtubule assembly. Int Rev Cytol 1997 ; 171 : 167-224.
- http://www.orpha.net/data/patho/FR/fr-alzheim.pdf
- J.-C. Lambert et al., Genome-wide association study identifies variants at CLU and CR1 associated with Alzheimer's disease, Nature Genetics, vol. 41, pp. 1094-1099, 2009. (Résumé)
- D. Harold et al., Genome-wide association study identifies variants at CLU and PICALM associated with Alzheimer's disease, Nature Genetics, vol. 41, pp. 1088-1093, 2009 (Résumé)
- OMS (WHO/IPCS) ; 1991 : extrait de Global Mercury Assessmenr (ONU; Mercury Programm, chap 4). (OnLine)
- Weiner JA, Nylander M. ; The relationship between mercury concentration in human organs and different predictor variables. Sci Total Environ. Septembre 1993 ; 0;138(1-3):101-15
- Nylander M, Friberg L, Lind B ; Mercury concentrations in the human brain and kidneys in relation to exposure from dental amalgam fillings. Swed Dent J. ; 1987 ; 11(5):179-87
- Eggleston DW, Nylander M J Prosthet ; Correlation of dental amalgam with mercury in brain tissue. Dent. ; Décembre 1987 ; 58(6):704-7
- Drasch G, Schupp I, Hofl H, Reinke R, Roider G Eur ; Mercury burden of human fetal and infant tissues. ; J Pediatr. ; Aout 1994 ; 153(8):607-10
- Guzzi G, Grandi M, Cattaneo C, Calza S, Minoia C, Ronchi A, Gatti A, SeveriDental amalgam and mercury levels in autopsy tissues: food for thought. G. ; Am J Forensic Med Pathol. 2006 Mar;27(1):42-5
- Mutter J, Naumann J, Sadaghiani C, Schneider R, Walach H. Alzheimer disease: mercury as pathogenetic factor and apolipoprotein E as a moderator;Neuro Endocrinol Lett.Octobre 2004 ; 25(5):331-9.
- Pendergrass JC, Slevin JT, Haley BE. Duhr EF,; HgEDTA complex inhibits GTP interactions with the E-site of brain beta-tubulin. ; Toxicol Appl Pharmacol. 1993 Oct;122(2):273-80
- Jones JA, Lavallee N, Alman J, Sinclair C, Garcia RI. ; Caries incidence in patients with dementia. Geriatric Dental Program , Department of Veterans Affairs Medical Center, Bedford, MA 01730, USA. Gerodontology. 1993 Dec;10(2):76-82.
- Eggleston et al. ont montré que le cerveau de personnes qui avaient de 5 à 15 amalgames dentaires en bouche contenait 2 à 3 fois plus de mercure que celui des personnes ayant peu d'amalgames.
- Rejnefelt I, Andersson P, Renvert S. (Département des sciences de la santé de l'Université de Kristianstad) Oral health status in individuals with dementia living in special facilities. Int J Dent Hyg. Mai 2006 ; 4(2):67-71
- Pendergrass JC, Haley BE, Vimy MJ, Winfield SA, Lorscheider FL. Mercury vapor inhalation inhibits binding of GTP to tubulin in rat brain: similarity to a molecular lesion in Alzheimer diseased brain.; Neurotoxicology. ; 1997 ;18(2):315-24
- Thompson CM, Markesbery WR, Ehmann WD, Mao YX, Vance DE Regional brain trace-element studies in Alzheimer's disease. Neurotoxicology. 1988 Spring;9(1):1-7
- Ehmann WD, Markesbery WR, Alauddin M, Hossain TI, Brubaker EH ; Brain trace elements in Alzheimer's disease ; Neurotoxicology. 1986 Spring;7(1):195-206
- Increased blood mercury levels in patients with Alzheimer's disease. Hock C, Drasch G, Golombowski S, Müller-Spahn F, Willershausen-Zönnchen B, Schwarz P, Hock U, Growdon JH, Nitsch RM. J Neural Transm. 1998;105(1):59-68
- Krauhs E, Little M, Kempf T, Hofer-Warbinek R, Ade W, Ponstingl H. ; Complete amino acid sequence of beta-tubulin from porcine brain; Proc Natl Acad Sci U S A. 1981 Jul;78(7):4156-60
- Olivieri G, Brack C, Muller-Spahn F, Stahelin HB, Herrmann M, Renard P, Brockhaus M, Hock C. Mercury induces cell cytotoxicity and oxidative stress and increases beta-amyloid secretion and tau phosphorylation in SHSY5Y neuroblastoma cells. ; J Neurochem. 2000 Jan;74(1):231-6
- Olivieri G, Brack C, Muller-Spahn F, Stahelin HB, Herrmann M, Renard P, Brockhaus M, Hock C. ; Mercury induces cell cytotoxicity and oxidative stress and increases beta-amyloid secretion and tau phosphorylation in SHSY5Y neuroblastoma cells. ; J Neurochem. 2000 Jan;74(1):231-6
- Duhr EF, Pendergrass JC, Slevin JT, Haley BE.; HgEDTA complex inhibits GTP interactions with the E-site of brain beta-tubulin.Toxicol Appl Pharmacol. 1993 Oct;122(2):273-80
- Lorscheider FL, Vimy MJ, Summers AO, Zwiers H. ; The dental amalgam mercury controversy--inorganic mercury and the CNS; genetic linkage of mercury and antibiotic resistances in intestinal bacteria.; Toxicology. 1995 Mar 31;97(1-3):19-22
- Leong CC, Syed NI, Lorscheider FL, Retrograde degeneration of neurite membrane structural integrity of nerve growth conesfollowing in vitro exposure to mercury. ;Neuroreport. 2001 Mar 26;12(4):733-7
- Cedrola S, Guzzi G, Ferrari D, Gritti A, Vescovi AL, Pendergrass JC, La Porta CA Inorganic mercury changes the fate of murine CNS stem cells. ; The FASEB Journal Mai 2003 ; 17(8):869-71. Epub 2003 Mar 28
- Fonte J, Miklossy J, Atwood C, Martins R The severity of cortical Alzheimer's type changes is positively correlated with increased amyloid-beta Levels: Resolubilization of amyloid-beta with transition metal ion chelators. ;J Alzheimers Dis. Avril 2001 ; 3(2):209-219
- Bush AI. ;Metal complexing agents as therapies for Alzheimer's disease.;Neurobiol Aging. Nov-Dec 2002 ; 23(6):1031-8
- Danbolt NC ; Glutamate uptake. ;Prog Neurobiol. Septembre 2001 ; 65(1):1-105
- Brookes N. ; In vitro evidence for the role of glutamate in the CNS toxicity of mercury. ; Toxicology. 1992 Dec 4;76(3):245-56.
- Mutkus L, Aschner JL, Syversen T, Shanker G, Sonnewald U, Aschner M. Mercuric chloride inhibits the in vitro uptake of glutamate in GLAST- and GLT-1-transfected mutant CHO-K1 cells
- Allen JW, Mutkus LA, Aschner M; Mercuric chloride, but not methylmercury, inhibits glutamine synthetase activity in primary cultures of cortical astrocytes ; Brain Res. Février 2001 Feb 9;891(1-2):148-57
- Boyd E. Haley (University du Kentucky); The Relationship of the toxic effects of mercury to exacerbation of the medical condition classified as Alzheimer’s disease (2002) ; (étude accessible sur le site de l’UNEP)
- Aksenov M, Aksenova M, Butterfield DA, Markesbery WR. ;Oxidative modification of creatine kinase BB in Alzheimer's disease brain. ; J Neurochem. Juin 2000;Jun;74(6):2520-7
- David S, Shoemaker M, Haley BE. ; Abnormal properties of creatine kinase in Alzheimer's disease brain: correlation of reduced enzyme activity and active site photolabeling with aberrant cytosol-membrane partitioning ; Brain Res Mol Brain Res. Mars 1998 ; 1;54(2):276-87
- Blacker D, Haines JL, Rodes L, Terwedow H, Go RC, Harrell LE, Perry RT, Bassett SS, Chase G, Meyers D, Albert MS, Tanzi R. ApoE-4 and age at onset of Alzheimer's disease: the NIMH genetics initiative. 1: Neurology. Janvier 1997 Jan ; 48(1):139-47
- Olarte L, Schupf N, Lee JH, Tang MX, Santana V, Williamson J, Maramreddy P, Tycko B,Mayeux R.Apolipoprotein E epsilon4 and age at onset of sporadic and familial Alzheimer disease in Caribbean Hispanics. ; Arch Neurol. Novembre 2006 ; 63(11):1586-90
- Aggarwal NT, Wilson RS, Beck TL, Bienias JL, Berry-Kravis E, Bennett DA. ; The apolipoprotein E epsilon4 allele and incident Alzheimer's disease in persons with mild cognitive impairment. Neurocase. Février 2005 ; 11(1):3-7
- Huang Y. ; Apolipoprotein E and Alzheimer disease. ; Neurology. 2006 Jan 24;66(2 Suppl 1):S79-85
- Slooter AJ, Cruts M, Kalmijn S, Hofman A, Breteler MM, Van Broeckhoven C, van Duijn CM Arch Neurol ; Risk estimates of dementia by apolipoprotein E genotypes from a population-based incidence study : the Rotterdam Study. Juillet 1998 ; 55(7):964-8
- Effects of age, sex, and ethnicity on the association between apolipoprotein E genotype and Alzheimer disease. A meta-analysis. APOE and Alzheimer Disease Meta Analysis Consortium.Farrer LA, Cupples LA, Haines JL, Hyman B, Kukull WA, Mayeux R, Myers RH, Pericak-Vance MA, Risch N, van Duijn CM JAMA. Octobre 1997 ; 2-29;278(16):1349-56
- Le motif R permet à la protéine TAU de se fixer sur les microtubules.
- [ http://www.actualites-news-environnement.com/20070710-Alzheimer-diagnostic-precoce-maladie.php D'après actualites-news-environnement.com]
- Kehoe PG, Wilcock GK. Is inhibition of the renin-angiotensin system a new treatment option for Alzheimer’s disease? ; Lancet Neurol 2007;6:373-8 (Web of science)
- Skoog I, Lithell H, Hansson L, Elmfeldt D, Hofman A, Olofsson B, et al. Effect of baseline cognitive function and antihypertensive treatment on cognitive and cardiovascular outcomes: Study on COgnition and Prognosis in the Elderly (SCOPE). Am J Hypertens 2005;18:1052-9. (CrossRef)
- Forette F, Seux ML, Staessen JA, Thijs L, Babarskiene MR, Babeanu S, et al. The prevention of dementia with antihypertensive treatment: new evidence from the Systolic Hypertension in Europe (Syst-Eur) study. Arch Intern Med 2002;162:2046-52. (Résumé)
- Ara S. Khachaturian et al. ; Antihypertensive Medication Use and Incident Alzheimer Disease ; Arch Neurol. 2006;63:686-692. Published online March 13, 2006 (doi:10.1001/archneur.63.5.noc60013) (Résumé)
- Matchar DB, McCrory DC, Orlando LA, Patel MR, Patel UD, Patwardhan MB, et al. Systematic review: comparative effectiveness of angiotensin-converting enzyme inhibitors and angiotensin II receptor blockers for treating essential hypertension. Ann Intern Med 2008;148:16-29.
- Wilson RS, The relation of cognitive activity to risk of developing Alzheimer's disease. Neurology, 27 juin 2007
- Luchsinger JA, Reitz C, Honig LS, Tang MX, Shea S, Mayeux R. Aggregation of vascular risk factors and risk of incident Alzheimer disease. Neurology 2005;65:545-51
- Qiu C, Winblad B, Fratiglioni L. The age-dependent relation of blood pressure to cognitive function and dementia. Lancet Neurol 2005;4:487-99 (CrossRef)
- Jick H, Zornberg GL, Jick SS, Seshadri S, Drachman DA. Statins and the risk of dementia. Lancet 2000;356:1627-31
- Wolozin B, Kellman W, Ruosseau P, Celesia GG, Siegel G. Decreased prevalence of Alzheimer disease associated with 3-hydroxy-3-methyglutaryl coenzyme A reductase inhibitors. Arch Neurol 2000;57:1439-43.(résumé)
- travaux de recherche présentés lors du 4e Symposium scientifique international sur le thé et la santé humaine, Washington D.C. ; janvier 2008
- [7] Le thé qui soigne. Art. du Journal de Montréal (2008/01/16)
- http://www.organicconsumers.org/madcow/alzheimers81004.cfm
- http://www.emaxhealth.com/1275/91/34818/methionine-meat-other-foods-may-increase-alzheimers-risk.html
- http://timesofindia.indiatimes.com/life-style/health-fitness/health/Too-much-of-red-meat-fish-may-cause-Alzheimers/articleshow/5347074.cms
- http://www.massacreanimal.org/fr/mefaits_proteines_animales_alzheimer.php
- http://www.peta.org/living/vegetarian-living/alzheimers.aspx
- http://www.youngindianvegetarians.co.uk/Newsletter/Issue050/Ahimsa_2007_050.pdf
- http://www.expressindia.com/latest-news/Too-much-of-red-meat-fish-garlic-yogurt-may-raise-Alzheimers-risk/555311/
- http://www.ajcn.org/cgi/content/abstract/90/2/392?maxtoshow=&HITS=10&hits=10&RESULTFORMAT=&fulltext=omega+3+dementia+india&andorexactfulltext=and&searchid=1&FIRSTINDEX=0&sortspec=relevance&resourcetype=HWCIT
- Indian village may hold key to beating dementia
- http://healthmad.com/conditions-and-diseases/beware-of-meat-consumption
- (National Institute for Health and Clinical Excellence) : Alzheimer's disease - donepezil, galantamine, rivastigmine (review) and memantine Extrait du site di NICE
- Revue Prescrire, Numéro 278, Médicaments de la maladie d'Alzheimer : à l'origine de tremblements et d'aggravation de symptômes parkinsoniens, décembre 2006
- Revue Prescrire ; Les médicaments de la maladie d'Alzheimer, Mini dossier maj 15 Février 2007
- [8] National Institute for Health and Clinical Excellence (NICE)
- (en)Community based occupational therapy for patients with dementia and their care givers: randomised controlled trial, Maud J L Graff, Myrra J M Vernooij-Dassen, Marjolein Thijssen, Joost Dekker, Willibrord H L Hoefnagels, Marcel G M Olde Rikkert, BMJ, 2006;333:1196
- Courtney C, Farrell D, Gray R, Hills R, Lynch L, Sellwood E, Edwards S, Hardyman W, Raftery J, Crome P, Lendon C, Shaw H, Bentham P; AD2000 Collaborative Group. Long-term donepezil treatment in 565 patients with Alzheimer's disease (AD2000): randomised double-blind trial. Lancet 2004;363:2105-15. PMID 15220031
- Amélioration du service médical rendu
- la revue Prescrire, n°293, Mars 2008
- Areosa SA, McShane R, Sherriff F. Memantine for dementia. Cochrane Database Syst Rev 2004(4);CD003154.pub2. PMID 15495043
- Holmes C, Boche D, Wilkinson D, et als. Long-term effects of Aβ42 immunisation in Alzheimer's disease: follow-up of a randomised, placebo-controlled phase I trial, Lancet 2008;372:216-223
- le Pr Tohru Hasegawa travaille au Women's Junior College de Saga au Japon
- HASEGAWA Tohru, MIKODA Nobuyuki, KITAZAWA Masashi, LAFERLA Frank M. "Treatment of Alzheimer's Disease with Anti-Homocysteic Acid Antibody in 3xTg-AD Male Mice" - - PLoS ONE 5(1): e8593 - 20/01/2010 - doi:10.1371/journal.pone.0008593
- Japon numéro 528 (1/02/2010) - Ambassade de France au Japon / ADIT
- Polydor JP, Alzheimer, mode d'emploi, le livre des aidants, Ed. L'esprit du temps, 2009
- Banerjee S, Hellier J, Dewey M, et al. Sertraline or mirtazapine for depression in dementia (HTA-SADD): a randomised, multicentre, double-blind, placebo-controlled trial, Lancet, 2011;378:403-411
- Arendash GW, Sanchez-Ramos J, Mori T, Mamcarz M, Lin X, Runfeldt M, Wang L, Zhang G, Sava V, Tan J, Cao C. ; Electromagnetic field treatment protects against and reverses cognitive impairment in Alzheimer's disease mice. ; J Alzheimers Dis. 2010 ; Jan;19(1):191-210. PMID:20061638
- Arendash GW, Cao C. ; Caffeine and Coffee as Therapeutics Against Alzheimer's Disease. ; J Alzheimers Dis. 2010 Feb 24 (Résumé)
- Riemersma-van der Lek et coll. ; Effect of bright light and melatonin on cognitive and non cognitive function of elderly residents of group care facilities. A randomized controlled trial. Revue JAMA 2008 ; 299 : 2642-2655
- Cité dans un Article de Julie Luong intitulé Lumière et mélatonine contre la maladie d'Alzheimer( 15/10/2008)
- Étude Pixel
- HAS : Maladie d'Alzheimer et maladies apparentées : suivi médical des aidants naturels
- Patient Alzheimer-aidant : un reste à charge de 1 000 euros (Le quotidien du médecin n° 8887 p. 9 - 18/1/2011) notice 1855 ; citant une Etude de l' association France-Alzheimer
- Plan Alzheimer 2008-2012 : les Maisons d'accueil et d'intégration des malades Alzheimer sur la voie de la généralisation - Le Quotidien du Médecin, n° 8877, p. 8, 15/12/2010 Alzheimer, des raisons d'espérer ? - Marianne, n° 715, p. 64-69, 7/1/2011
- Joël Ménard, émission Avec ou sans rendez-vous sur le plan Alzheimer sur France Culture, 12 juillet 2011
- Alzheimer: placer ou non la personne atteinte?
- Quotidien belge "Le Soir" du 5 mars 2009, page 6, article "Santé - (Des recommandations concrètes) Pour mieux vivre avec Alzheimer
- Novoviva.fr
- Dr Douçot-Hermelin (Revue de Gériatrie 2008;33:787)
Voir aussi
Articles connexes
- Neurodon
- Les dernières informations:
Liens externes
Catégorie Alzheimer de l’annuaire dmoz
- Page du Gouvernement français concernant la maladie d'Alzheimer
- Portail d'Alzheimer de l'Union européenne partiellement en français
- Société Alzheimer du Canada
- (en) Journal of Alzheimer's Disease
Catégories :- Trouble mental organique, y compris trouble symptomatique
- Maladie neurodégénérative
Wikimedia Foundation. 2010.