- Modulateur Endocrinien
-
Modulateur endocrinien
La notion de modulateur endocrinien (ou perturbateur endocrinien, disrupteur endocrinien, leurre hormonal ou Xénooestrogène...) est une notion apparue à la fin du XXe siècle pour désigner toute molécule ou agent chimique composé, xénobiotique ayant des propriétés hormono-mimétiques.
Ces molécules agissent sur l'équilibre hormonal d'espèces vivantes animales (voire végétales dans le cas des phytohormones). Elles sont souvent susceptibles d'avoir des effets indésirables sur la santé en altérant des fonctions telles que la croissance, le développement, le comportement, la production, l'utilisation et le stockage de l'énergie, l'hémodynamique et la circulation sanguine, la fonction sexuelle et reproductrice.
Ces molécules agissent à très faible dose, du même ordre de grandeur que les concentrations physiologiques des hormones. Il ne s'agit donc pas d'un effet toxique au sens habituel du terme empoisonnement mais plutôt d'une perturbation discrète qui peut être difficile à reconnaître. Elles peuvent avoir un impact sur un individu, mais parfois aussi sur ses descendants (ex Distilbène chez la femme et ses descendantes) ou sur des populations entières (ex : escargots marins ou faune piscicole vivant dans des zones où des perturbateurs endocriniens sont très présents, dont les alligators de Californie ou grèbles exposés à du DDT ne pouvant plus se reproduire, qui ont fait l'objet d'études déjà anciennes).
Définitions officielles
L'UE a défini le perturbateur endocrinien (PE) comme agent qui parait influer (ou "perturber") le fonctionnement du système endocrinien et plus précisément comme « une substance ou un mélange exogène altérant les fonctions du système endocrinien, et induisant donc des effets nocifs sur la santé d’un organisme intact, de ses descendants ou sous-populations »
Le perturbateur endocrinien en tant qu'altéragène biologique, physique ou chimique répond à la définition normalisée du mot polluant retenue par l'AFNOR en France[1].
La réglementation REACH [2] permet d’identifier les perturbateurs endocriniens comme substances extrêmement préoccupantes, susceptibles de faire l’objet de mesures de gestion spécifiques[3].Trois modes d'action différents
Ces molécules interfèrent avec le fonctionnement des glandes endocrines ou des organes cibles par :
- imitation de l'action d'une hormone naturelle (comme une fausse clé dans les "serrures biologiques" qui existent dans les organes et cellules) ;
- blocage de l'action d'une hormone naturelle (en en saturant les récepteurs par exemple) ;
- perturbation (gêne ou blocage de la production, du transport, ou du métabolisme des hormones ou des récepteurs, induite par une action hormonale anormale dans l'organisme qui interfère avec les processus métaboliques ou de croissance et division cellulaire. Ces perturbations sont d'autant plus graves qu'elles se produisent tôt (fœtus, embryon, jeune enfant, car des effets irréversibles peuvent être induits, y compris des malformations génitales).
Découverte
Dès les années 1950, des études ont mis en évidence dans de nombreux pays industrialisés une diminution de la fertilité masculine — altérations morphologiques et baisse du nombre de spermatozoïdes —, une augmentation de la fréquence du cancer du testicule, de la prostate et du sein, ainsi qu'une puberté féminine de plus en plus précoce. Les études épidémiologiques, puis des expériences de laboratoire, ont montré que l'exposition à des molécules hormono-mimétiques était au moins en partie responsable de ces phénomènes.
L'hydrosphère est le réceptacle de nombreuses substances chimiques, dont des hormones naturelles et les métabolites d'hormones naturelles ou de synthèse contenues dans les pilules anticonceptionnelles, ou utilisées pour des traitements médicaux ou vétérinaires. Ces hormones s'avèrent présentes en grande quantité dans les eaux usées qui arrivent aux stations d'épuration, mais aussi, bien que moindrement pour nombre d'entre elles, dans les exutoires de station d'épuration d'eaux résiduaires urbaines. Certains organismes aquatiques sont estimés être de bons révélateurs (poissons affectés de troubles de la fertilité et d'anomalies de type intersexualité). Certaines espèces sont aussi des concentrateurs (moules, moule zébrée) d'une pollution des milieux aquatiques par ces effluents.
Dans les années 1960, aux États-Unis, la baisse de fertilité des visons constatée par les éleveurs de la région des Grands Lacs fut attribuée aux polluants bio-accumulés par les poissons. En 1962, dans Silent Spring, Rachel Carson met en évidence la toxicité reproductive du DDT. En 1988, les phoques de la mer du Nord furent décimés. En Grande-Bretagne, les poissons mâles vivant en aval d’une station d’épuration présentaient des caractères femelles. La découverte de l'altération du système reproducteur des alligators sauvages de Floride a relancé les travaux de recherche sur ce thème dans les années 1990. Au début des années 1990 il y a une prise de conscience de la présence dans l'environnement de substances capables de perturber le système endocrinien. En Europe, le Danemark, l'Allemagne et le Royaume-Uni ont été pilotes dans ce domaine de recherche. Les observations faites sur certaines populations animales soulèvent suffisamment de soupçons pour encourager la poursuite de la recherche dans le domaine.
Cinétique des perturbateurs endocriniens dans l'environnement
Les polluants organiques persistants (POP), tels le dichlorodiphényltrichloroéthane (DDT), les dioxines (PCDD) et les polychloro-biphényles (PCB), labiles et s’accumulant le long des chaînes trophiques, peuvent persister dans l’environnement plusieurs décennies, circuler dans différents compartiments environnementaux — atmosphère, biosphère, hydrosphère, lithosphère — au-delà des frontières : on a ainsi montré que les ours polaires pouvaient être contaminés par le DDT émis à des milliers de kilomètres.
Chez l'homme, la contamination peut également être alimentaire, naturelle avec les phytoœstrogènes de germe de blé, soja, bière/houblon...), ou artificielle avec des produits migrants des emballages, des résidus de pesticides, de détergents ou de médicaments, ou encore via l'ingestion d'animaux filtreurs contaminés tels que des coques[4]
Un perturbateur endocrinien avéré pour l'homme est le diéthylstilbestrol (DES), œstrogène synthétique prescrit en France entre 1948 et 1977 aux femmes enceintes afin de prévenir le risque d'avortement. Le 17-ß-estradiol — œstrogène naturel prescrit lors du traitement des femmes ménopausées (THS) — ainsi que la 17-α-éthynylestradiol qui est utilisé dans les pilules contraceptives. Les diverses substances qui sont ingérées par l'homme en tant que médicaments peuvent être retrouvées en aval des stations d'épuration puisque les installations sont relativement inefficaces pour détruire ces types de composés. La quantité d'agents chimiques qui s'y retrouve est fonction des conditions météorologiques (rayonnement ultraviolet, et température)[5],[6] et l'activité microbienne[7], [8].
Le bisphénol A, polybromodiphényléthers (PBDE), et une variété de phtalates et d'autres perturbateurs endocriniens sont communément trouvés à faible dose dans de nombreux produits et dans l’environnement[9]. Certains auteurs estiment que les risques pour la santé ne sont pas significatifs [10],[11] alors que d'autres estiment qu'il y a des preuves suffisantes pour dire que ces substances posent un risque pour la santé humaine et la fertilité humaine .[12],[13],[14],[15]
Le bisphénol A a notamment attiré l’attention en tant que composant du plastique de nombreux biberons. En mars 2007, un recours collectif (class action lawsuit) a été déposé en Californie contre les fabricants et détaillants de biberons en plastique, mais qui a échoué à prévenir les consommateurs que leurs produits contenaient du bisphénol A, qui selon certains pourrait altérer la santé et le développement des nourrissons et enfants[16].
Origine des différentes sources de contamination
Parmi les perturbateurs endocriniens, on trouve deux grandes classes qui sont d'origine soit naturelle, soit synthétique. Une partie des molécules antiandrogènes utilisées à des fins médicales (dont vétérinaires) ou anticonceptionnelles sont encore présentes dans les urines et ne sont pas filtrées par les stations d'épuration. Ils posent des problèmes graves de féminisation des poissons mâles dans les fleuves anglais en aval des stations d'épuration, ce qui préoccupe les pêcheurs et les écologues, mais aussi les professionnels de santé publique qui craignent des effets similaires chez l'Homme.
On a d'abord pensé que les stéroïdes œstrogènes provenant principalement des urines humaines étaient principalement responsables des syndromes de dysgénésie testiculaire observés chez les poissons. Une étude récente [17] a cherché si ce syndrôme était du à une ou plusieurs causes, et plus précisément si ces poissons n'étaient pas exposés à des cocktails de substances chimiques aux effets à la fois oestrogéniques et anti-androgèniques, et avec quels effets. Pour cela, les concentration et activité de produits (de type oestrogénes et anti-androgènes) ont été modélisés dans 51 cours d'eau du Royaume-Uni et comparés aux taux de poissons sauvages touchés par un syndrôme de féminisation dans ces rivières. Les analyses ont monté qu'outre des oestrogènes, les rivières contiennent diverses substances anti-androgène, trouvées dans presque tous les effluents de station d'épuration. De plus, les résultats de la modélisation confirment que les effets féminisants affectant les poissons sauvages pourraient être mieux modélisés et mieux prédits en prenant mieux en compte l'exposition à la fois aux anti-androgènes et aux œstrogènes ou aux antiandrogènes seuls. Les auteurs concluent au caractère multi-causale de la féminisation des poissons sauvages au Royaume-Uni, impliquant à la fois des produits stéroïdiens et des œstrogènes ou xénoestrogènes et d'autres contaminants (encore inconnu) aux propriétés anti-androgène. Cette étude a conclu que c'est bien un coktail de divers produits chimiques présents dans les eaux usées et dilué dans les rivières, qui inhibe la production de testostérone des poissons et leur capacité de bonne reproduction.
Types de perturbateurs endocriniens
On distingue souvent :
- Composés naturels :
- myco-œstrogènes : zéaralénone ;
- phyto-œstrogènes : isoflavonoïdes (par exemple présent dans le houblon et la bière).
- Composés synthétiques :
- antioxydants : alkylphénols ;
- composés organométalliques : sels de tributylétain (TBT) ;
- détergents : alkylphénols, nonylphénol, nonylphénol polyéthoxylés ;
- médicaments : stéroïdes synthétiques, tels ceux utilisés dans les pilules contraceptives ;
- pesticides : organochlorés (DDT, HCH, PCDD) ou organo-azotés (triazines) ;
- plastifiants : alkylphénols,nonylphénol, phtalates ;
- polychloro-biphényles (PCB).
Quelques exemples de xénoestrogènes
Les xénoestrogènes sont des substances ayant un potentiel œstrogénique (c'est-à-dire capable d'induire un caractère femelle) et émises dans l'environnement essentiellement suite à l'activité humaine. En voici quelques exemples :
Œstrogènes stéroidïens
Une forte diminution de la capture de poissons a été observée dans plusieurs rivières du Plateau suisse. Cette diminution pourrait venir de la présence de xénoestrogènes dans l'eau. La détermination de l'activité œstrogène moyenne dans l'eau d'une rivière est une variable difficile à mesurer. Pour pouvoir calculer une activité œstrogène totale (exprimé en équivalents en 17_ß-estradiol, EEQ), il faut pouvoir définir un facteur d'équivalence en 17_ß-estradiol (FFA) :
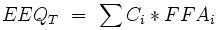 où Ci est la concentration de l'espèce i. Le groupe de molécules qui contribue le plus à augmenter cette valeur dans les effluents domestiques est le groupe des œstrogènes stéroïdiens[18].Généralement, le calcul est basé sur l’œstrone (FFA=0,4), le 17β-œstradiol (FFA=1) et le 17α-éthynylœstradiol (FFA=1,2).
où Ci est la concentration de l'espèce i. Le groupe de molécules qui contribue le plus à augmenter cette valeur dans les effluents domestiques est le groupe des œstrogènes stéroïdiens[18].Généralement, le calcul est basé sur l’œstrone (FFA=0,4), le 17β-œstradiol (FFA=1) et le 17α-éthynylœstradiol (FFA=1,2).Bisphénol A
Du bisphénol A[19], connu pour avoir des propriétés œstrogéniques, est trouvé dans l'eau, dans certains polymères (dont plastiques de biberons), emballages plastiques d’aliments, matériaux dentaires, boîtes métalliques (type boîtes de conserve), et les garnitures en métal de la nourriture en boîte.
Risque sanitaire : il est facteur de délétion de la spermatogenèse et est suspecté de jouer un rôle dans certaines fausses couches, obésité et certains cancers[20],[21],[22],[23]Agents ignifuges bromés
Certains de ces agents (polybromodiphényléthers ou diphényléthers polybromés dits « PBDE ») sont utilisés pour ignifuger des matériaux aussi divers que plastiques de téléviseurs, ordinateurs, composants électroniques, matériel électrique et d’éclairage, tapis, matériel de couchage, vêtements, composants automobiles, coussins en mousse et autres textiles ignifugés.
Risque sanitaire : les PBDE ont une structure chimique très similaire aux polychlorobiphényles (PCB), et ont les mêmes effets neurotoxiques, ce pourquoi il pourraient perturber les systèmes hormonaux thyroïdien et contribuer à une variété de troubles neurologiques et de déficit de développement (dont neurologiques avec pour conséquence de diminuer les facultés d'apprentissage et de cognition). Certaines populations pourraient être plus exposées, dont par exemple les pompiers et les personnels effectuant le tri des déchets électroniques. Une étude faite en Suède comparant les taux de PBDE chez différents types de travailleurs a montré que les recycleurs de matériel électronique étaient particulièrement touchés[24].L’usage de certains PBDE a été interdit dans l’UE en 2006.
Phtalates
Ces composés sont surtout utilisés comme plastifiants pour rendre les plastiques plus souples et plus flexibles. On trouve des phtalates dans de nombreux objets (jouets souples, revêtements de sol, équipements médicaux, cosmétiques, assainisseurs d'air, peintures, adhésifs, colles et encres)
Risques pour la santé : ils sont suspectés de poser problème, car ces produits sont connus pour perturber le système endocrinien des animaux (en laboratoire), et certaines études laissent penser qu’ils sont responsables de certaines malformations congénitales de l'appareil reproducteur masculin [25],[26]Un phtalate, le Bis (2-éthylhexyl) phtalate (DEHP) est présent dans certains plastiques utilisés dans le domaine médical (cathéters et sacs de sang). En 2002, la Food and Drug Administration a mis en garde contre l'exposition au DEHP des bébés de sexe masculin, sur la base des effets constatés sur les animaux de laboratoire. Selon la FDA : « L'exposition au DEHP a produit une série d'effets néfastes chez les animaux de laboratoire, mais les plus préoccupants sont les effets sur le développement du système reproductif mâle et de la production normale de spermatozoïdes chez les jeunes animaux ». La FDA ne dispose pas d’étude concernant l’homme, mais aucune étude ne permet d’exclure des effets similaires. Par précaution, l'exposition à ce produit par des organismes en développement doit être évitée estime la FDA [27],[28]
Autres soupçonnés perturbateurs endocriniens
Parmi les produits suspectés figurent : vinclozoline, zéaralénone, les dioxines, le polychlorobiphényle (BPC), des HAP, les furanes, les phénols, divers pesticides (dont organochlorés, tels que l’insecticide endosulfan, le DDT et ses dérivés).
Effets
Les modulateurs endocriniens peuvent perturber la maturation sexuelle, le développement des organes reproducteurs — malformation des gonades ou régression pénienne — ou la reproduction et entraîner des cancers hormono-dépendants. Ils peuvent également perturber la fonction thyroïdienne, altérer le système immunitaire ou engendrer des troubles du comportement.
De nombreuses études écotoxicologiques sur les organismes aquatiques, en particulier sur les mollusques et les poissons, ont montré que ces molécules pouvaient conduire jusqu'à l'imposex, c'est-à-dire le changement de sexe de l'animal. Les poissons sont souvent très sensibles aux contaminants de ce type : dans certains estuaires[29] de Grande-Bretagne ou en aval de stations d’épuration d'eaux résiduaires, on peut rencontrer des populations de poissons hermaphrodites. Chez des flets mâles vivant en milieu contaminé par des polluants hormono-mimétiques, des ovocytes apparaissent au milieu des spermatozoïdes.
Depuis plusieurs années, les chercheurs suspectent de nombreux composés chimiques d'être des perturbateurs endocriniens pour l'espèce humaine. Des méta-analyses publiées dans les années 1990 ont montré le déclin régulier de la qualité du sperme chez l’homme depuis 50 ans, en particulier en Amérique du Nord et en Europe. L’incidence du cancer du testicule augmente depuis plusieurs décennies dans un certain nombre de pays européens. Il y aurait une corrélation entre la présence de perturbateurs endocriniens et les malformations de l'appareil reproducteur, par exemple entre la présence de pesticides et la cryptorchidie ou entre des composés de type bisphénol A ou dioxines et l’hypospadias. Chez la femme, on constate des anomalies de la fonction ovarienne, de la fertilité, de la fécondation, de la gestation et de l’implantation utérine ainsi qu'un déplacement de l’âge de la puberté.
Les doses auxquelles les effets se manifestent peuvent être faibles : une ingestion par le rat de 20 microgrammes de bisphénol-A, un composé dont les éthers servent à protéger l'intérieur des boîtes de conserve, est suivie d'effets œstrogéniques.
Les modulateurs endocriniens peuvent agir in utero : à Seveso, il est apparu une prépondérance des naissances de filles parmi la population contaminées par la dioxine. Il a été montré que le DES était responsable de cancers de l'appareil génital et d'atteinte de la fertilité chez les hommes et les femmes exposés in utero. Le bisphénol-A et le diéthylstilbestrol (DES) provoquent une hypertrophie de la prostate des souris exposées in utero.
La synergie résultant des interactions entre xénobiotiques, micro-nutriments et médicaments peut aggraver les effets : l'exposition simultanée de la femelle immature à des faibles doses de flavonoïdes et d’œstradiol se traduit par un fort effet œstrogénique.
Comme pour tout produit chimique, l'effet dépend de la dose ; ainsi, si l'activité œstrogènique du nonylphénol est un fait, le potentiel d'action est très faible en comparaison avec les œstrogènes naturels : une étude de l'évaluation de risques sur les mammifères, préparée par la Commission européenne, a clairement indiqué que les effets dommageables résultant de la perturbation du système hormonal n'interviennent que pour des expositions nettement plus élevées que la toxicité générale. Pour les mammifères, le déclin de la population des phoques de la Baltique, exposés à des composés organochlorés (PCD et DDE) pourrait au moins en partie être expliqué par des perturbation des systèmes endocrinien et immunitaires. Chez les oiseaux contaminés par de faibles doses de DDT et/ou par des PCB, la coquille de l'œuf est amincie, et des anomalies de l'appareil reproducteur et congénitales sont plus fréquentes.
Études récentes
En Chine, une étude a montré une corrélation entre une sous-fertilité chez des hommes vivant à Hong Kong ayant consommé plus de quatre repas de poisson par semaine, qui ont aussi des taux de mercure plus élevés dans les cheveux (avec également des problèmes de peau et des autismes plus fréquent chez les enfants qui ont les plus haut taux de mercure (mesuré dans le sang, les cheveux et l'urine)[30].
Dans la réserve amérindienne d'Aamjiwnaang, au cœur de la « chemical valley » du Canada, on soupçonne des produits tels le mercure, les dioxines, l'HCB ou les PCB d'être à l'origine de la modification du sex-ratio constaté : une étude conduite par Constanze MacKenzie, de l'université d'Ottawa, a montré que le ratio à la naissance est passé de un garçon pour une fille en 1984 à un garçon pour deux filles en 1999. En outre, le taux de fausses couches est de 39 % contre 25 % habituellement et 23 % des enfants de moins de 16 ans souffrent soufrent d'ADHD (hyperactivité avec déficit d'attention), au lieu de 4 % habituellement.Entre les années 1999 et 2001, une étude sur les effets d'un oestrogène synthétique sur des populations aquatiques ont été réalisés. L’expérience prend place sur un lac entier dans la région des lacs expérimentaux dans le nord-ouest de l'Ontario au Canada.
En 2000, 24 ans après l'accident d'une usine d'herbicides à Seveso (Italie), une étude a montré que les hommes exposés au nuage de dioxines ont eu deux fois plus de filles que de garçons.
En 2002, à Ufa (Russie), des chercheurs ont montré que les travailleurs d'une usine d'herbicides, contaminés par les dioxines, ont eu des filles dans les deux tiers des cas.
État de la recherche
Thème de recherche situé à la confluence de la biologie, de la chimie et de la médecine, l'étude des modulateurs endocriniens demeure en plein essor.
Des expérimentations sont en cours pour juger de l'effet des perturbateurs endocriniens sur l'homme — tels la diminution de la spermatogenèse ou l'augmentation de malformations génitales — et de l'incidence de l'épigénétisme sur la sensibilité de certaines populations. Dans les années 2000, la recherche a été élargie aux effets sur le système endocrinien et, notamment, la production d'enzymes responsables de la différenciation sexuelle.
L'expérimentation animale est employée afin de mettre au point des tests de toxicité dose-réponse permettant de différencier l'effet perturbateur de l'effet hormono-mimétique chez l'homme. Par exemple, des souris sauvages, aux réactions normales, et des souris transgéniques ArKo (Aromatase knock out) — qui présentent une déficience en œstrogènes — sont utilisées pour mesurer les effets de molécules à activité œstrogénique (féminisante) — tel le méthoxychlore, un insecticide organo-chloré — ou anti-androgénique (anti-masculinisante) — telle la vinclozoline, un fongicide. Les molécules qui présentent un effet œstrogénique in vitro (test de E-screen) font l’objet d’études in vivo sur des rats femelles immatures ou ayant subi une ovariectomie.
Quelques études in situ sont faites ou en cours, notamment sur les poissons (ex : chevaine ou épinoche à trois épines[31]) chez laquelle la spiggin est un biomarqueur d'exposition aux androgènes). La vitellogénine, qui indique une exposition à des œstrogènes mimétiques, est le biomarqueur le plus utilisé. Certaines études s'intéressent aussi aux effets de la métabolisation des polluants organiques, du stress oxydant et de la neurotoxicité de certains perturbateurs, ou à d'éventuelles synergies. L’activité aromatase devrait aussi être mesurée en France vers 2008 (chez le chevaine, l’épinoche..).
Parallèlement aux études in situ, les mésocosmes et les microcosmes constituent des modèles pertinents pour étudier l'effet de ces molécules dans l'environnement, notamment dans l'hydrosphère. Réalistes d'un point de vue écologique et contrôlables, les mésocosmes permettent d'évaluer les effets à long terme sur la biocénose et le devenir des substances chimiques dans le biotope. En 2004, l'OCDE a organisé une campagne internationale d'intercomparaison des méthodes d'analyse de la vitellogenèse chez le poisson-zèbre (Brachydanio rerio).
Méthodes d'analyse et de détection
Une des premières approches est d'utiliser différents organismes vivants comme biodétecteurs. Les doses auxquelles les hormones et certains perturbateurs endocriniens peuvent agir sont tellement faibles que leur analyse pose un défi. Certains systèmes de biodétection peuvent donner une réponse à des concentrations en stéroïdes de l’ordre 10 à 1000 fois plus faible que les techniques permettant de doser les agents anabolisants (technique qui répond bien à des concentrations de l’ordre du nanogramme par millilitre). De plus, les faibles doses constituent souvent un mélange complexe et le biodétecteur révèle toutes ces substances.
Comme exemple de biodétecteurs on peut faire appel à des cellules humaines (MCF7) en culture ou d’autres espèces, les rats de laboratoire, des levures, les bactéries, le poisson zèbre. Chaque biodétecteur a ses particularités et ses problèmes éthiques. Par exemple, les cellules humaines MCF7 sont utilisées comme biodétecteur de composés œstrogènes depuis presque 20 ans. Ces cellules sont dérivées d’un cancer du sein et elles ont gardé plusieurs caractéristiques comme le fait d’être stimulées par la présence d’œstrogène. Les œstrogènes, ou les substances qui les imitent, fonctionnent en activant une protéine réceptrice de la cellule, qui régule tout un jeu de gènes, il suffit de compter les cellules au bout de quelques jours pour déterminer leur présence.
Un autre test in vitro utilisé est basé sur une souche de levure possédant un gène exprimant le récepteur humain aux œstrogènes, dit YES (yeast estrogen screen). Les levures ont la capacité, par une suite de réactions enzymatiques, de produire la β-galactosidase qui transforme la couleur jaune de départ du mélange en couleur rose qui absorbe à 540 nm en spectroscopie ultraviolet-visible[32].
Les taux plasmatiques en vitellogénine peuvent être mesurés chez certains types de poissons (truites saumonées). La vitellogénine est une protéine vitelline synthétisée par le poisson femelle mature. Elle est également produite chez le poisson mâle exposé à un perturbateur endocrinien. Les poissons mâles exposés à ces œstrogènes produisent des protéines d'œufs, ont des gonades plus petites et, dans les cas plus graves, produisent des œufs. La réponse biologique du poisson mâle qui est le taux plasmatique en vitellogénine est nettement accrue sur les sites à forte activité œstrogène. Pour permettre l’analyse du plasma contenant la vitellogénine on utilise un test ELISA (enzyme linked immunosorbent assay)[33]. En plus de la vitellogénine, il a été démontré qu’il peut avoir bioaccumulation des perturbateurs dans le foie, la bile et le gras[34].
Les diverses analyses prennent le plus souvent place dans des rivières puisqu’elles sont l’endroit établi pour le rejet des eaux usées. Pour une rivière, le débit est fortement touché par les précipitations. La répartition des produits chimiques est tributaire des conditions météorologiques (UV et température) et de l’activité microbienne. Il est donc difficile de déterminer une concentration constante à laquelle les organismes vont faire face. Il est donc nécessaire d’obtenir un échantillonnage dans le temps. La première méthode pour pallier cette difficulté est l’utilisation de biocapteurs comme les poissons.
Plusieurs autres techniques d’extraction existent pour l’eau brute ou filtrée. L’eau peut être vectrice de perturbateurs endocriniens à double titre : les molécules qui sont les plus solubles ou les plus concentrées peuvent être entraînées sous forme dissoute. Pour ce qui est des molécules moins solubles ou répandues depuis un certain temps dans l’environnement, elles peuvent être associées à des particules de sol et des sédiments en suspension dans l’eau. L’estimation de la contamination de l’eau doit apparaître dans sa globalité. Finalement l’évaluation de la contamination de l’eau peut être envisagée sous l’angle de la concentration de l’eau en perturbateur endocrinien ou en termes d’exposition. Pour pallier la concentration, un préleveur automatique ou instantané (dit actif) peut être utilisé et pour déterminer l’exposition, aussi l’utilisation de capteurs passifs est possible.
L’extraction liquide-liquide au dichlorométhane est la plus largement utilisée, puisque cette méthode possède un bon rendement, un large spectre d’action et cette technique est aisée à mettre en œuvre. Elle utilise les caractéristiques physico-chimiques de la molécule de dichlorométhane qui sont : polaire, non miscible à l’eau et lipophile. Un autre technique fait intervenir des cartouches (SPE). Ces pièges fixent les molécules lorsque l’eau est passée au travers. Un mélange de solvants peut ainsi être employé pour éluer ces cartouches et recueillir les molécules recherchées. La solution obtenue est de plus faible volume et constitue une étape de préconcentration. L’extraction est donc sélective à des molécules spécifiques puisque tous les produits ne sont pas nécessairement retenus par la cartouche et élués par le solvant utilisé comme éluant. Ces capteurs sont souvent des instruments automatisés permettant la prise de données dans des intervalles de temps. Néanmoins, ce type d’appareil est sujet à des inconvénients majeurs comme l’utilisation de source d’énergie, le bris de pièce mécanique, le dérèglement dû aux conditions météorologiques.
Une autre méthode utilise une technique récente soit l’usage de capteur passif qui intègre la contamination dans le temps. L’exposition plutôt que le flux de contaminant est estimée. Les dispositifs se présentent sous la forme de poche SPMD (pour semi-permeable membrane device) ou de capteurs POCIS (pour polar organic componds integrative samplers). Dans ces capteurs il y a une résine d’une capacité d’absorption spécifique à l’hydrophobicité de polluants organiques. Les SPMD sont utilisés pour les composés hydrophobes (PCB, organochlorés) alors que les POCIS sont pour les composés plus hydrophiles comme les résidus pharmaceutiques. Les POCIS possédant une phase permettant la rétention de composés tels que les pesticides (Particule de Isolute ENV+ et Ambersorb1500 dispercé sur S-X3 BioBeads) ont démontré une meilleure sélectivité pour les xénoestrogènes[35].
Pour réaliser les tests quantitatifs la GC-MS ou la LC/MS/MS peut être utilisée. Une des méthodes utilisées par le gouvernement du Québec pour doser les perturbateurs endocriniens est la GC/MS. Les hormones et autres substances sont extraites avec l’aide de colonne Oasis HLB. L’extraction prend un volume de 1 litre et met 14 jours à être réalisée, la colonne préconcentre les analytes à un volume de 500 mg. Par la suite, le diéthyl éther est utilisé pour laver cette phase, et conditionné avec le méthanol. On lave encore avec un mélange d’eau/méthanol dans des proportions de 60 :40 et une autre élution avec diéthyl éther/eau 90 :10. Une purification sur gel de silice avec le même solvant d’élution est la prochaine étape. Finalement, avant l’analyse par GC/MS une déviation au BSTFA est réalisée. Les caractéristiques de la colonne ainsi que les divers paramètres expérimentaux peuvent être observés dans le lien externe correspondant.
Moyens de lutte
La prévention des risques requiert une bonne connaissance des propriétés toxicologiques des molécules et la restriction ou l'interdiction de leur utilisation ; de nombreux programmes de recherche ont donc été mis en place, et la directive REACH devrait élargir le champ de la connaissance dans ce domaine, même si certains produits y échappent (dont les pesticides).
Divers états prennent des mesures contraignantes. Par exemple, la commercialisation, la fabrication, l’importation et l’exportation des jouets et articles de puériculture contenant des phtalates ont été interdits en France en 1999. Le nonylphénol a été interdit en Allemagne en 2003. Quelques pesticides dont le chlordécone et l'atrazine (qui perturbait gravement le développement des grenouilles) ont été interdits, pour ne citer que les plus médiatisés. L'usage du DDT a été mondialement interdit en 1973, mais alors qu'on le trouve encore dans l'environnement et les graisses de nombreux organismes, des pressions existent pour réautoriser son usage dans les pays pauvres.Les eaux usées, contaminées par les différents perturbateurs endocriniens (ex : xénoestrogènes ou médicaments) sont traitées au travers des stations d’épurations (STEP). Dans ces traitements, les composés chimiques peuvent être dégradés entièrement ou partiellement, créer des boues d’épuration par leur absorption sur des particules en suspension. Différents facteurs comme le type de traitement ou le temps de séjour peuvent influencer l’efficacité de l’élimination des polluants au travers des STEP. La problématique découle de l’inefficacité des STEP à retenir certaines substances, il s’en suit que ces dernières se retrouvent dans les eaux traitées qui vont alors contaminer les eaux de surface. Il a été démontré que le traitement additionnel des eaux usées à l’ozone ou au charbon actif permet une meilleure élimination des micropolluants. Malheureusement l’efficacité économique des différentes options de mise à niveau des stations d’épuration rencontre des obstacles au niveaux des divers niveaux de gouvernements.
Stratégies
Dans le monde
Plusieurs États ont des programmes nationaux sur ce thème (Japon, USA, Suisse, France.). L'OCDE y travaille également, avec la commission européenne, dont sur les méthodes d'essai et d'évaluation des PE ; d'abord pour la santé humaine puis pour l'environnement. Diverses commissions internationales visant notamment la protection des océans (OSPAR, HELCOM...) s'intéressent aussi à ces questions.
la recherche porte généralement sur les thèmes suivant :
- Le criblage, c'est à dire les méthodes analytiques (chimiques, tests biologiques, biomarqueurs d'effets) pour déterminer le taux de ces polluants dans un milieu ;
- La mesure de la répartition et durée de vie dans l’environnement (eau, sol, air, sédiments, aliments..) et/ou dans les organismes vivants (monitoring, biomonitoring...)
- L’identification des dangers et l’évaluation des risques, la mesure du degré d'impact effectif (chez quelques espèces jugées représentatives ou faciles à étudier) ;
- La compréhension des mécanismes d’action (et d'éventuels effets épigénétiques), mais aussi de dégradation naturelle de ces molécules, par des études écocinétiques et toxicologique des PE ;
- L'étude des voies métaboliques dans l’organisme et les étapes clef de la biodégradation ;
Des études de population ou écoépidémiologiques ont mis en évidence des effets à long terme. Elles ont permis de développer des modèles animaux et de commencer à développer des modélisations des effets des perturbateurs endocriniens.
États-Unis : Par exemple, l’EPA (Agence de protection de l’environnement des États-Unis) s’est donnée comme objectif de tester des milliers de substances chimiques différentes au cours des prochaines années pour en vérifier les effets endocriniens.Canada : Des mesures d’alkylphénols polyéthoxylés entrant dans la composition de pesticides ont été prélevés dans plusieurs cours d’eau.
Suisse Au début des années 2000, le Conseil fédéral le Fonds national a lancé un programme de recherche en Suisse (PNR 50 visant à développer des stratégies pour évaluer les risques et dangers de l’exposition du vivant aux perturbateurs endocriniens, pour 2001-2007 ; 17 projets subventionnés en 2001, et 7 autres en 2003, ayant abouti à des conclusions et recommandations pour les autorités et les industries, afin de limiter les effets négatifs de ces substances et des futurs composés développés.
France : Un « Programme national de recherche sur les perturbateurs endocriniens » a été lancé en 2005, en lien avec l’ANR et l’AFSSET, suite aux recommandations du Comité de la Prévention et de la Précaution (CPP) consécutive à une saisine sur les perturbateurs endocriniens (conclusions publiées en décembre 2003 ), ainsi qu’à l’annonce faite en juin 2004 par monsieur le ministre en charge de l'Environnement S. Lepeltier. Un nouvel appel à projet a été lancé mi-2008 ciblant des « questions orphelines », dont celle des impacts sur fonction thyroïdienne ou le système immunitaire.
Union européenne
L'UE a mis en place une « Stratégie communautaire concernant les perturbateurs endocriniens » pour « aborder, d'urgence, le problème des perturbateurs endocriniens nocifs à la santé et à l'environnement »[36],[37],[38]. Cette stratégie prévoit trois types de mesures : à court, moyen et long terme.
À court terme, l'UE veut faire évaluer une liste prioritaire de molécules (« liste prioritaire PE ») fortement suspectes d'effets hormonaux, en identifiant les manques de connaissances. L'UE veut utiliser les instruments législatifs existants, dont REACH (Règlement relatif à l'évaluation des risques) et la directive relative à la classification des substances dangereuses, pour établir des programmes de surveillance qui doivent estimer les doses et durées d'exposition aux substances PE « prioritaires » et en étudier les effets. Il est aussi prévu d'identifier d'éventuels cas particuliers et les groupes vulnérables à certaines substances (ex : enfants...) si ces substances ne sont pas déjà réglementées, elles devront être inscrites sur la liste des PE prioritaires ; Des réseaux d'échange, d'information et de consultation des acteurs (niveau international, Commission, États membres, industrie, etc.) sont également prévus. L'UE veut une « pleine information » de la population, notamment sur les activités entreprises, les mécanismes, la liste prioritaire PE. L'UE finance diverses études dès les années 2000, y compris interrégionales via les crédits Interreg.
En 2000, 553 substances artificielles et 9 hormones de synthèse ou naturelles ont été inscrites dans la « liste prioritaire ». Des actions prioritaires ont été listées pour évaluer le rôle de ces substances, et une conférence a été organisée par la Commission sur les perturbateurs endocriniens (18-20 juin 2001, en Suède). Un appel à propositions de recherche de mai 2001 a bénéficié d'un budget de 20 millions d'euros. Le Livre blanc sur la stratégie pour la future politique dans le domaine des substances chimiques inclut les PE et la future directive sur la sécurité générale des produits devrait permettre de prendre plus facilement des « mesures d'urgence au niveau communautaire ». Une Stratégie communautaire sur le mercure qui est aussi un perturbateur endocrinien a également fait l'objet d'une communication[39],[40].À moyen terme, l'UE veut contribuer à identifier et évaluer les perturbateurs endocriniens, développer des produits de substitution et des tests capables d'identifier les PE, notamment via le cinquième programme-cadre de recherche et développement et les initiatives privées.
À long terme, l'UE veut adapter/modifier la législation pour prendre en compte les PE, notamment via le Règlement (CEE) n° 793/93 concernant l'évaluation des risques et la directive 67/548/CEE concernant la classification des substances dangereuses. Le bon état écologique prévu par la Directive cadre sur l'eau doit intégrer les aspects PE.
France
Un PNRPE (Programme national de recherche sur les perturbateurs endocriniens) sera animé par l’AFSSET à partir de 2009, avec un budget de 2 millions €/an.
Voir aussi
Articles connexes
Gonades
- Gamète, Gamétogénèse,
- Ovaire, ovules,
- Ovogenèse
- spermatogonies,
- Cellules de Leydig,
- Cellules de Sertoli,
- spermatogenèse, Spermiogenèse
- Spermatozoïde
- Sperme,
- spermogramme, Spermocytogramme,
- Compétition spermatique
Système hormonal
- Système endocrinien,
- Hormone,
- Testostérone,
- Gonadostimulines,
- Hypophyse,
- Glande surrénale
- Hormone Lutéinisante ou LH (contrôle la sécrétion pulsatile de testostérone),
- Hormone folliculo-stimulante ou FSH,
- Fécondation assistée.
Malformations, anomalies :
- Diphallia,
- hypospadias,
- micropénis
- distance ano-génitale (indice chez le garçon d'exposition prénatale à des hormones féminisantes),
- Délétion de la spermatogenèse ;
- tératospermie,
- azoospermie,
- asthénospermie
- oligoasthénotératospermie ou oligospermie,
- Nécrospermie,
- Cryptozoospermie,
- Syndrome de l'insensibilité aux androgènes
Cancers ;
Médecine, Recherche
- santé reproductive, santé-environnement,
- Environnement
- Toxicologie, écotoxicologie
- Reprotoxicité
- Fertilité,
- Reproduction (biologie), Procréation,
- Fécondation in vitro,
- clonage,
- CECOS, Donneur de sperme, Banque du sperme.
Divers ;
Liens externes
- (en) Évaluation mondiale des connaissances scientifiques sur les perturbateurs endocriniens (2002, Programme International sur la Sécurité Chimique de l'OMS)
- (fr) Consensus scientifique sur les perturbateurs endocriniens - un résumé pour non-spécialistes du rapport de l'OMS par GreenFacts
- (fr)Les perturbateurs endocriniens et leurs impacts sur les milieux aquatiques (Rencontres scientifiques de l’eau, jeudi 23 novembre 2006, Agence de l'eau Artois-Picardie).
- (fr)Perturbateurs endocriniens dans les milieux aquatiques(P Vasseur, Rencontres scientifiques de l'Agence de l'Eau Artois-Picardie, 23 nov 2006, Villeneuve-d'Ascq)
- (fr)Colloque « Perturbateurs endocriniens et qualité des milieux aquatiques », 23 octobre 2007.
- (fr)Exposé de C Minier : Contamination et effets des xéno-oestrogènes dans le compartiment aquatique en Manche orientale(Rencontres scientifiques de l'Agence de l'Eau Artois-Picardie, 23 nov 2006, Villeneuve-d'Ascq)
- (fr)Perturbateurs endocriniens et santé humaine (Luc Multigner (INSERM), Rencontres scientifiques de l'Agence de l'Eau Artois-Picardie, 23 nov 2006, Villeneuve-d'Ascq, France)
- (fr) - Résumé des conditions d'analyses (par GC/MS)
- (fr) Appel à Propositions de Recherche 2008 (Programme National de Recherche « Perturbateurs endocriniens » (PNRPE)
- (en) Endocrine disruption in the marine environment (Programme anglais EDMAR, initié en 1998, qui a étudié 14 estuaires et éprouvé de nouvelles méthodes de détection des perturbateurs endocriniens)]
- (fr) Hormones dans l'eau : Quels effets sur l'homme et les animaux? - Département fédéral de l'environnement, des transports, de l'énergie et de la communication (DETEC), Suisse
Bibliographie
Mi-2009, La société internationale d’endocrinologie a lors de son colloque annuel (10 juin 2009) réalerté sur la question des perturbateurs endocriniens et de leurs effets sur la reproduction, mais aussi les cancers du sein et de la prostate, et pathologies cardiovasculaires, de la thyroïde et l’obésité. Elle a appelé à réduire l’exposition de la population à ces molécules ; au nom du principe de précaution. Elle a publié une « déclaration scientifique » [41],[42] dans la revue Endocrine Reviews.
Notes et références
- ↑ Dictionnaire du vocabulaire normalisé de l'Environnement, AFNOR
- ↑ Règlement du 18 décembre 2006
- ↑ Définitions reprise par l'appel à projet français 2008 (Programme national de recherche «Perturbateurs endocriniens» (PNRPE)), page 1
- ↑ étude du CIMAR et de l'UAlg : « Alteracao hormonal nas ameijoas provocada por quimicos nas aguas pode afectar fertilidade humana » - CienciaHoje (avril 2008), brève reprise par l'ambassade de France (Bulletin ADIT n° 54559)
- ↑ Bertilsson, S.;Widenfalk, A. Photochemical degradation of PAHs in freshwaters and their impact on bacterial growth - influence of water chemistry. Hydrobiologia 2002, 469,23-32.
- ↑ Maruyama,K; Yuan, 0.; Otsuki, A. Seasonal changes in ethylene oxide chain length of poly(oxyethylene)alkylphenyl ether nonionic surfactants in three main rivers in Tokyo. Environ. Sci. Technol. 2000, 34, 343-348.
- ↑ Jurgens, M.D.; Holthaus, K. I. E.; Jonhson, A. C.; Smith, J. J. L.; Hetheridge, M.; Williams, R. J. The potential for estradiol and ethinylestradiol degradation in English rivers. Environ. Toxicol, Chem. 2002, 21, 480-488
- ↑ Kang, J.-H,; Kondo, F. Effects of bacterial counts and temperature on the biodegradation of biphenol A in river water. Chemosphere. 2002, 49, 493-498.
- ↑ National Report On Human Exposure to Environmental Chemicals (CDC, USA)
- ↑ Endocrine disruptors and human health--Is there a problem? An update. PMID 10856020
- ↑ Evidence of effects of environmental chemicals on the endocrine system in children PMID 12837917
- ↑ Environment and health: 6. Endocrine disruption and potential human health implications[1]
- ↑ How strong is the evidence of a link between environmental chemicals and adverse effects on human reproductive health? "Little definite data links human reproductive disorders or cancers with exposure to environmental chemicals..."[2]
- ↑ Hypospadias and Endocrine Disruption: Is There a Connection?[3]
- ↑ Neurodevelopment and Endocrine Disruption[4]
- ↑ Calif. Lawsuit Targets Baby Bottles With Chemical Additive[5]
- ↑ Statistical modelling suggests that anti-androgens in wastewater treatment works effluents are contributing causes of widespread sexual disruption in fish living in English rivers, Susan Jobling et al., Environmental Health Perspectives, en ligne le 7 janvier 2009 (Télécharger l'étude en pdf)
- ↑ Routledge, E. J.; Sheahan, D.; Desbrow, C.; Brighty, G. C,; Waldock, M.; Sumpter, J. P. Identification of estrogenic chemicals in STW effluent. 2. In vivo responses in trout and roach. Environ. Sci. Technol. 1998, 32, 1559-1565
- ↑ Temporal Variability and Predictors of Urinary Bisphenol A Concentrations in Men and Women
- ↑ Babies, Bottles, and Bisphenol A: The Story of a Scientist Mother[6]
- ↑ Toxic Chemical Leaches from Popular Baby Bottles[7]
- ↑ Replace bisphenol A or a child's health?[8]
- ↑ California's Bogus Baby Bottle Scare [9]
- ↑ Article Seattlepi/sur les PDE
- ↑ Jane S Fisher, Environmental anti-androgens and male reproductive health: focus on phthalates and testicular dysgenesis syndrome, journal = REPRODUCTION, Vol 127, Chap 3, pages 305 à 315, 2004 Voir
- ↑ Swan, S.H. et al. 2005. An overview of this paper is given in the same volume: Julia R. Barrett, Phthalates and Baby Boys: Potential Disruption of Human Genital Development, Environ. Health Perspect. 2005 Aug; 113(8): A542.
- ↑ FDA Public Health Notification: PVC Devices Contenant le Plastifiant DEHP [10]
- ↑ rFDA Public Health Notification: PVC Devices Containing the Plasticizer DEHP[11]
- ↑ Programme Endocrine disruption in the marine environment] (EDMAR), entamé en 1998, développé sur les 14 plus grands estuaires du Royaume-Uni
- ↑ L. Zhanga and M.H. Wong, a, "Environmental mercury contamination in China: Sources and impacts ", Croucher Institute for Environmental Science and Department of Biology, Hong Kong Baptist University, Hong Kong, PR China, reçu le 23 mars 2006; mis en ligne par Environment International, Volume 33, Issue 1, January 2007, Pages 108 à 121 le 17 aout 2006.
- ↑ Étude in situ de la réponse d'une batterie de biomarqueurs chez l'épinoche à 3 épines / Biosurveillance)
- ↑ Murk et al. (2002) Environ. Toxicol. Chem.
- ↑ Vermeirseen, E. L. M.; Burki, R.; Joris, C.; Peter, A.; Segner, H.; Suter, M. J.-F.; Burkhardt-Holm, P. Characterization of the estrogenicity of Swiss midland rivers using a recombinant yeast bioassay and plasma vitellogenin concentrations in feral male brown trout. Environ. Toxicol. Chem. 2005, 24, 226-2233.
- ↑ Vethaak, A. D.; Rijs, G. B. J.; Schrap, S. M.; Ruiter, H.; Gerritsen, A.; Lahar, J. Estrgens and xeno-œstrogens in the aquatic Environment of The Netherlands: Occurence, Potency and Biological Effects; RIZA/RIKZ: Lelystad/Den Haag. Netherland 2002.
- ↑ 1Characterization of Environmental Estrogens in River Water Using a Three Pronged Approach: Active and Passive Water Sampling and the Analysis of Accumulated Estrogens in the Bile of Caged FishEtiënne L. M. Vermeirssen, Oliver Körner, René Schönenberger, Marc J.-F. Suter, and Patricia Burkhardt-Holm. Environ. Sci. Technol., 2005, 39, (21), pp 8191–8198.
- ↑ Stratégie communautaire concernant les perturbateurs endocriniens
- ↑ Communication de la Commission au Conseil et au Parlement européen, du 17 décembre 1999, sur une stratégie communautaire concernant les perturbateurs endocriniens [COM(1999) 706 final - Non publié au Journal officiel]
- ↑ Communication de la Commission au Conseil et au Parlement européen, du 14 juin 2001, sur la mise en œuvre de la stratégie communautaire concernant les perturbateurs endocriniens [COM(2001) 262 final - Non publié à ce jour]
- ↑ Stratégie communautaire sur le mercure
- ↑ Communication de la Commission, du 28 janvier 2005, « Stratégie communautaire sur le mercure » (COM(2005) 20 - Journal officiel C 52 du 2 mars 2005)
- ↑ Diamanti-Kandarakis et al. ; «Endocrine-Disrupting Chemicals: An Endocrine Society Scientific Statement» ; Endocrine Reviews vol. 30, n°4, p. 293-342 (juin 2009) (Déclaration, en anglais, 56 pages, PDF, consulté 2009 06 17)
- ↑ Résumé de l'étude EDRV, en Anglais
Systèmes et organes du corps humain
Catégories : Biochimie | Toxicologie | Pollution | Polluant | Perturbateur endocrinien
Wikimedia Foundation. 2010.
