- Atrazine
-
Atrazine 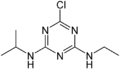
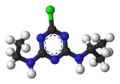
Formule semi-développée et représentation 3D de l'atrazine Général Nom IUPAC 1-chloro-3-ethylamino-5-isopropylamino-2,4,6-triazine No CAS No EINECS SMILES InChI Apparence cristaux incolores[1]. Propriétés chimiques Formule brute C8H14ClN5 [Isomères] Masse molaire[2] 215,683 ± 0,01 g·mol-1
C 44,55 %, H 6,54 %, Cl 16,44 %, N 32,47 %,Propriétés physiques T° fusion 173 à 177 °C[1] T° ébullition 200 °C Solubilité dans l'eau à 25 °C : nulle[1] Masse volumique 1,2 g·cm-3[1] Pression de vapeur saturante à 20 °C : très basse[1] Précautions Directive 67/548/EEC 
Xn
NPhrases R : 43, 48/22, 50/53, Phrases S : (2), 36/37, 60, 61, Transport - 2763 SGH[4] 

AttentionClassification du CIRC Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[3] Unités du SI & CNTP, sauf indication contraire. L'atrazine, 2-chloro-4-(éthylamine)-6-(isopropylamine)-s-triazine, est la substance active d’un produit phytosanitaire (ou produit phytopharmaceutique, ou pesticide), qui présente un effet herbicide, et qui appartient à la famille chimique des triazines (caractérisée par un cycle s-triazine).
Alors qu'elle a été interdite dans l'Union Européenne, l'atrazine est utilisée dans un grand nombre de pays pour le traitement en pré et post-émergence des mauvaises herbes dans de nombreuses cultures annuelles ou pérennes. L’atrazine se lie à la plastoquinone, une protéine de transport du système de photo-synthèse, inhibant le transport d’électrons. L'atrazine est l'un des herbicides les plus couramment utilisés et selon l’Agence de protection de l'environnement des Etats-Unis (EPA) les États-Unis ont utilisé 77 millions de livres d'atrazine en 2003.*
Sommaire
Caractéristiques physico-chimiques
Les caractéristiques physico-chimiques dont l'ordre de grandeur est indiqué ci-après, influencent les risques de transfert de cette substance active vers les eaux, et le risque de pollution des eaux :
- Hydrolyse à pH 7 : très stable,
- Solubilité : 33 mg·l-1,
- Coefficient de partage carbone organique-eau : 90 cm3·g-1. Ce paramètre, noté Koc, représente le potentiel de rétention de cette substance active sur la matière organique du sol. La mobilité de la matière active est réduite par son adsorption sur les particules du sol.
- Durée de demi-vie dans les sols : 44 jours en moyenne (varie de 15 à 100 jours, voire plus selon le type de sol, la présence ou l'absence de certaines bactéries, le travail du sol et sa température[5]. Ce paramètre, noté DT50, représente le potentiel de dégradation de cette substance active, et sa vitesse de dégradation dans le sol.
- Coefficient de partage octanol-eau : 2,75. Ce paramètre, noté log Kow ou log P, mesure l’hydrophilie (valeurs faibles) ou la lipophilie (valeurs fortes) de la substance active.
Toutefois, l'atrazine est l’herbicide le plus largement employé dans les programmes de préservation des sols, qui sont des systèmes conçus pour prévenir l'érosion des sols et diminuer le ruissellement d’un facteur de l'ordre de 90 pour cent.
Biodégradation
Le début de la biodégradation de l’atrazine peut survenir selon trois mécanismes connus. L'atrazine peut d’abord être déchlorée, puis le cycle restant est enlevé par les amidohydrolases. Ces étapes sont effectuées par les enzymes Atz A et C, respectivement, qui sont communément produites par les organismes vivants les plus répandus. Le produit final, l’acide cyanurique, servira ensuite de source de carbone et d'azote. Le micro-organisme le plus connu pour utiliser cette voie est l’ADP d’une souche de pseudomonas . L'autre mécanisme implique la désalkylation du groupe amine. Dans ce mécanisme la déchloration peut être réalisée dans une seconde étape pour finalement aboutir éventuellement à la formation d’acide cyanurique, ou bien à un produit final qui est le 2-chloro-4-hydroxy-6-amino-1,3,5-triazine, pour lequel on ne connaît pas encore actuellement de voie de dégradation ultime. Cette voie métabolique peut être empruntée par une seule espèce de Pseudomonas ou par un grand nombre de bactéries.
L’absorption de l'atrazine par les sols détermine sa biodisponibilité pour la dégradation, qui est réalisée surtout par des micro-organismes. Un faible taux de biodégradation de l’atrazine est la conséquence d’une faible solubilité et d’une absorption dans des zones inaccessibles pour les bactéries. L'ajout de tensioactifs augmente la solubilité, et catalyse sa dégradation. Avant d'utiliser un tensioactif, il est indispensable d’évaluer ses effets sur l'environnement, ainsi que son utilisation comme source préférentielle d'énergie et de carbone. L'atrazine est elle-même une faible source d'énergie en raison du niveau élevé d’oxydation des atomes de carbone de son cycle. Il est catabolisé comme source de carbone et d'azote dans des environnements limités bien que sa disponibilité optimale en azote et en carbone soit inconnue. Il a été démontré que l'azote inorganique augmentait alors que le catabolisme de l'atrazine alors que l'azote organique le diminuait. De faibles concentrations en glucose peuvent avoir pour effet de diminuer la biodisponibilité par le biais de la formation d'atrazine liée, tandis que des concentrations plus élevées peuvent stimuler le catabolisme de l'atrazine[6].
Les gènes AtzA-C ont été retrouvés partout et on a constaté qu’ils étaient largement répandus dans le monde entier chez les micro-organismes capables de dégrader l'atrazine. Cela pourrait être la conséquence d’une diffusion massive des gènes AtzA-C à l'échelle mondiale. Dans l’ADP de l’espèce Pseudomonas, les gènes atz sont situées sur le même plasmide que les gènes responsables du catabolisme du mercure sans toutefois être contigus. En laboratoire ce plasmide est transférable par conjugaison aux bactéries Gram négatives ce qui pourrait facilement conduire à une diffusion mondiale étant donné les quantités d'atrazine et de mercure produites actuellement. Les gènes AtzA-C ont également été retrouvés chez une bactérie Gram positive, mais dans ce cas ils sont situés sur un chromosome[7]. Cela n'est pas surprenant en raison de la présence d'éléments d'insertion accompagnant chaque gène et de la détection de ces gènes sur différents plasmides. Leurs configurations sur ces différents plasmides suggèrent que l'insertion de ces éléments est impliquée dans la formation de cette voie spécialisée de catabolisme.
Écotoxicologie
La dose létale 50 (DL50) par voie orale de l'atrazine a été fixée aux valeurs suivantes :
- DL50 chez le rat :3 090 mg·kg-1,
- DL50 chez la souris : 1 750 mg·kg-1,
- DL50 chez le lapin :750 mg·kg-1,
- DL50 chez le hamster : 1000 mg/Kg,
La DL50 cutanée est de :
- 7 500 mg·kg-1 chez le lapin,
- plus de 3 000 mg·kg-1 chez le rat.
La LC50 1 heure par inhalation est supérieure à 0,7 mg·l-1 chez le rat. La LC50 4 heures pour l'inhalation est de 5,2 mg·l-1 chez le rat.
Sur le plan de l’écotoxicologie, les concentrations létales 50 (CL50) dont l'ordre de grandeur est indiqué ci-après, sont observées :
Mais outre ces effets toxiques évidents sur la flore (l'atrazine étant un herbicide), les principaux effets écotoxiques et écologiques de l'atrazine pourraient venir non de sa toxicité directe mais de ses effets de perturbateur endocrinien et semble-t-il d'un effet de dépression de l'immunité, au moins chez certaines espèces ou groupe d'animaux.
En effet, non seulement l'atrazine (second herbicide le plus utilisé après le Roundup aux États-Unis), s’est montré un puissant perturbateur endocrinien pour les amphibiens anoures (grenouilles, crapauds), en mimant l'action d'une hormone féminisante chez le mâle (œstrogène), mais elle rend les salamandres macrodactylum (espèce nord américaine vivant souvent à proximité des lieux de traitement) beaucoup plus sensibles aux infections notamment par le virus « Ambystoma tigrinum Virus » (ATV) l'une des deux maladies émergentes qui tuent les amphibiens, dont les salamandres par hémorragies internes. L’atrazine est donc suspectée d’être une des causes du phénomène récent d’explosion des infections fongiques et virales qui déciment les amphibiens sur toute la planète.
Dans une expérience récente[8], 384 larves de salamandres exposées à des taux d’atrazine identiques à ceux mesurés dans leur milieu naturel, puis exposées (à la 12 ème semaines de développement) au virus ATV pendant 3 semaines se sont montrées deux fois plus sensibles au virus que le groupe témoin.
Dans le domaine des risques de synergie, quand l’atrazine est combinée au nitrate de sodium (engrais le plus commun et le plus utilisé, notamment là où l’atrazine est la plus employée, et par ailleurs très soluble dans l’eau), les taux de lymphocytes chutent d'environ 20%.
Les amphibiens sont généralement considérés comme de bons bioindicateurs, parce qu’ils vivent à la fois dans l’eau et dans l’air, et que leur peau est plus perméable que celle des hommes. D’autres études ont mis en évidence un lien entre l'atrazine, le cancer du sein et le cancer de la prostate. En France, l'utilisation de l'atrazine est interdite par la réglementation depuis 2003, et par l'Union Européenne depuis 2007 avec la décision 2004/141/CE (l'interdiction étant plus ancienne en l’Allemagne). Mais ce produit y a été très utilisé, et il peut être rémanent dans les sols et à l’abri des UV solaires.
Controverses
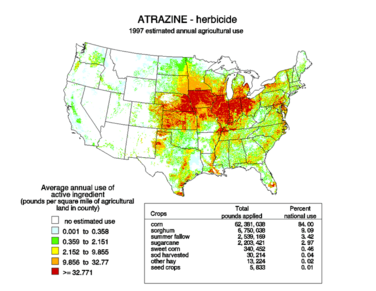 Utilisation de l’atrazine en livres par mille carré par comté. L'atrazine est l'un des herbicides les plus couramment utilisés aux États-Unis[9]
Utilisation de l’atrazine en livres par mille carré par comté. L'atrazine est l'un des herbicides les plus couramment utilisés aux États-Unis[9]
.
L'atrazine a été interdite dans l’Union européenne[10],[11].
La Commission Européenne justifie le retrait des herbicides à base d'atrazine par le motif suivant, précisé dans la décision 2004/248/CE du 10 mars 2004 : « Il ressort des évaluations effectuées que les informations fournies ne sont pas suffisantes pour démontrer que, dans les conditions d'utilisation envisagées, les produits phytopharmaceutiques contenant de l'atrazine satisfont d'une manière générale aux exigences fixées à l'article 5, paragraphe 1, points a) et b), de la directive 91/414/CEE. En particulier, les données disponibles en matière de contrôle étaient insuffisantes pour démontrer que sur de grandes superficies, les concentrations de la substance active et de ses produits de décomposition ne seront pas supérieures à 0,1 μg/l dans les eaux souterraines. En outre, il ne peut être garanti qu'une utilisation continue sur d'autres superficies permettra une reconstitution satisfaisante de la qualité des eaux souterraines où les concentrations sont déjà supérieures à 0,1 μg/l dans les eaux souterraines. Ces niveaux de la substance active sont supérieurs aux limites fixées à l'annexe VI de la directive 91/414/CEE et auraient une incidence inacceptable sur les eaux souterraines. Il n'y a donc pas lieu d'inclure l'atrazine à l'annexe I de la directive 91/414/CEE ».
Des herbicides contenant une substance active proche de l'atrazine, la terbuthylazine, sont actuellement utilisés dans plusieurs États membres de l'Union européenne. En revanche, ces herbicides sont interdits en France par l'avis du 26 septembre 2003 en raison du risque cancérogène pour l'opérateur, selon l'avis du 19 janvier 2003 de la Commission d'étude de la toxicité des produits antiparasitaires à usage agricole. Ils sont employés dans environ 80 pays répartis dans le monde entier[12].
L'atrazine est l'un des herbicides les plus largement diffusé aux États-Unis, avec 76 millions de livres répandues chaque année[13]. C'est probablement l’herbicide le plus répandu dans le monde.
Il a été démontré dans certaines expériences par le biologiste Tyrone Hayes de l’Université de Berkeley que l'atrazine était une substance tératogène, et que, même à des concentrations très faibles de l’ordre de 0,1 partie par milliard, elle pouvait féminiser les grenouilles mâles en induisant la production d’œufs par leurs gonades, ce qui transformait effectivement les mâles en hermaphrodites[14]. Hayes a également constaté que l'atrazine pouvait faire baisser le taux de testostérone des grenouilles mâles à des niveaux inférieurs à celui des femelles[12]. L’Agence de Protection de l’Environnement (EPA) et son Comité scientifique consultatif indépendant (SAP) a examiné toutes les études disponibles sur ce sujet - y compris les travaux de Hayes - et a conclu qu'il existe « des données actuellement insuffisantes » pour déterminer si l'atrazine affecte le développement des amphibiens. Hayes, qui faisait initialement partie du groupe SAP, en a démissionné en 2000 pour poursuivre ses études de façon autonome[15].
En 2003, l'EPA a classé l'herbicide comme « probablement non cancérogène » chez l'homme, affirmant qu'il n'avait « aucun résultat parmi les études disponibles qui nous conduirait à conclure qu'un risque potentiel[16] de cancer est probable suite à l'exposition à l'atrazine »[17]. Après 10 ans de revue critique de la science, l'EPA a recommandé d’homologuer à nouveau l'atrazine en octobre 2003[18].
L'EPA a réexaminé pour l’enregistrement final en 2006, les risques d’effets cumulatifs pour les herbicides du groupe des triazines, dont l'atrazine fait partie, et a conclu que ces herbicides ne suscitaient « aucune inquiétude pour les dommages qui résulteraient de son usage pour la population générale américaine, les nourrissons, les enfants ou ... les autres consommateurs ».
Il semble qu'en Europe, les firmes phytosanitaires n'aient pas cherché à fournir des études complémentaires approfondies sur les aspects toxocologiques et écotoxicologiques de cette matière active. Par exemple la phrase de risque R40 attribuée à l'atrazine signifie que le produit est « potentiellement » cancérogène. En d'autre termes qu'il n'y a pas d'études complémentaires fournies pour dire qu'il ne l'est pas.
L'interdiction de l'atrazine, matière active tombée dans le domaine public depuis 20 ans environ, à permis de « revaloriser » le marché des herbicides destinés à la culture du maïs, son interdiction est donc profitable aux industries de la protection des cultures en obligeant les producteurs à utiliser des herbicides dont les coûts sont de 3 à 5 fois plus élevés[19].
Réglementation
Sur le plan de la réglementation des produits phytopharmaceutiques :
- pour l’Union européenne : cette substance active est interdite par la décision 2004/141/CE à la suite de l'examen relatif à l'inscription à l’annexe I de la directive 91/414/CEE.
- pour la France : cette substance active n'est pas autorisée dans la composition de préparations bénéficiant d’une autorisation de mise sur le marché.
En France, parmi les pesticides, l'atrazine est le principal polluant des eaux. Pour cette raison, les herbicides contenant de l'atrazine ont été :
- interdits à la commercialisation à partir du 30 septembre 2002,
- interdits à l'utilisation à partir du 30 juin 2003.
En effet, il était observé à la date de la décision une présence généralisée dans l'eau de traces d'atrazine et de ses produits dérivés : 40 % des prélèvements effectués en eaux de surface et 25 % des prélèvements en eaux souterraines nécessitaient la mise en place d'un traitement de l'eau.
Par ailleurs, l'AFSSA a confirmé l'absence de risques cancérigènes avérés, mais elle recommande de ne plus consommer l'eau lorsque la présence d'atrazine et de ses dérivés dépassent des valeurs-seuils situées à respectivement 0,4 microgrammes (µg/l) pour les nourrissons, 0,6 μg·l-1 pour les enfants et 2 μg·l-1 pour les adultes. Or, les réseaux de mesures observaient que ces niveaux étaient atteints dans un nombre croissant de cas.
Enfin, il était observé une efficacité de moins en moins avérée de l'atrazine et de ses dérivés, liée non seulement à la réduction des dosages autorisés mais aussi à l'apparition de phénomènes de résistances de certaines mauvaises herbes à cette famille de pesticides.
Introduite en France en 1962, l'atrazine était simple d’utilisation et peu coûteuse. Étant l'un des herbicides les moins chers du marché, elle était massivement utilisée pour la culture du maïs, ce qui a favorisé l'ampleur de la pollution de l'eau. Consécutivement à la chute de son prix de vente, les multinationales de la chimie ont préféré développer de nouvelles molécules plutôt que d'investir dans des études très coûteuse pour défendre un vieux produit devenu sans intérêt économique. De cette façon, le marché du désherbage du maïs s'est vu considérablement revalorisé.
Partie expérimentale
Il existe plusieurs techniques pour surveiller la présence d’atrazine, le diéthylatrazine et le déisopropylatrazine dans l'eau: il y a entre autres la chromatographie en phase gazeuse (CG) couplée à divers systèmes de détection, notamment l'ionisation de flamme, la capture d'électrons, la spectrométrie de masse (SM) et des détecteurs spécifiques azote-phosphore. La GC/MS[20] est utilisé par le CEAEQ (Centre Analyse Environnemental Du Québec) où l'échantillon est extrait dans un extracteur liquide-solide ;élué au dichlorométhane et concentré par évaporation ;ensuite analysé au moyen d'un spectromètre de masse muni d'un piège ionique et le seuil de détection (s.d.) est 0,1 μg·l-1] . Dans le cas du détecteur spécifique azote phosphore (méthode 507 de l'EPA des É.-U.) ; ici l'échantillon est extrait au dichlorométhane, séché, concentré avec de l'oxyde de méthyle et de butyle tertiaire ensuite analysé grâce au détecteur azote-phosphore, tandis que le seuil de détection (s.d.) est de 0,13 μg·l-1].Pour ces méthodes, le seuil de quantification moyen serait environ de 0,2 à 1,3 μg·l-1. Dans le cas de la détection par capture d'électrons (méthode 505 de l'EPA des É.-U.). L’extraction se fait à l'hexane ; le seuil de détection de 2,4 μg·l-1, il est trop élevé pour la surveillance environnementale.
Synonymes
2-chloro-4-(2-propylamino)-6-ethylamino-s-triazine, 2-chloro-4-ethylamino-6-isopropylamino-1,3,5-triazine,2-chloro-4-ethylamino-6-isopropylamino-s-triazine, 2-Chloro-4-(isopropylamino)-6-ethylamino-s-triazine, Ortho St. Augustine Weed and Feed, 6-chloro-N-ethyl-N'-isopropyl-1,3,5-triazine-2,4-diamine, A 361, aatrex, AAtrex 4L, AAtrex 80W, aatrex nine-o, actinite pk, akticon, aktikon, aktikon pk, aktinit a, aktinit pk, argezin, atazinax, Atranex, atrasine, atrataf, Atratol, atratol a, Atrazine, Atrazine 4L, Atrazine 80W, Atrazine, Atrazines, ATRAZINE (PRIMATOL), Atred, Atrex, Attrex, ATZ, Azinotox 500, Candex, cekuzina-t, chromozin, Crisamina, crisatrina, crisazine, Crisazina, Cyazine, Extrazine II, farmco atrazine, fenamine, Fenatrol, Fogard, g 30027, geigy 30,027, gesaprim, gesaprim 50, gesaprim 500, gesoprim, Griffex, Griffex 4L, hungazin, hungazin pk, inakor, Laddock, maizina, Mebazine, oleogesaprim, oleogesaprim 200, pitezin, primatol, Primatol A, primaze, radizine, Radazine, Scotts Bonus Type S, strazine, triazine a 1294, Vectal, Vectal SC, Vectral SC, Weedex, weedex a, Wonuk, zeaphos, zeapos, zeazin.
Voir aussi
- Substance active d'un produit phytopharmaceutique
- Liste de substances actives de produits phytosanitaires
- Liste de substances actives de produits phytopharmaceutiques autorisées par l'Union Européenne
- Liste de substances actives de produits phytopharmaceutiques interdites par l'Union Européenne
Références
- ATRAZINE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme » sur http://monographs.iarc.fr, CIRC, 16 janvier 2009. Consulté le 22 août 2009
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- Relations entre les coefficients d'adsorption de l'atrazine et les caractéristiques physico-chimiques et colorimétriques de la phase organique de différents sols (Mémoire de maîtrise en sols et environnement de l'Université Laval, Dpt. des sols et de génie agroalimentaire, Faculté des Sciences de l'Agriculture, l'Alimentation et de la Consommation, Décembre 2006, par Kathleen Béland (Télécharger le mémoire)
- * Ralebitso TK, Senior E, van Verseveld HW. (2002). Microbial aspects of atrazine degradation in natural environments. Biodegradation. 13:11-19. Abstract
- Cai B, Han Y, Liu B, Ren Y, Jiang S. (2003). Isolation and characterization of an atrazine-degrading bacterium from industrial wastewater in China. Letters in Applied Microbiology.36:272-276. Abstract
- « Effects of atrazine and iridovirus infection on survival and life-history traits of the long-toed salamander (Ambystoma macrodactylum) », 2006, Forson D. Environ Toxicol Chem. 25(1) pp168-73. (Télécharger)
- USGS Pesticide Use Maps
- Lee, Jennifer : Popular pesticide faulted for frogs' sexual abnormalities, New York Times (2003-06-19), pp. 20.
- EU ban on spray 'wrecks' crop trial, Financial Times (2003-10-13), pp. 25.
- Briggs H. (April 15, 2002), Pesticide 'causes frogs to change sex'. BBC News. Retrieved on 2007-10-16
- Walsh, Edward : EPA Stops Short of Banning Herbicide, Washington Post (2003-02-01), pp. A14.
- Hayes T, Haston K, Tsui M, Hoang A, Haeffele C, and Vonk A, « Atrazine-Induced Hermaphroditism at 0.1 ppb in American Leopard Frogs », dans Environmental Health Perspectives, vol. 111, 2003
- Weedkiller 'threatens frogs', BBC News
- Rappelons qu’un risque ne peut être potentiel : ou il existe, ou il n’existe pas
- EPA Interim Reregistration Eligibility Decision (IRED), January 2003
- Revised EPA Interim Reregistration Eligibility Decision (IRED), October 2003
- Triazine Cumulative Risk Assessment and Atrazine, Simazine, and Propazine Decisions, June 22, 2006, EPA.
- Centre Analyse Environnemental Du Québec, 2000a, eaux - Détermination des pesticides organochloré, triazine, carbamate, urée substituée, phtalimide et pyréthrinoide; extraction in situ avec dichlorométhane : chromatographie en phase gazeuse couplé au spectromètre de masse;M.A 403-pest. 4.0. Ministère de l’environnement du Québec ; 31p
Autres lectures
- Environ Health Perspect. 2007 May;115(5):720-7. Epub 2007 Feb 5. PMID 17520059
Liens externes
- (fr)Fiche INERIS
- (fr)Dossier Atrazine
- (fr)Fiche Télétox
- (fr)Fiche internationale de toxicologie
- (fr)Fiche Institut National de Santé Publique Québec
- Portail de la chimie
- Portail de l’agriculture et l’agronomie
Wikimedia Foundation. 2010.
