- Azote
-
 Cet article concerne l'élément chimique. Pour le gaz N2, voir diazote.
Cet article concerne l'élément chimique. Pour le gaz N2, voir diazote.Azote Carbone ← Azote → Oxygène —
7N ↑ N ↓ P Table complète • Table étendue Informations générales Nom, symbole, numéro Azote, N, 7 Série chimique Non-métaux Groupe, période, bloc 15 (VA), 2, p Masse volumique 1,2506 g·l-1 [1] Couleur Incolore No CAS (atome)
(molécule)No EINECS Propriétés atomiques Masse atomique 14,0067 ± 0,0002 u[1] Rayon atomique (calc) 65 pm (56 pm) Rayon de covalence 0,71 ± 0,01 Å [2] Rayon de van der Waals 150 pm [3] Configuration électronique [He] 2s2 2p3 Électrons par niveau d’énergie 2, 5 État(s) d’oxydation -3, 0, +2, +3, +4, +5 Oxyde Acide fort Structure cristalline Hexagonale Propriétés physiques État ordinaire Gaz Point de fusion -210,00 °C [1] Point d’ébullition -195,798 °C [1] Énergie de fusion 0,3604 kJ·mol-1 Énergie de vaporisation 2,7928 kJ·mol-1 Température critique -146,94 °C [1] Volume molaire 13,54×10-3 m3·mol-1 Vitesse du son 334,5 m·s-1 à 20 °C Divers Électronégativité (Pauling) 3,04 Chaleur massique 1 040 J·kg-1·K-1 Conductivité thermique 0,02598 W·m-1·K-1 Énergies d’ionisation[4] 1re : 14,5341 eV 2e : 29,6013 eV 3e : 47,44924 eV 4e : 77,4735 eV 5e : 97,8902 eV 6e : 552,0718 eV 7e : 667,046 eV Isotopes les plus stables iso AN Période MD Ed PD MeV 13N {syn.} 9,965 min ε 2,22 13C 14N 99,634 % stable avec 7 neutrons 15N 0,366 % stable avec 8 neutrons 16N {syn.} 7,13 s β- 10,419 16O Unités du SI & CNTP, sauf indication contraire. L'azote est un élément chimique de la famille des pnictogènes, de symbole N (du latin nitrogenium) et de numéro atomique 7. Dans le langage courant, l'azote désigne le gaz diatomique diazote N2, constituant majoritaire de l'atmosphère terrestre, représentant presque les 4/5e de l'air (78,06 %, en volume).
L'azote est le 34e élément constituant la croûte terrestre par ordre d'importance.
Les « minéraux » contenant de l'azote sont essentiellement les nitrates : nitrate de potassium KNO3 (constituant du salpêtre) ou « nitre » qui servait autrefois à faire des poudres explosives ; nitrate de sodium NaNO3 (constituant du salpêtre du Chili).
Sommaire
Histoire
Nomenclature et origine
Antoine Lavoisier a choisi le nom azote, composé de a- (privatif) et du radical grec ζωτ-, « vivant » et signifie donc « privé de vie », du fait que contrairement à l'oxygène, il n'entretient pas la vie des animaux.
L'origine du symbole N est son nom latin « nitrogenium » provient du grec nitron gennan, ce qui signifie « formateur de salpêtre » (nitrate de potassium). Le terme anglais nitrogen a conservé cette racine pour désigner l'azote.
Chronologie
Bien que des composés contenant l'élément chimique azote furent connus depuis l'antiquité, (par exemple le salpêtre, c'est-à-dire les nitrates de sodium et de potassium, le diazote n'a été isolé par Daniel Rutherford qu'en 1772, et indépendamment par C. W. Scheele et H. Cavendish.
Le protoxyde d'azote N2O a été préparé par J. Priestley également en 1772.
L'ammoniac NH3 a été préparé en 1774, également par J. Priestley.
Le premier composé accepteur - donneur faisant intervenir l'azote, H3N.BF3 a été préparé en 1809 par Louis Joseph Gay-Lussac.
Le premier composé présentant une liaison azote - halogène, le trichlorure d'azote NCl3 a été préparé par Pierre Louis Dulong qui perdit un œil et trois doigts en étudiant les propriétés de ce corps très instable et violemment explosif.
Entités contenant l'élément chimique azote
L'élément chimique azote est présent dans des entités ne contenant que l'élément chimique N et dans les composés de l'azote.
Entités ne contenant que l'élément chimique N
Il existe plusieurs entités chimiques ne contenant que l'élément chimique azote, la molécule de diazote, l'atome, et deux ions de l'azote.
Le diazote
Le diazote N2 est la forme la plus courante d'entité ne contenant que l'élément chimique azote. La triple liaison liant les deux atomes est une des liaisons chimiques les plus fortes (avec le monoxyde de carbone CO). De ce fait, sa réactivité est faible. C'est l'espèce chimique la plus abondante de l'atmosphère. C'est là qu'il est récupéré industriellement.
Sa réactivité principale est la formation d'ammoniac
- N2 + 3H2 → 2NH3
L'atome
Il est formé à partir de diazote sous faible pression (0,1 - 2 mm Hg) en présence d'une décharge électrique. A sa formation succède pendant plusieurs minutes une pale lueur jaune. Celle-ci résulte de la désexcitation de N2* suite à la recombinaison de deux atomes N. Cette forme excitée de diazote peut être mise en évidence en présence de CO2. Il se forme alors CO et de l'oxygène atomique dans un état triplet.
Les ions de l'azote
Il existe deux ions de l'azote :
- l'ion nitrure N3- qui n'existe que dans les solides (nitrures métalliques) ou dans les complexes métalliques.
- l'ion azoture N3-, forme basique de l'acide azotique HN3 ; il se rencontre aussi à l'état de sel dans l'azoture de sodium NaN3
Composés de l'azote
L'azote forme des composés avec de nombreux autres éléments chimiques. Il est présent dans des substrats organiques et inorganiques.
Azote et hydrogène
Le principal composé comportant une des liaisons chimique N-H est l'ammoniac NH3. D'autres composés contiennent également cette liaison
- les ions ammonium NH4+
- les ions amidure NH2-
- les amines primaires RNH2 et secondaires R2NH
- l'acide azothydrique HN3
- l'hydrazine N2H4
et une grande famille de composés moins courants, les azanes et les azènes, comme le trans-diazène N2H2 et son isomère le 1,1-diazène, le triazène N3H3, le triazaneN3H5, etc.
Azote et oxygène
Les oxydes d'azote
Huit oxydes d'azote sont connus[5]; Par nombre d'oxydation (moyen) croissant :
- l'azoture de nitrosyle N4O découvert en 1993
- le protoxyde de diazote N2O, communément appelé protoxyde d'azote
- le monoxyde d'azote NO
- le trioxyde de dinitrogène N2O3
- le dioxyde d'azote NO2
- son dimère le tétraoxyde de diazote N2O4
- pentaoxyde de diazote N2O5
- le trioxyde d'azote NO3
Tous sont instables au regard de la décomposition en N2 et O2.
Les oxoanions de l'azote
Les principaux oxoanions de l'azote, stables en milieu aqueux, sont les ions nitrate NO3- et nitrite NO2-. L'ion nitrate est la base conjugée d'un acide fort, l'acide nitrique. L'ion nitrite est la base conjuguée d'un acide faible, l'acide nitreux. Ce dernier n'est pas stable et, dans l'eau, il se dismute et monoxyde d'azote (qui se réoxyde en dioxyde d'azote en présence d'air) et en ion nitrate.
Azote et halogène
Le plus stable des halogènures d'azote, NF3 ne fut préparé qu'en 1928, plus d'un siècle après le très instable trichlorure NCl3. Le tribromure d'azote NBr3, très explosif, ne fut isolé qu'en 1975. Le triiodure NI3 n'a jamais été isolé, mais son adduit I3N.NH3, solide noir hautement instable au choc et à la température, a été préparé en 1812. Des combinaisons comme modifier] Azote et métaux
De nombreux azotures métalliques existent. Plusieurs voies de synthèse sont possibles :
La réaction entre le métal et le diazote à chaud
- 3Ca + N2 → Ca3N2
La réaction entre le métal et l'ammoniac à haute température
- 3Mg + 2NH3 → Mg3N2 + 3H2
La décomposition d'amidures
- 3Zn(NH2)2 → Zn3N2 + 3NH3
Des réactions de transfert
- Al2O2 + 3C + N2 → 2AlN + 3CO
- 2ZrCl4 + 4H2 + N2 → 2ZrN + 8HCl
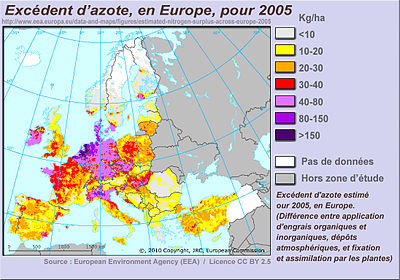 Un excédent d'azote (source d'eutrophisation de l'eau, des sols et des écosystèmes) est relevé partout en Europe (ici pour 2005, selon les données disponibles de la Commission européenne et de l'Agence européenne de l'environnement
Un excédent d'azote (source d'eutrophisation de l'eau, des sols et des écosystèmes) est relevé partout en Europe (ici pour 2005, selon les données disponibles de la Commission européenne et de l'Agence européenne de l'environnement
Exploitation et usages
Diazote
Aujourd'hui, l'azote gazeux ou diazote est généralement obtenu par liquéfaction de l'air, dont il est le principal constituant avec une concentration de 78,06 % en volume et de 75,5 % en masse. La production mondiale est d'environ 150 millions de tonnes par an.
Article détaillé : diazote.Le gaz diazote lui-même a en particulier les applications suivantes :
- Emballage de denrées alimentaires (MAP): L'inertage des aliments emballés augmente leur durée de conservation en remplaçant l'air ambiant (contenant de l'oxygène) par de l'azote (pureté de 95 à 99,5 %)[6]* gaz « neutre » utilisé pour protéger (grâce à la constitution d'une atmosphère inerte confinée) des produits, des objets ou des contenants (citernes par exemple) dans l'industrie, les musées ou autres lieux : protection contre la corrosion, des insectes, champignons... ;
- Gaz utilisé comme pesticide doux pour éliminer par asphyxie les vers du bois ou certains organismes (ex : Petite vrillette) ayant colonisé des objets anciens fragiles (cadres, sculptures et objets de bois, incunables, les parchemins, gravures, etc.) ;
- Gaz de gonflage de pneumatiques. Bien que l'air contienne déjà 78 % d'azote (de diazote pour être plus précis), certains professionnels de l'aviation ou de la formule 1, (par exemple), augmentent cette proportion et gonflent les pneumatiques avec de l'azote presque pur. Ce gaz ayant la propriété d'être inerte et stable conserve une pression plus constante même en cas d'échauffement intense du pneumatique. Une polémique existe d'ailleurs quant à l'introduction de cette méthode pour les véhicules particuliers. En effet, ceux-ci sont soumis à des contraintes bien moindres ce qui rend la différence avec l'air moins notable. Par contre le gonflage devient payant et on lui reproche souvent d'avoir un prix non justifié (le gonflage à l'air est souvent gratuit et jugé satisfaisant). Ceux qui l'utilisent devraient avoir, en principe, à rectifier le gonflage plus rarement, mais ils doivent néanmoins contrôler les pressions régulièrement.
- Gaz utile pour gonfler les accumulateurs hydrauliques en raison de sa passivité vis-à-vis des huiles.
- Construction mécanique: Beaucoup de machines de découpe modernes fonctionnent avec un rayon laser, celui-ci nécessite de l'azote comme gaz moteur ou comme gaz d'inertage[6].
- Agent de lutte contre les incendies : allié à 50 % d'argon et parfois avec du dioxyde de carbone, il est présent dans certaines installations d'extinction automatique à gaz protégeant des salles informatiques ou des stockages particuliers ne devant pas être endommagés par de la poudre ou de l'eau. Conservé dans des bonbonnes métalliques sous une pression d'environ 200 bars, il est libéré dans un local où un début d'incendie a été détecté. Le volume de diazote injecté remplace une partie de l'atmosphère de la pièce et entraine une chute du taux d'oxygène dans l'air. Le niveau généralement retenu de 15 % de comburant interrompt le phénomène de combustion sans effet létal sur la respiration humaine.
- Azote liquide : agent réfrigérant.
- Métallurgie : l'azote est régulièrement injecté dans des fours de production de métaux hautement oxydables (p.ex. l'aluminium et ses alliages) pour en empêcher la réaction avec l'oxygène de l'air. Il est également utilisé pour éviter la corrosion lors de brasures (p.ex. brasure du Cuivre)[6].
Le diazote, contrairement aux gaz inhibiteurs chimiques halogénés et aux CFC ne présente a priori aucun effet nocif pour l'environnement (pas d'impact sur l'effet de serre, ni sur la couche d'ozone). Mais il requiert des réservoirs volumineux, des canalisations adaptées et des mesures constructives pour faire face à la détente brutale d'un équivalent de 40 à 50 % du volume protégé.
Danger du gaz diazote : l'utilisation de diazote pour créer des atmosphères confinées inertes est à l'origine de plusieurs morts par asphyxie, lorsqu'une personne pénètre sans s'en rendre compte dans une enceinte inertée ; il est nécessaire de vérifier la présence d'une proportion suffisante d'oxygène dans de tels espaces confinés avant d'y pénétrer, ou de s'équiper d'un appareil respiratoire autonome.
En plongée, l'azote contenu dans l'air respiré sous pression est à l'origine du phénomène de la narcose. La pression partielle d'azote devient en effet "toxique" pour l'organisme à partir de PpN2= 3,6 bars et la narcose est réelle à PpN2=4,6 Bars (soit une plongée à environ 50 m de profondeur). C'est aussi l'élément principal dictant la durée des paliers de décompression.
Article connexe : Azote liquide.Usage des composés de l'azote
Article détaillé : cycle de l'Azote.Paradoxalement, et malgré son nom, l'élément chimique « azote » est (avec le carbone, l'oxygène et l'hydrogène) un des composants principaux du Vivant et des écosystèmes ainsi que des agrosystèmes. Il entre dans la composition des protéines (pour environ 15 %). L'azote est présent dans de très nombreux produits chimiques, dont certains pesticides dits à (« urées substituées »).
L'azote a été exploité et l'est encore en tant qu'engrais naturel dans l'urée animale (ou humaine) et le guano (excréments sec d'oiseau ou de chauve-souris), notamment au Chili, au Pérou, en Inde, en Bolivie, en Espagne, en Italie et en Russie. La nitre (nitrate naturel minéral) était autrefois récoltée pour produire la poudre à canon.
Aujourd'hui, ses composés sont essentiellement produits industriellement par synthèse chimique pour de nombreux usages, dont par exemple :
- fertilisants agricoles (engrais) ; les sels d'ammonium sont absorbés par les plantes, qui sont alors forcées d'absorber plus d'eau (équilibre osmotique). Ces sels forcent ainsi la plante à grossir. Si d'autres minéraux sont présents en suffisance (phosphore, potassium en particulier) cet azote dope la croissance des plantes cultivées. De l'azote est pour cette raison utilisé sous forme de nitrate d'ammonium, NH4NO3, de sulfate d'ammonium, (NH4)2SO4, de monophosphate d'ammonium, NH4H2PO4, ou d'urée, CO(NH2)2. C'est aujourd'hui le principal usage de l'azote dans le monde, qui est également responsable d'une pollution généralisée (eutrophisation, dystrophisation) de l'environnement (eaux de nappes, estuaires, certains littoraux, avec l'apparition de vaste zones mortes dans les océans jugées très préoccupantes par l'ONU).
- produits pharmaceutiques :
- certains composés organiques nitrés, telle la nitroglycérine, sont utilisés pour soigner certaines affections cardiovasculaires ;
- le protoxyde d'azote (gaz hilarant) est utilisé comme anesthésiant ;
- l'ammoniac NH3, utilisé comme matière première de production de polymères, d'explosifs, d'engrais, ou comme fluide réfrigérant dans certains installations industrielles ;
- combustibles (l'hydrazine et autres dérivés comme combustibles de fusée) ;
- explosifs (composés chimiques organiques qui possèdent plusieurs groupes -ONO2 ou -NO2 : dynamite) ;
- gaz propulseurs pour bombes aérosols (N2O) ou aérographes ;
- conservateur (nitrite de sodium, NaNO2, sous le numéro E E250) ;
- azoture de sodium, utilisé pour gonfler instantanément les coussins gonflables de sécurité (d'une automobile par exemple) en cas de choc.
Notes et références
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, 2009, 90e éd., Relié, 2804 p. (ISBN 978-1-420-09084-0)
- (en) Beatriz Cordero, Verónica Gómez, Ana E. Platero-Prats, Marc Revés, Jorge Echeverría, Eduard Cremades, Flavia Barragán et Santiago Alvarez, « Covalent radii revisited », dans Dalton Transactions, 2008, p. 2832 - 2838 [lien DOI]
- Paul Arnaud, Brigitte Jamart, Jacques Bodiguel, Nicolas Brosse, Chimie Organique 1er cycle/Licence, PCEM, Pharmacie , Cours, QCM et applications, Dunod, 8 juillet 2004, Broché, 710 p. (ISBN 2100070355)
- "Ionization Energies of Atoms and Atomic Ions," in CRC Handbook of Chemistry and Physics, 91st Edition (Internet Version 2011), W. M. Haynes, ed., CRC Press/Taylor and Francis, Boca Raton, FL., p. 10-203
- Greenwood N. & Earnwhaw A. (2003). Chemistry of the elements, 2nde Ed. Elsevier, p.443.
- www.technofluid.be
Voir aussi
Article connexe
Liens externes
- (en) Portail d’un groupe de travail international sur la pollution azotée (ONU), cadré par le Global Programme of Action for the Protection of the Marine Environment from Land-Based Activities (ONU / PNUED)
s1 s2 g f1 f2 f3 f4 f5 f6 f7 f8 f9 f10 f11 f12 f13 f14 d1 d2 d3 d4 d5 d6 d7 d8 d9 d10 p1 p2 p3 p4 p5 p6 1 H He 2 Li Be B C N O F Ne 3 Na Mg Al Si P S Cl Ar 4 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 5 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 6 Cs Ba La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 7 Fr Ra Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr Rf Db Sg Bh Hs Mt Ds Rg Cn Uut Uuq Uup Uuh Uus Uuo 8 Uue Ubn * Ute Uqn Uqu Uqb Uqt Uqq Uqp Uqh Uqs Uqo Uqe Upn Upu Upb Upt Upq Upp Uph Ups Upo Upe Uhn Uhu Uhb Uht Uhq Uhp Uhh Uhs Uho ↓ g1 g2 g3 g4 g5 g6 g7 g8 g9 g10 g11 g12 g13 g14 g15 g16 g17 g18 * Ubu Ubb Ubt Ubq Ubp Ubh Ubs Ubo Ube Utn Utu Utb Utt Utq Utp Uth Uts Uto Métalloïdes Non-métaux Halogènes Gaz rares Métaux alcalins Métaux alcalino-terreux Métaux de transition Métaux pauvres Lanthanides Actinides Superactinides Éléments non classés Catégories :- Élément chimique
- Non-métal
- Gaz
- Réfrigérant
- Pnictogène
- Métabolisme de l'azote
- Théorie de la plongée
Wikimedia Foundation. 2010.

