- Actinide
-
La série chimique des actinides comprend les éléments chimiques du tableau périodique se situant entre l'actinium et le lawrencium, possédant donc un numéro atomique entre 89 et 103 inclus.
Les actinides sont tous des éléments radioactifs et tirent leur nom de l'actinium (Z=89), un métal lourd, car ils possèdent des propriétés chimiques voisines. L'uranium et le thorium, qui sont relativement abondants à l'état naturel du fait de la très longue demi-vie de leurs isotopes les plus stables, sont des actinides. Les actinides comprennent des éléments artificiels, les transuraniens, plus lourds que l'uranium : ils sont générés par des captures de neutrons qui n'ont pas été suivies de fissions.
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 1 H He 2 Li Be B C N O F Ne 3 Na Mg Al Si P S Cl Ar 4 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 5 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 6 Cs Ba * Lu Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 7 Fr Ra * Lr Rf Db Sg Bh Hs Mt Ds Rg Cn Uut Uuq Uup Uuh Uus Uuo ↓ * La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb * Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No 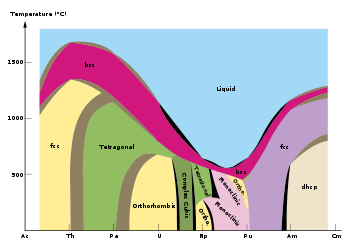 Structures cristallines des actinides, montrant la complexité du plutonium.
Structures cristallines des actinides, montrant la complexité du plutonium.
Sommaire
Plutonium et actinides mineurs
L'actinide produit le plus abondamment est le plutonium, avec en tête son principal isotope le plutonium-239, lui-même fissile. Mais les réacteurs nucléaires génèrent, en quantité moindre, d'autres actinides qui sont appelés « mineurs » pour cette raison. Les principaux sont le neptunium 237, les américium 241 et 243 et les curium 244 et 245. Les actinides mineurs constituent avec les produits de fission une grande partie des déchets radioactifs à haute activité et à vie longue (HAVL), c’est-à-dire les déchets de l'industrie électronucléaire les plus fortement radioactifs. Le plutonium-239 n'est pas considéré comme un déchet radioactif car il est fissible.
Ils possèdent des caractéristiques chimiques semblables à celles des lanthanides, lorsqu'ils sont au même degré d'oxydation. Contrairement aux lanthanides, les actinides légers peuvent être stables aux degrés d'oxydation +5 (Pa, U, Np, Pu, Am) et +6 (U, Np, Pu, Am). Cette plus grande facilité d'ionisation (des actinides par rapport aux lanthanides) s'explique par le fait que les orbitales de valence 5f des actinides, sont moins internes que les 4f des lanthanides, car plus écrantées par les électrons de cœur. Les actinides au même degré d'oxydation sont analogues chimiques entre eux, à l'exception notable de Pa(V).
Les isotopes des éléments transuraniens ont souvent une demi-vie très courte, aux exceptions notables, de quelques isotopes de Np, Pu, Am et Cm produits en quantités pondérables dans les réacteurs nucléaires.
Dans le tableau périodique, les actinides sont placés sous les lanthanides, ces deux séries étant généralement sous la partie principale du tableau, à la manière d'une note de bas de page.
Actinides mineurs (AMin)
Lors de l'irradiation en réacteur, les atomes d'uranium (notamment l'isotope 238) du combustible peuvent capturer un neutron sans subir de fission. Ces captures, souvent suivies de décroissance radioactive béta, conduisent à une augmentation du numéro atomique (du nombre de nucléons contenus dans le noyau). Autrement dit ce sont les noyaux lourds (isotopes) formés dans les réacteurs par capture successive de neutrons par les noyaux du combustible.
Il se forme alors des transuraniens : du plutonium et des actinides mineurs : principalement le neptunium (237), l’américium (241, 243) et le curium (243, 244, 245).
La qualification de « mineurs » rend compte du fait que ces éléments sont présents en bien moins grandes proportions que les actinides majeurs : uranium et plutonium.Les actinides mineurs à vie moyenne
Ils constituent environ 35 % du total des actinides mineurs formés :
- L’américium 241 (période 458 ans) pour environ 32 % du total des AMin formés,
- Le curium 244 (période 17,6 ans) pour environ 3,1 % du total des AMin formés,
- L’américium 242 métastable (période 152 ans) pour environ 0,1 % du total des AMin formés.
Ces éléments contribuent fortement au dégagement thermique du combustible irradié. Ils sont radioactifs alpha et émettent donc de l'hélium.
Les actinides mineurs à vie longue
Ils constituent environ 65 % du total qui sont les suivants :
- Le neptunium 237 émetteur alpha de période 2,14 millions d’années pour environ 50 % du total des AMin formés
- L’américium 243 émetteur alpha de période 7 370 ans pour environ 14,5 % du total des AMin formés,
- Le curium 245 émetteur alpha de période 9 300 ans pour environ 0,17 % du total des AMin formés,
- Le curium 246 émetteur alpha de période 5 500 ans pour environ 0,03 % du total des AMin formés.
Risques et dangers liés aux actinides mineurs (AMin)
De façon générale, ils représentent les déchets radioactifs qui posent les principaux problèmes, dont au niveau du Stockage des déchets radioactifs en couche géologique profonde pour les raisons suivantes :
- en tant qu'émetteurs alpha, ils présentent une forte toxicité si l'élément entre dans la chaîne alimentaire (inhalé, injecté ou ingéré) ;
- ils dégagent une forte chaleur ; la plupart des émissions alpha des actinides le sont à une énergie élevée de l'ordre de 5,5 MeV ;
- ils dégagent de l'hélium, qui est suspecté de pouvoir dégrader la cohésion du verre de conditionnement des déchets.
Couleur et magnétisme
couleurs approximatives d'actinides (ions en solution aqueuse)[1],[2] État d'oxydation 89 90 91 92 93 94 95 96 97 98 99 +3 Ac3+ Th3+ Pa3+ U3+ Np3+ Pu3+ Am3+ Cm3+ Bk3+ Cf3+ Es3+ +4 Th4+ Pa4+ U4+ Np4+ Pu4+ Am4+ Cm4+ Bk4+ Cf4+ +5 PaO2+ UO2+ NpO2+ PuO2+ AmO2+ +6 UO22+ NpO22+ PuO22+ AmO22+ +7 NpO23+ PuO23+ [AmO6]5- Les couleurs des actinides (sous forme ionique) dans les états d'oxydation inférieurs sont dues aux transitions f-f. Dans les états d'oxydation élevée, il peut aussi y avoir des transitions charge-transfer. Il y a une interaction spin-orbite forte, mais leurs caractéristiques cristallines font qu'il existe de petites variations de couleur pour les composés d'un élément donné dans un état d'oxydation donné. Les transitions entre orbites 5f et 6d peuvent être observées dans région ultraviolette du spectre. Les moments magnétiques des espèces paramagnétiques sont loin d'être seulement des valeurs de spin.
Voir aussi
Articles connexes
Bibliographie
- {...}
Liens externes
- UICPA : Page de liens vers le tableau périodique
- UICPA : Tableau périodique officiel du 22/06/2007
Notes et références
- Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie, 102. Auflage, de Gruyter, Berlin 2007, S. 1956; ISBN 978-3-11-017770-1.
- dtv-Atlas zur Chemie 1981, Teil 1, S. 224.
s1 s2 g f1 f2 f3 f4 f5 f6 f7 f8 f9 f10 f11 f12 f13 f14 d1 d2 d3 d4 d5 d6 d7 d8 d9 d10 p1 p2 p3 p4 p5 p6 1 H He 2 Li Be B C N O F Ne 3 Na Mg Al Si P S Cl Ar 4 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 5 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 6 Cs Ba La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 7 Fr Ra Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr Rf Db Sg Bh Hs Mt Ds Rg Cn Uut Uuq Uup Uuh Uus Uuo 8 Uue Ubn * Ute Uqn Uqu Uqb Uqt Uqq Uqp Uqh Uqs Uqo Uqe Upn Upu Upb Upt Upq Upp Uph Ups Upo Upe Uhn Uhu Uhb Uht Uhq Uhp Uhh Uhs Uho ↓ g1 g2 g3 g4 g5 g6 g7 g8 g9 g10 g11 g12 g13 g14 g15 g16 g17 g18 * Ubu Ubb Ubt Ubq Ubp Ubh Ubs Ubo Ube Utn Utu Utb Utt Utq Utp Uth Uts Uto Métalloïdes Non-métaux Halogènes Gaz rares Métaux alcalins Métaux alcalino-terreux Métaux de transition Métaux pauvres Lanthanides Actinides Superactinides Éléments non classés
Wikimedia Foundation. 2010.
