- Version etendue du tableau periodique des elements
-
Version étendue du tableau périodique des éléments
 Pour les articles homonymes, voir Tableau.
Pour les articles homonymes, voir Tableau.Cette version étendue du tableau périodique des éléments représente tous les éléments chimiques, groupés par leur orbitale atomique et leur couche électronique.
Sommaire
Histoire
Cette version étendue du tableau périodique des éléments a été mise au point par Glenn T. Seaborg en 1969. C'est une extension logique des principes édictés par Mendeleïev dans sa classification périodique des éléments permettant ainsi d'inclure les éléments chimiques encore non découverts à ce jour. L'ensemble des éléments chimiques encore non découverts est nommé d'après la dénomination systématique définie par la nomenclature de l'UICPA (Union internationale de chimie pure et appliquée). Cette nomenclature permet de créer la dénomination d'un élément avant sa découverte, sa confirmation et l'obtention de son nom officiel.
Le symbole en bleu situé en haut de chaque colonne indique la dernière orbitale atomique. Le chiffre en rouge situé à la gauche de chaque ligne indique la période de la dernière couche électronique (Notez qu'il y a quelques exceptions, telles que le cuivre).
L'hélium est placé à coté de l'hydrogène plutôt qu'au dessus du néon puisqu'il fait partie du groupe s² et non du groupe p6.
Tableau périodique étendu
Tableau périodique (Étendu) Periode s1 s2 1 1
2
p1 p2 p3 p4 p5 p6 2 3
4
5
6
7
8
9
10
3 11
12
d1 d2 d3 d4 d5 d6 d7 d8 d9 d10 13
14
15
16
17
18
4 19
20
21
22
23
24
25
26
27
28
29
30
31
32
33
34
35
36
5 37
38
f1 f2 f3 f4 f5 f6 f7 f8 f9 f10 f11 f12 f13 f14 39
40
41
42
43
44
45
46
47
48
49
50
51
52
53
54
6 55
56
57
58
59
60
61
62
63
64
65
66
67
68
69
70
71
72
73
74
75
76
77
78
79
80
81
82
83
84
85
86
7 87
88
g1 g² g³ g4 g5 g6 g7 g8 g9 g10 g11 g12 g13 g14 g15 g16 g17 g18 89
90
91
92
93
94
95
96
97
98
99
100
101
102
103
104
105
106
107
108
109
110
111
112
113
114
115
116
117
118
8 119
120
121
122
123
124
125
Ubp
126
127
128
129
130
Utn
131
Utu
132
Utb
133
Utt
134
Utq
135
Utp
136
137
138
139
140
141
Uqu
142
Uqb
143
Uqt
144
Uqq
145
Uqp
146
Uqh
147
Uqs
148
Uqo
149
Uqe
150
Upn
151
Upu
152
Upb
153
Upt
154
Upq
155
Upp
156
Uph
157
Ups
158
Upo
159
Upe
160
Uhn
161
Uhu
162
Uhb
163
Uht
164
Uhq
165
Uhp
166
Uhh
167
Uhs
168
Uho
9 169
Uhe
170
Usn
171
Usu
172
Usb
173
Ust
174
Usq
175
Usp
176
Ush
177
Uss
178
Uso
179
Use
180
Uon
181
Uou
182
Uob
183
Uot
184
Uoq
185
Uop
186
Uoh
187
Uos
188
Uoo
189
Uoe
190
Uen
191
Ueu
192
Ueb
193
Uet
194
Ueq
195
Uep
196
Ueh
197
Ues
198
Ueo
199
Uee
200
Bnn
201
Bnu
202
Bnb
203
Bnt
204
Bnq
205
Bnp
206
Bnh
207
Bns
208
Bno
209
Bne
210
Bun
211
Buu
212
Bub
213
But
214
Buq
215
Bup
216
Buh
217
218
Groupes Groupe S Groupe P Groupe D Groupe F Groupe G Tableau de Mendeleïev corrigé
Ce tableau[1] ne présente que les éléments connus ; des éléments non encore observés sont représentés par leur numéro atomique.
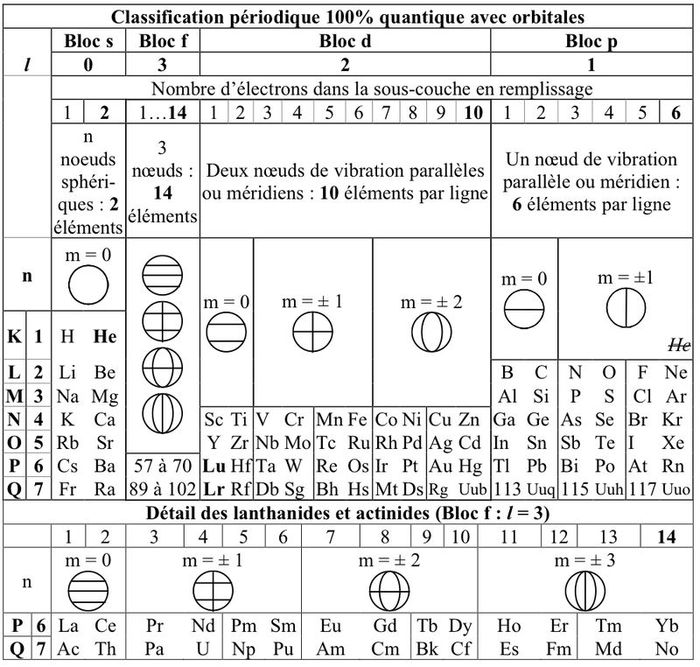
Il tient compte de ce que, comme montré ci-dessus, l'hélium (bloc s) doit être à côté de l'hydrogène et pas avec les autres gaz rares (bloc p) qui ont 6 électrons dans leur couche externe alors que l'hélium n'en a que deux. Les lanthanides et actinides (bloc f) sont bien 14, conformément au principe de Pauli et non 15 comme dans la représentation officielle qui est conforme à 97% avec la mécanique quantique. Les trois éléments non conformes sont donc He (2-Hélium), Lu (71-Lutécium) et Lr (103-Lawrencium) que les chimistes veulent continuer à classer selon les propriétés chimiques. Cependant il faut se rappeler que Mendeleïev avait classé les éléments selon la masse, qui est une propriété physique et non chimique. Plus tard, Moseley a remplacé la masse par le numéro atomique comme critère de classement grâce aux rayons X. Ce qui n'est pas non plus un critère chimique. Les actinides, découverts par Seaborg se caractérisent plus par leur propriété physique commune, la radioactivité, que par leurs propriétés chimiques. Pour les lanthanides, c'est moins clair.
Les dessins indiquent les orbitales des couches externes ou, plus précisément les harmoniques sphériques correspondantes.
Références
Voir aussi
Articles connexes
- Élément chimique
- Tableau périodique des éléments
- Table des isotopes
- Atome d'hydrogène
- Atome à N électrons
- Classification périodique
Liens externes
- (fr) Carrefour atomique Historique du tableau périodique
- (en) Apsidium If you want to know more about the structure of atoms
- Portail de la chimie
Catégories : Classification chimique | Atome
Wikimedia Foundation. 2010.