- Hydrocarbure aromatique polycyclique
-
 Pour les articles homonymes, voir HAP.
Pour les articles homonymes, voir HAP. Une illustration d'hydrocarbures aromatiques polycycliques. Dans le sens des aiguilles en partant d'en haut à gauche : benz[e]acéphénanthrylène, pyrène et dibenz[a, h]anthracène.
Une illustration d'hydrocarbures aromatiques polycycliques. Dans le sens des aiguilles en partant d'en haut à gauche : benz[e]acéphénanthrylène, pyrène et dibenz[a, h]anthracène.
 Structure cristalline d'un dérivé hexa-t-butyle de l'hexa-péri-hexabenzo[bc, ef, hi, kl, no, qr]coronène publiée par Müllen et al., Chem. Eur. J., 2000, 1834-1839. Les groupes t-butyles permettent à ce composé d'être soluble dans des solvants communs comme l'hexane, dans lequel le composé HAP non substitué est insoluble.
Structure cristalline d'un dérivé hexa-t-butyle de l'hexa-péri-hexabenzo[bc, ef, hi, kl, no, qr]coronène publiée par Müllen et al., Chem. Eur. J., 2000, 1834-1839. Les groupes t-butyles permettent à ce composé d'être soluble dans des solvants communs comme l'hexane, dans lequel le composé HAP non substitué est insoluble.
Les hydrocarbures aromatiques polycycliques (HAP) sont une sous-famille des hydrocarbures aromatiques, c'est-à-dire des molécules constitués d’atomes de carbone et d’hydrogène mais dont la structure comprend au moins deux cycles aromatiques condensés.
Depuis de nombreuses années, les HAP sont très étudiés car ce sont des composés présents dans tous les milieux environnementaux et qui montrent une forte toxicité. D’ailleurs, c’est une des raisons qui a conduit à leur ajout dans la liste des polluants prioritaires par l’agence de protection de l'environnement des États-Unis (EPA US Environmental Protection Agency), dès 1976. Aujourd’hui, ils font également partie des listes de l’OMS (Organisation mondiale de la santé) et de la communauté européenne. Bien qu'ils ne soient pas cités dans la liste déclaratoire de la Convention de Stockholm portant sur les polluants organiques persistants (POP)[1], ils sont répertoriés en tant que tels dans le protocole d'Aarhus[2].
Les HAP font par ailleurs l'objet de recherches actives chez les astrophysiciens et astrochimistes, depuis qu'Alain Leger et Jean-Lou Puget[3] les ont proposés en 1984 comme responsables de l'émission interstellaire des bandes infra-rouge entre 3 et 15µm. Bien qu'aucune molécule HAP précise n'ait à ce jour (Février 2010) été identifiée, la communauté astrophysique accepte majoritairement l'hypothèse que les HAP constituent une partie des grains de poussière interstellaire et jouent un rôle majeur dans le milieu interstellaire.
Sommaire
Généralités
Selon le nombre de cycles, ils sont classés en HAP légers (jusqu’à trois cycles) ou lourds (au-delà de trois cycles), et ont des caractéristiques physico-chimiques et toxicologiques très différentes.
Le nombre de HAP susceptibles d’être rencontrés est sans limite. En effet, non seulement il n’y a pas de limite au nombre de noyaux accolés, mais le nombre d’isomères augmente considérablement avec le nombre de cycles aromatiques. De plus, ils peuvent être alkylés.
Les HAP purs sont des substances colorées et cristallines à température ambiante. Les propriétés physiques des HAP varient selon leur masse moléculaire et leur structure. À l’exception du naphtalène, les HAP sont très hydrophobes, et donc leurs solubilités dans l’eau sont faibles. Parallèlement, leurs coefficients de partage octanol/eau (Kow) sont relativement élevés, témoignant d’un important potentiel d’adsorption sur les matières organiques particulaires en suspension dans l’air ou dans l’eau, ainsi que d’un fort potentiel de bioconcentration dans les organismes.
Principaux HAP
Composé chimique Composé chimique Anthracène 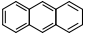
Benzo[a]pyrène 
Chrysène 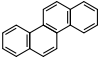
Coronène 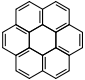
Corannulène 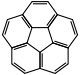
Tétracène 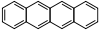
Naphtalène 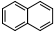
Pentacène 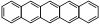
Phénanthrène 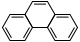
Pyrène 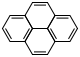
Triphénylène 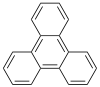
Ovalène 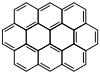
Sources des HAP
La formation des HAP peut avoir de nombreuses origines qui peuvent être regroupées en trois catégories. On peut distinguer les origines pyrolytiques, diagénétiques et pétrogéniques. Cependant, les deux dernières sont négligeables dans l’atmosphère, en comparaison des sources pyrolytiques.
HAP d'origine pyrolytique
Avant l’utilisation du charbon, du pétrole et du gaz naturel comme sources d’énergie, l’apport de HAP d’origine pyrolytique était principalement dû à des phénomènes naturels tels que les feux de forêts et de prairies. Aujourd’hui, c’est l’origine pyrolytique anthropique qui est considérée comme la source majeure de HAP dans l’environnement, notamment à cause des émissions domestiques et industrielles. Les HAP pyrolytiques sont générés par des processus de combustion incomplète de la matière organique à haute température. Les mécanismes mis en jeu lors de leur formation font intervenir la production de radicaux libres par pyrolyse à haute température (≥ 500 °C) de la matière fossile (pétroles, fioul, matières organiques…) dans des conditions déficientes en oxygène. Les HAP d’origine pyrolytique proviennent de la combustion du carburant automobile, de la combustion domestique (charbon, bois…), de la production industrielle (aciéries, alumineries…), de la production d’énergie (centrales électriques fonctionnant au pétrole ou au charbon…) ou encore des incinérateurs.
Également, une partie des HAP présents dans l’environnement provient de processus naturels tels que les éruptions volcaniques.
En fonction de l’origine, certains HAP se formeront préférentiellement. Ceci permet de les utiliser comme indicateurs d’origine. Ainsi, les rapports de concentration en différents HAP permettent de calculer des indices moléculaires. Par exemple, si le rapport de la concentration en anthracène sur celle du phénantrène est supérieur à 10, alors l’origine sera pétrogénique tandis que s'il est inférieur à 10, il sera d’origine pyrolytique.
En France, les émissions anthropiques de HAP sont dominées par le secteur domestique, du fait de la consommation énergétique (notamment le chauffage au bois, émetteur largement majoritaire de HAP dans l'atmosphère). Ensuite viennent le secteur des transports routiers, notamment des véhicules diesel, puis celui de l’industrie manufacturière.
Il est à noter que la consommation de produits grillées ou fumés fournit un apport très faible, mais à considérer, en HAP d'origine pyrolytique et en AHC (Amines Hétérocycliques)[4].
Cinétique environnementale
Les HAP sont hydrophobe ; ils ne persistent donc pas facilement dans l'eau, sauf associés à des surfactants ou adsorbés sur des particules en suspension ou dans le sédiment ; Ils sont surtout présent dans les sols où ils peuvent être stockés ou circuler (adsorption, percolation, bioturbation), mais ils peuvent contaminer l'air en phase vapeur, et être présents dans l'eau ou dans le biofilm. Ils peuvent passer d'un compartiment environnemental (eau, air, sol) à l'autre.
Concentrations atmosphériques
Dans l’atmosphère, les concentrations de HAP particulaires sont très variables. En effet, les concentrations peuvent être faibles dans les lieux reculés, comme l’Antarctique où on retrouve quelques dizaines de pg/m³, et élevées en ville, à proximité de voies routières, où les concentrations peuvent atteindre quelques centaines de ng/m³, comme à Santiago du Chili.
En milieu urbain, les taux de HAP vont de 2 à 300 ng/m³, voire plus. Ces valeurs tendent à diminuer dans les pays riches, compte tenu de l’avancée des technologies sur la limitation des émissions automobiles (réduction de la consommation, utilisation de pots catalytiques, développement des filtres à particules…).
Il existe une variabilité saisonnière, marquée par des concentrations plus importantes en hiver, surtout pour les HAP particulaires, expliquées principalement par quatre processus :
- - les variation des émissions dues au chauffage domestique ;
- - les processus de dégradation des HAP (car la photodégradation par les UV solaires se fait moins en moins en hiver, qui est le moment on se chauffe le plus) ;
- - la température plus faible qui fait que les HAP auront tendance à rester en phase particulaire ;
- - une plus grande stabilité de la colonne atmosphérique en hiver (hors moments venteux), ou phénomènes d'inversions atmosphériques limitant la dispersion.
Des variations importantes existent entre les différents lieux de prélèvements et pour les différents HAP.
En s’éloignant des sources de combustions, les concentrations en HAP diminuent très rapidement. En milieu rural, les concentrations sont très faibles. Cependant, les HAP sont présents sur toute la planète du fait du transport atmosphérique.Les sols pollués de certaines friches industrielles (carbochimie, pétrochimie en particulier) ou urbaines (anciennes stations d'essence...) peuvent contenir des taux élevés de HAP, parfois très perceptibles par l'odorat humain.
Toxicité
L’une des raisons ayant conduit au classement des HAP dans la liste des polluants prioritaires de l’EPA est le caractère toxique de certains d’entre eux. Ce sont des molécules biologiquement actives qui, une fois absorbées par les organismes, se prêtent à des réactions de transformation sous l’action d’enzymes conduisant à la formation d’époxydes et/ou de dérivés hydroxylés. Les métabolites ainsi formés peuvent avoir un effet toxique plus ou moins marqué en se liant à des molécules biologiques fondamentales telles que les protéines, l’ARN, l’ADN et provoquer des dysfonctionnements cellulaires.
Toxicité des HAP[5] HAP Toxicité Cancérogénèse Mutagenèse Rapporté dans Naphtalène Modérée Non confirmée EPA-TSCA Acénaphtène Modérée Constatée EPA-TSCA Acénaphtylène Modérée Constatée EPA-TSCA Fluorène Faible Constatée EPA-TSCA, IARC Phénanthrène Modérée Constatée EPA-TSCA, IARC Anthracène Modérée Constatée EPA-TSCA, IARC Fluoranthène Modérée Non confirmée Constatée * EPA-TSCA, IARC Pyrène Modérée Non confirmée Constatée * EPA-TSCA, IARC Benzo[a]anthracène Elevée Confirmée Constatée * EPA-TSCA, IARC Chrysène Confirmée Constatée * EPA-TSCA, IARC Benzo[b]fluoranthène Confirmée Constatée IARC Benzo[k]fluoranthène Confirmée Constatée IARC Benzo[a]pyrène Elevée Confirmée Constatée * EPA-TSCA, IARC Benzo[e]pyrène Non confirmée Constatée * IARC Indéno(1,2,3-cd)pyrène Confirmée Constatée EPA-TSCA, IARC Benzo[ghi]pérylène Non confirmée Constatée IARC Dibenzo(a, h)anthracène Elevée Confirmée Constatée * EPA-TSCA, IARC (*) Mutagène pour l’homme
IARC : Centre international de recherche sur le cancer
EPA-TSCA : Environmental Protection Agency-Toxic Substances Control Act
Benzo(a)pyrène
Le Benzo(a)pyrène (B(a)P) est un des HAP les plus toxiques. En effet, il est reconnu comme cancérogène par l’IARC (International Association for Research on Cancer). Ceci est lié à sa capacité à former des adduits avec l’ADN. Il existe plusieurs voies d’activation du B(a)P, mais la plus importante est celle des diols époxydes car elle conduit à la formation d’adduits stables. Le B(a)P va être oxydé par les systèmes enzymatiques du cytochrome P450, pour finalement former un époxyde. Ce dernier produit, le Benzo(a)Pyrène-7,8-dihydrodiol-9,10-époxyde (BPDE), est susceptible de réagir avec l’ADN. Ainsi, la toxicité du benzo(a)pyrène est en partie directement liée au pouvoir cancérogène de l’un de ses métabolites, le BPDE, qui se fixe au niveau de l’ADN des cellules et entraîne des mutations pouvant à terme aboutir au développement de cancers.
Outre leurs propriétés cancérogènes, les HAP présentent un caractère mutagène dépendant de la structure chimique des métabolites formés. Ils peuvent aussi entraîner une diminution de la réponse du système immunitaire augmentant ainsi les risques d’infection.
Partition gaz/particule
À l’issue des processus de formation essentiellement pyrolytiques, les HAP sont émis dans l’atmosphère, compartiment à partir duquel ils peuvent ensuite se disperser dans les autres compartiments de l’environnement. Durant leur temps de résidence dans l’atmosphère, les HAP coexistent à la fois en phase gazeuse et en phase particulaire.
Ce qui détermine la répartition des HAP entre la phase gazeuse et la phase particulaire, c’est la pression de vapeur saturante des composés. En effet, les HAP les plus légers, dont les pressions de vapeur saturante sont élevées, seront majoritairement présents dans la phase gazeuse alors que les HAP les plus lourds, dont les pressions de vapeur saturante sont plus faibles, seront plutôt liés à la phase particulaire. En général, les composés possédant deux cycles benzéniques seront présents en phase gazeuse alors que ceux possédant plus de six cycles seront plutôt rencontrés dans la phase particulaire.
Pour les composés intermédiaires (entre trois et six cycles), la répartition se fait entre la phase particulaire et la phase gazeuse. Lorsque la masse moléculaire des HAP augmente, et donc que le nombre de cycles aromatiques croît, la partition se fait en faveur de la phase particulaire. Jusqu’à quatre cycles benzéniques, les HAP sont majoritairement présents en phase gazeuse, et qu’au-delà, ils sont plutôt retrouvés en phase particulaire.
La température ambiante influence également la partition gaz/particule. En effet, la pression de vapeur saturante dépend de la température. Ainsi, plus la température augmente, plus les HAP auront tendance à être présents en phase gazeuse. D’ailleurs, il a été observé qu’en été le pourcentage des HAP en phase gazeuse est plus élevé qu’en hiver. Cependant, cette variation selon les saisons est beaucoup moins importante que celle du degré d’aromaticité des HAP.
Notes et références
- Marc J. Olivier, Chimie de l'environnement, 5e éd., PJB Éditeur, Lévis, 2007 (ISBN 978-2-9810039-0-4), chap. 6 («La pollution par les produits organiques anthropiques»)
- Polluants Organiques Persistants
- "Identification of the 'unidentified' IR emission features of interstellar dust?" , Leger, A.; Puget, J. L., Astronomy and Astrophysics (ISSN 0004-6361), vol. 137, no. 1, Aug. 1984, p. L5-L8.
- La Nutrition.fr, septembre 2007
- Hydrocarbures Aromatiques Polycycliques dans l’air ambiant document PDF de l'INERIS - pages 9 et 45, 46
Voir aussi
Bibliographie
- Anyakora, C. (2007). Polynuclear Aromatic Hydrocarbons. Tiré de : Nollet, L.M .L. (ed), Handbook of water analysis, CRC Press, 579-598.
- European Food Safety Autority (EFSA) (2008). Polycyclic Aromatic Hydrocarbons in Food - Scientific Opinion of the Panel on Contaminants in the Food Chain. The EFSA Journal, 724, 1-114.
- Harrison, R., M., Perry, R., Wellings, R., A. (1975). Polynuclear aromatic hydrocarbons in raw, potable and waste water. Water Res., 9, 331-46.
- Haritash, A., K., Kaushik, C., P. (2009). Biodegradation aspects of polycyclic aromatic hydrocarbons (PAHs): a review. Journal of Hazardous Materials, 169, 1–15.
- Höner, A. (2001). Polycyclic aromatic hydrocarbon (PAH) metabolites. Tiré de : Kleïbohmer, W. (éd.), Environmental Analysis, Handbook of Analytical Separations, Elsevier, 3, 99-121.
- Manoli, E., Samara, C. (1999). Polycyclic aromatic hydrocarbons in natural waters: sources, occurrence and analysis. Trends in analytical chemistry, 18, 6.
- United States Environmental Protection Agency (US-EPA) (1985). Evaluation and estimation of potential carcinogenic risks of polynuclear aromatic hydrocarbons: carcinogen assessment group. Office and Health and Environmental Assessment.
- Varanasi, U. (1989). Metabolism of polycyclic aromatic hydrocarbons in the aquatic environment. CRC Press, 341 p.
- Walker, H.C. (2008). Polycyclic Aromatic Hydrocarbons. Tiré de : Organic pollutants: an ecotoxicological perspective, CRC Press, 181-192.
Articles connexes
Lien externe
Wikimedia Foundation. 2010.
