- Fluorène
-
Fluorène 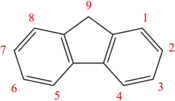
Structure du fluorène.Général Nom IUPAC 9H-Fluorène Synonymes 9H-Fluorène;
o-Biphénylèneméthane;
Diphénylèneméthane;
2,2'-Méthylènebiphényle;
2,3-Benzindène;
o-BiphénylméthaneNo CAS No EINECS SMILES InChI Apparence cristaux blancs Propriétés chimiques Formule brute C13H10 [Isomères] Masse molaire[3] 166,2185 ± 0,0111 g·mol-1
C 93,94 %, H 6,06 %,pKa 22,6 (dans le DMSO)[1] Susceptibilité magnétique χM 110,5×10-6 cm3·mol-1[2] Propriétés physiques T° fusion 113 à 115 °C[4] T° ébullition 295 °C[4] Solubilité 1,8 mg·l-1 (eau)[4] Masse volumique 1,2 g·cm-3[4] Point d’éclair 152 °C[4] Pression de vapeur saturante 13 mbar à 146 °C[4] Précautions Directive 67/548/EEC[5] 
NPhrases R : 50/53, Phrases S : 60, 61, SGH[5] 
AttentionComposés apparentés Isomère(s) Phénalène Unités du SI & CNTP, sauf indication contraire. Le fluorène ou 9H-fluorène est un composé chimique de la famille des hydrocarbures aromatiques polycycliques (HAP). Il se présente sous la forme de cristaux blancs, dégageant une odeur proche de celle du naphtalène.
Contrairement à ce que son nom pourrait laisser supposer, cette molécule n'a rien à voir avec l'élément chimique fluor dont elle est dépourvue; le nom de fluorène provient du fait que sous lumière ultraviolette (UV), le composé émet une lumière fluorescente violette.
Sommaire
Propriétés
Le fluorène est presque insoluble dans l'eau, mais soluble dans le benzène et l'éther. Les deux atomes d'hydrogène en position 9 sont acides, avec un pKA de 22,6 dans le DMSO. La réaction d'une base avec le fluorène donne donc un anion aromatique (de couleur orange très prononcée) très nucléophile. L'anion du fluorène est utilisé de façon similaire à celui du cyclopentadiène ou de l'indène comme ligand en chimie organométallique.
Occurrence
Le fluorène est naturellement présent dans le goudron, plus précisément dans les fractions à haute température d'ébullition. Il est obtenu par distillation de ces fractions. On le trouve aussi en faible quantité, avec d'autre hydrocarbures polycycliques, dans les produits de chauffage ou de combustion en manque d'oxygène de substances organiques. On en trouve aussi des traces dans la combustion de l'essence ou du diesel.
Utilisations
Le fluorène est utilisé pour fabriquer des matières plastiques, des colorants et des pesticides. Il est utilisé pour synthétiser la fluorénone, le fluorénol et le fluorène-9-méthanol
Le groupe fluorénylméthoxycarbonyle (Fmoc) est un groupe protecteur, utilisé dans la synthèse peptidique pour protéger les fonctions amines.
Le polyflurorène est utilisé comme luminophore dans les diodes électroluminescentes organiques (O-LED). Les co-polymères de fluorène sont aussi étudiés pour la fabrication de cellules photovoltaïques.Notes et références
- Equilibrium acidities in dimethyl sulfoxide solution, F. G. Bordwell, Acc. Chem. Res.; 1988; 456-463, DOI:10.1021/ar00156a004
- (en) Hyp J. Dauben, Jr., James D. Wilson et John L. Laity, « Diamagnetic Susceptibility Exaltation in Hydrocarbons », dans Journal of the American Chemical Society, vol. 91, no 8, 9 avril 1968, p. 1991-1998
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Entrée de « Fluorene » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 12/05/2009 (JavaScript nécessaire)
- SIGMA-ALDRICH
- (de) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en allemand intitulé « Fluroen » (voir la liste des auteurs)
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Fluroene » (voir la liste des auteurs)
Catégories :- Produit chimique dangereux pour l'environnement
- Hydrocarbure aromatique polycyclique
- Composé tricyclique
Wikimedia Foundation. 2010.
