- Acénaphtylène
-
Acénaphtylène 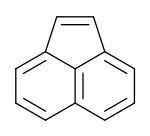
Général Nom IUPAC Acénaphtylène No CAS No EINECS PubChem ChEBI SMILES InChI Apparence solide jaune Propriétés chimiques Formule brute C12H8 [Isomères] Masse molaire[2] 152,1919 ± 0,0102 g·mol-1
C 94,7 %, H 5,3 %,Susceptibilité magnétique χM 111,6×10-6 cm3·mol-1[1] Propriétés physiques T° fusion 91,8 °C [3] T° ébullition 280 °C [3] Solubilité 3,927 mg·l-1 (eau,25 °C)[4] Masse volumique 0,8987 g·cm-3 à 16 °C Erreur de référence : Clôture </ref>manquante pour la balise<ref>.Thermochimie ΔfH0solide 190,8 kJ·mol-1 [5] ΔfusH° 6,94 kJ·mol-1 à 89,45 °C [5] ΔvapH° 64,3 kJ·mol-1 [6] Cp 166,4 J·K-1·mol-1 (solide,24,85 °C)
208,72 J·K-1·mol-1 (gaz,126,85 °C)[5]PCI -6 058 kJ·mol-1 (solide)[5] Précautions Directive 67/548/EEC[7] 
XiPhrases R : 22, Phrases S : 36, NFPA 704[8] SIMDUT[9] Produit non contrôlé SGH[10] 
AttentionÉcotoxicologie LogP 4,07 [11] Composés apparentés Isomère(s) Acénaphtène Unités du SI & CNTP, sauf indication contraire. L'acenaphtylène est un hydrocarbure aromatique polycyclique (HAP) constitué d'une molécule de naphtalène dont les carbones 1 et 8 sont reliés par un pont éthylénique. Il se présente sous la forme de poudre cristalline blanche à jaune qui, contrairement à la plupart des hydrocarbures aromatiques polycycliques, n'est pas fluorescente.
C'est un constituant du goudron, et on le trouve aussi dans la houille ainsi qu'en très faible quantité dans le pétrole. La réduction du pont éthylénique donne le composé voisin, l'acénaphtène.
Sommaire
Propriétés physico-chimiques
L'acénaphtylène est presque insoluble dans l'eau, mais est en revanche soluble dans le benzène, l'éther, le chloroforme et dans l'alcool à chaud. L'acénaphtylène a des propriétés mutagènes, toxiques et irritantes.
Utilisation
L'acénaphtylène est essentiellement réduit en acénaphtène qui est nécessaire à la synthèse de l'anhydride naphtalique et à la fabrication de matière plastiques, de colorants, de pigments de couleur, d'insecticides et de produits pharmaceutiques.
La polymérisation de ce composé donne des polymères ayant d'excellentes propriétés thermiques et mécaniques[12]: la polymérisation de l'acénaphtylène avec l'acétylène en présence d'un acide de Lewis donne un polymère conducteur utilisé comme finition anti-statique pour les plastiques, la cocondensation avec le phénol et le formaldéhyde forme des résines résistantes du point de vue chimique et thermique. L'acénaphtylène est un excellent anti-oxydant pour le caoutchouc à base d'éthylène et de propylène.Production et synthèse
L'acénaphtylène est disponible dans le goudron à une concentration d'environ 2 % et peut être synthétisé par déshydrogénation catalytique de l'acénaphtène[12].
Notes et références
- (en) Hyp J. Dauben, Jr., James D. Wilson et John L. Laity, « Diamagnetic Susceptibility Exaltation in Hydrocarbons », dans Journal of the American Chemical Society, vol. 91, no 8, 9 avril 1968, p. 1991-1998
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) W. M Haynes, CRC Handbook of chemistry and physics, Boca Raton, CRC Press/Taylor and Francis, 2011, 91e éd., 2610 p. (ISBN 978-143982-077-3), p. 3-4
- (en) Lizhong Zhu et Shaoliang Feng, « Synergistic solubilization of polycyclic aromatic hydrocarbons by mixed anionic–nonionic surfactants », dans Chemosphere, vol. 53, no 5, novembre 2003, p. 459-467
- Erreur de référence : Balise
<ref>incorrecte ; aucun texte n’a été fourni pour les références nomméesNIST. - (en) James S. Chickos, Donald G. Hesse, Sarah Hosseini, Joel F. Liebman, David G. Mendenhall, Sergej P. Verevkin, Klaus Rakus, Hans-Dieter Beckhaus et Christoph Rüchardt, « Enthalpies of vaporization of some highly branched hydrocarbons », dans The Journal of Chemical Thermodynamics, vol. 27, no 6, juin 1995, p. 693-705
- Entrée de « Acenaphthylene » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 19 janvier 2010 (JavaScript nécessaire)
- UCB Université du Colorado
- « Acenaphtylène » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- SIGMA-ALDRICH
- (en) P. Lee Ferguson, G. Thomas Chandler, Ryan C. Templeton, Amanda DeMarco, Wally A. Scrivens et Benjamin A. Englehart, « Influence of Sediment−Amendment with Single-walled Carbon Nanotubes and Diesel Soot on Bioaccumulation of Hydrophobic Organic Contaminants by Benthic Invertebrates », dans Environmental Sciences & Technology, vol. 42, no 10, 16 avril 2008, p. 3879-3885
- (en) Karl Griesbaum, Arno Behr, Dieter Biedenkapp, Heinz-Werner Voges, Dorothea Garbe, Christian Paetz, Gerd Collin, Dieter Mayer, Hartmut Höke, Hydrocarbons, Wiley-VCH Verlag GmbH & Co, coll. « Ullmann's Encyclopedia of Industrial Chemistry », 15 juin 2000
Catégories :- Produit chimique irritant
- Hydrocarbure aromatique polycyclique
- Composé tricyclique
Wikimedia Foundation. 2010.

