- Biofilm
-
 Autre exemple, essentiellement constitué d'algues couvrant une eau stagnante. Ce type de biofilm (en « voile » algual ou bactérien, ou les deux) ne perdure généralement pas (quelques jours à une ou deux semaines) sur l'eau, mais peut perdurer des années sur un sol (sable humide par exemple) ou sur de la vase
Autre exemple, essentiellement constitué d'algues couvrant une eau stagnante. Ce type de biofilm (en « voile » algual ou bactérien, ou les deux) ne perdure généralement pas (quelques jours à une ou deux semaines) sur l'eau, mais peut perdurer des années sur un sol (sable humide par exemple) ou sur de la vase
 Le biofilm prend ici l'aspect d'une fine « croute », formée d'algues et bactéries fixant efficacement le sable soumis à érosion (sur un turricule de taupinière creusée dans un sable acide, qui malgré les pluies reste en place fixé par la substance mucilagineuse produite par les algues, bactéries. C'est aussi un substrat pour certains lichens mais qui ont ici fortement régressé en raison de la pollution de l'air (zone d'agriculture intensive et proche de 4 papeteries et d'une grande verrerie; sur le Plateau d'Helfaut près de la Colonne d'Helfaut dans le Pas-de-Calais, en France)
Le biofilm prend ici l'aspect d'une fine « croute », formée d'algues et bactéries fixant efficacement le sable soumis à érosion (sur un turricule de taupinière creusée dans un sable acide, qui malgré les pluies reste en place fixé par la substance mucilagineuse produite par les algues, bactéries. C'est aussi un substrat pour certains lichens mais qui ont ici fortement régressé en raison de la pollution de l'air (zone d'agriculture intensive et proche de 4 papeteries et d'une grande verrerie; sur le Plateau d'Helfaut près de la Colonne d'Helfaut dans le Pas-de-Calais, en France)
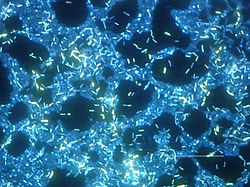 Les biofilms naturels sont fréquemment constitués de plusieurs espèces de microbes, éventuellement en associations symbiotiques. Ici il s'agit d'un biofilm polymicrobien cultivé sur une surface d'inox, en laboratoire, photographiée en microscopie à épifluorescence après 14 jours, avec coloration au 4,6-diamidino-2-phenylindole (DAPI) (échelle : trait = 20µm)
Les biofilms naturels sont fréquemment constitués de plusieurs espèces de microbes, éventuellement en associations symbiotiques. Ici il s'agit d'un biofilm polymicrobien cultivé sur une surface d'inox, en laboratoire, photographiée en microscopie à épifluorescence après 14 jours, avec coloration au 4,6-diamidino-2-phenylindole (DAPI) (échelle : trait = 20µm)
Un biofilm est une communauté multicellulaire plus ou moins complexe et symbiotique de micro-organismes (bactéries, champignons, algues ou protozoaires), adhérant entre eux et à une surface, et marquée par la sécrétion d'une matrice adhésive et protectrice.
Le biofilm est une étape normale ou potentielle du cycle de vie de la plupart des bactéries[1], qui affichent alors un comportement coopératif [1] et produisent des phénotypes différenciés conduisant à des fonctions spécifiques, parfois en réaction à un stress.
Sa structure est hétérogène, souvent sous forme d'une matrice extracellulaire, et composée de substances polymères. La définition d'un biofilm peut légèrement varier : certains auteurs choisissent par exemple d'exclure du terme « biofilm » les communautés bactériennes ne produisant pas leur propre matrice extracellulaire.S'étant jusque-là principalement attachée à étudier les cellules pour elles-mêmes et indépendamment de leur milieu, la microbiologie intègre les récents développements de la notion d'interactions avec le milieu et se tourne maintenant vers les biotopes, et notamment les biofilms, notamment observés comme habitat d'écotone ou comme élément du réseau trophique [2] .
Sommaire
Généralités
Le mode de vie en biofilm est l'un des deux modes de comportement des organismes unicellulaires – l'alternative étant la flottaison libre de type dit « planctonique », dans un médium liquide, fluide ou même solide. John William Costerton a proposé en 1978 le terme de biofilm en suggérant que ce serait le mode de vie naturel de la plupart des micro-organismes[3]. Cette proposition, qui s'appuyait initialement sur la comparaison du nombre de bactéries sous forme planctonique d'une part, et au sein de biofilms dans une rivière d'autre part, est désormais généralement admise par les microbiologistes.
Les biofilms sont, sauf exceptions, observés dans les milieux aqueux ou exposés à l'humidité. Ils peuvent se développer sur n'importe quel type de surface naturelle ou artificielle, qu'elle soit minérale (roche, interfaces air-liquide…) ou organique (peau, tube digestif des animaux, racines et feuilles des plantes), industrielle (canalisations, coques des navires) ou médicale (prothèses, cathéters)… Il est possible à un biofilm d'adhérer sur des matériaux « anti-adhésifs » comme le polytétrafluoréthylène (ou téflon). Voir l'article sur les micro-organismes extrémophiles pour la diversité étonnante de leurs habitats possibles dans les gammes de chaud, froid, pression, et autres extrêmes. Dans des conditions optimales de croissance, un biofilm peut rapidement devenir macroscopique, jusqu'à atteindre le mètre d'épaisseur si l'environnement le permet.
Hormis les cas où les bactéries se rassemblent sur une surface nutritive (bois immergé en décomposition par exemple), un biofilm n'est pas une parade à la pauvreté du milieu, mais plutôt à son agressivité envers les micro-organismes. Le biofilm croît d'ailleurs généralement d'autant plus rapidement que le milieu est riche en nutriments [4].
Traces fossiles
Les biofilms ont sans doute constitué les premières colonies d'organismes vivants, il y a plus de 3,5 milliards d'années. Avec les stromatolithes, ils semblent à l'origine des premières roches biogéniques et structures récifales, bien avant l'apparition des coraux.
Les voiles alguaux que l'on trouve encore sur certains sédiments exondés, certains sols humides ou certaines plages ou rivages d'eau douce pourraient aussi être à l'origine de processus de fossilisation, en particulier de traces (humaines, de dinosaures ou de microreliefs…). Certains biofilms encroutant sont capables de croître sur eux-mêmes ou plutôt sur les lamines générées par les générations précédentes de bactéries. Ils semblent, toujours avec les stromatolithes, à l'origine du premier puits de carbone majeur il y a plus de 3 milliards d'années.
L'environnement particulier du biofilm permet aux cellules de (ou les force à..) coopérer et agir les unes avec les autres de manière différente de ce qu'elles feraient en environnement libre. Les bactéries vivant dans un biofilm ont des propriétés sensiblement différentes de celles des bactéries « flottantes » de la même espèce, qui peut faire penser comme dans le cas des stromatolithes à des propriétés émergentes de super-organisme.
la promiscuité des bactéries dans le biofilm favorise aussi probablement le transfert horizontal de gènes de bactérie à bactérie de la même famille, ou à d'autres genres et familles.
Composition, propriétés, fonctions
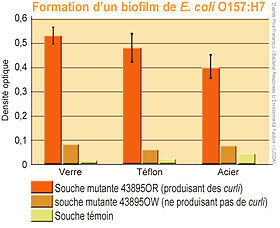
 2 colonies de deux souches différentes d' Escherichia coli O157:H7 ; la première (A) 43895OW ne produit pas de curli). La seconde (B) 43895OR produit des curlide type salé, qui lui permettent de former un solide biofilm pouvant créer des liaisons de type éthanol-NACL, et de se fixer sur des parois lisses (verre, inox[5], téflon). C'est un des principaux facteurs de résistance aux désinfectants, chlorés notamment). Ces deux cultures ont été faites sur une gelée d'agar durant 48 h à 28 °C
2 colonies de deux souches différentes d' Escherichia coli O157:H7 ; la première (A) 43895OW ne produit pas de curli). La seconde (B) 43895OR produit des curlide type salé, qui lui permettent de former un solide biofilm pouvant créer des liaisons de type éthanol-NACL, et de se fixer sur des parois lisses (verre, inox[5], téflon). C'est un des principaux facteurs de résistance aux désinfectants, chlorés notamment). Ces deux cultures ont été faites sur une gelée d'agar durant 48 h à 28 °C
Les espèces les mieux étudiées (parce que certaines souches en sont très pathogènes) sont Escherichia coli et Salmonella enterica. Des souches chlororésistantes et capables de produire des biofilms sur des substrats lisses (inox ou verre) et même antiadhésif (Téflon) présentant des similitudes ont été trouvées et cultivées pour ces deux espèces [6]. Ainsi le serovar de salmonelle Typhimurium - souche 43895OR, et les souches les plus résistantes de E.coli (ex : E.coli 43895OR) produisent toutes les deux des colonies bactériennes solidement consolidées par une matrice extracellulaire contenant des fibres de type curli (et cellulose dans le cas de la salmonelle), que se soit en culture sur de l'Agar, ou sur un substrat très lisse.
Dans tous les cas, les souches ayant formé des biofilms développent une résistance statistiquement plus élevée (P <0,05) que les cultures planctoniques des mêmes souches, face au peroxyde d'hydrogène, au chlore ou à des désinfectant à base d'ammonium quaternaire [6].
À la différence de E. coli, les Salmonelles semblent aussi capable de produire de la cellulose pour consolider leur biofilm[6].- Composition
Presque tous les micro-organismes ou certaines de leurs souches, éventuellement mutantes, ont développé des mécanismes d'adhérence aux surfaces et/ou les uns aux autres et ou avec les cellules symbiotes, et ou avec des cellules qu'ils doivent infecter pour survivre.
Ils peuvent s'intégrer à un biofilm en formation créé par d'autres espèces, de même qu'ils peuvent, plus ou moins facilement selon les cas, se détacher du biofilm sous l'action des forces mécaniques ou chimiques de l'environnement.
L'adhésion est le fait de divers mécanismes : fimbriae, pili, curli, impliquant des protéines de différents types (adhésines par exemple), production de cellulose [6] dans certains cas, etc. Il est donc mécaniquement et biochimiquement possible pour un biofilm d'abriter plusieurs espèces différentes, et de ce fait d'éventuellement être plus résistant, à l'érosion mécanique, à des détergents et à la désinfection (chloration par exemple, qui peut générer dans ce cas une chlororésistance); Il en va de même pour les biofilms monospécifiques (constitués, in vitro, par une seule espèce mise en culture) ; ces biofilms sont beaucoup plus résistants aux lavages agressifs quand une souche est accompagnée de souches « compagnonnes » [7]. On a montré que des souches de E. coli (dont de E. coli O157: H7) ne formant pas spontanément de biofilms peuvent néanmoins survivre en tant que souche compagnonne dans des biofilms générés par d'autres souches, bien qu'elles survivent alors moins bien que les souches plus résistantes en cas de stress.
De fait seuls quelques biofilms sont composés d'un seul type d'organisme - phénomène lié aux conditions environnantes plus souvent qu'à la nature même des organismes. Les biofilms naturels ne sont que rarement clonaux mais au contraire abritent souvent nombreux types de micro-organismes – bactéries, protozoaires et/ou algues, chaque groupe exécutant des fonctions métaboliques spécialisées, au profit de la résistance de la communauté constituée par le biofilm.
La « matrice » du biofilm à proprement parler, en plus de contenir les éléments dont sont faits les organismes qu'elle abrite (protéines, lipides, ADN, ARN…) est également constituée de polysaccharides, (peptidoglycanes, cellulose) et d'une importante proportion d'eau.
- Propriétés, fonctions
Un des aspects majeurs des biofilms est l'induction de changements dans les phénotypes correspondant au changement de mode de comportement (de «planctonique» et individuel, à fixe et communautaire). Des séries entières de gènes voient changer la durée et le rythme de leurs mécanismes d'activation, correspondant donc aussi à des changements de fonctions. L'environnement particulier du biofilm permet aux cellules de, ou les force à, coopérer et agir les unes avec les autres de manière différente qu'en environnement libre. Les bactéries vivant dans un biofilm ont des propriétés notablement différentes, voire très différentes de celles des bactéries « flottantes » de la même espèce.
Certaines souches de bactéries de laboratoire ont perdu leur capacité à former des biofilms, soit par les cultures et sélections successives de bactéries planctoniques, soit par la perte de leur plasmides naturels connus pour favoriser la formation de biofilm [8].
La plus spectaculaire propriété des biofilms est très certainement l'étonnante capacité de résistance qu'ils fournissent à leurs participants contre diverses agressions, comparée à la situation des mêmes organismes en état dit « planctonique ». Cette matrice est, d'autre part, elle-même, assez résistante pour que dans certaines conditions les biofilms puissent se fossiliser. Le biofilm pourrait d'ailleurs être être à l'origine des premiers processus de vie coloniale et récifale.
Les micro-organismes sont à plus d'un titre protégés et reliés entre eux par la matrice que fait le biofilm :
Protection passive
- Par sa simple présence cette matrice protège passivement les cellules dans un rôle de simple barrière physique contre l'entrée des agents antimicrobiens, détergents et antibiotiques[9],[10]: la matrice extracellulaire dense et la couche externe de cellules protègent l'intérieur de la communauté.
Protection métabolique.
- Autre facteur de résistance accrue : pour des raisons qui restent à déterminer les bactéries entourées de biofilm sont moins actives métaboliquement, donc moins réceptives aux agents antimicrobiens[11] et aux disruptions environnementales[10].
Protection active
- La résistance de P. aeruginosa aux antibiotiques a également été partiellement attribuée à des pompes de flux du biofilm expulsant activement les composants antimicrobiens[12],[13],[14]. Quelques biofilms se sont avérés contenir des canaux aqueux qui en sus de la distribution de nutriments permettent celle de molécules de signalisation, établissant la communication entre cellules par des signaux biochimiques. La formation du et par le biofilm est contrôlée par des signaux de cellule à cellule, et des mécanismes dits de quorum sensing [15],[16],[17],[18],[19], ou perception du quota, fondés sur le principe de masse critique. Les systèmes de perception du quota chez les bactéries gram-négatives détectent la densité des cellules en utilisant des signaux de cellule à cellule dépendant de la population, généralement une molécule d'acyl homosérine lactone. Quand cet [auto-inducer] atteint une certaine concentration critique, il active un régulateur transcriptionnel qui induit des gènes cibles spécifiques[20]. La nature et donc la fonction des molécules signalant les échanges de cellule à cellule changent à partir d'une concentration donnée des bactéries.
Protection génétique
- Dans certains cas, la résistance aux antibiotiques et biocides peut être exponentiellement multipliée. En effet, lors de leur implantation dans un biofilm l'expression génétique des bactéries est modifiée. Cet environnement d'échanges de matériel génétique permettant le transfert d'informations est donc propice à l'acquisition de nouveaux caractères.
Contribution à la corrosion ou dégradation de matériaux. De nombreux matériaux (métaux, bois) voient leur dégradation (ou corrosion) très accélérée, ou au contraire retardée, lorsqu'ils sont recouverts par certains biofilms, selon le contexte (humide ou sec, acide ou basique, chaud ou froid, eutrophe ou oligotrophe, etc.).
Formation et développement du biofilm
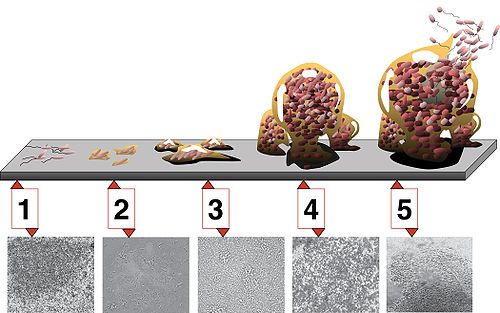 Les 5 étapes du développement d'un biofilm sur une surface dure.
Les 5 étapes du développement d'un biofilm sur une surface dure.
Étape 1 : attachement initial;
étape 2 : attachement irréversible;
étape 3 : apparition et « maturation I » du biofilm;
étape 4 maturation II;
étape 5, : dispersion.
Les photomicrographies (toutes à même échelle) sont celles d'un biofilm de Pseudomonas aeruginosa en développement. Vue (microscopie électronique) d'une agrégation de bactéries Staphylococcus aureus. ce biofilm s'est développé sur la surface luminale d'un cathéter placé à demeure. La substance qui colle les bactéries entre elles et au substrat est composée de polysaccharides sécrétés par ces bactéries. Ces molécules (polymères) contribuent à protéger les bactéries des "biofilm" des attaques d'agents antimicrobiens tels que les antibiotiques (Grossissement : 2363x) et certains autres biocides
Vue (microscopie électronique) d'une agrégation de bactéries Staphylococcus aureus. ce biofilm s'est développé sur la surface luminale d'un cathéter placé à demeure. La substance qui colle les bactéries entre elles et au substrat est composée de polysaccharides sécrétés par ces bactéries. Ces molécules (polymères) contribuent à protéger les bactéries des "biofilm" des attaques d'agents antimicrobiens tels que les antibiotiques (Grossissement : 2363x) et certains autres biocides
Les biofilms posent question dans le domaine médical, vétérinaire, de l'hygiène agroalimentaire, et de la qualité microbiologique des eaux potables.
L'eau potable - si elle était peu chargée en matière organique avant le traitement chloré - est considérée comme relativement bien désinfectée par la chloration permanente[21], mais elle est d'autant plus vulnérable en cas d'interruption de la chloration que :
- le contact permanent avec le chlore a pu éventuellement favoriser des mécanismes de chlororésistance chez les espèces présentes dans le biofilm (dont certaines peuvent être pathogènes)[21],
- la chloration ne saurait en aucun cas détruire les biofilms qui se sont développés sur toutes les parois des canalisations de distribution d'eau et qui constituent l'essentiel de la biomasse bactérienne présente dans réseau de distribution [21];
Même dans des réseaux de distribution d'eau « constamment chlorés, le biofilm peut représenter jusqu'à 107 bactéries/cm2 dont 1 % sont viables et capables de se multiplier, prouvant l'inefficacité réelle du traitement sur ces biomasses fixées » [21]; - on peut supposer que depuis un siècle environ (invention de la verdunisation de l'eau), le nombre de souches résistantes, et l'importance de la résistance a pu augmenter.
En France, l'étude des biofilm s'est notamment faite à l'INRA à partir de souches de culture de Bacillus subtilis (une bactérie Gram-positive, ubiquiste et facile à cultiver) qui durant dix ans a servi de modèle pour étudier les voies moléculaires et génétiques contrôlant la formation et l'organisation d'un biofilm. La plupart des données sur les biofilms de B. subtilis concernent les écotones air-liquide, ou air/gélose nutritive semi-solide. Quelques études ont porté sur la formation de macrocolonies complexes (formant parfois des excroissances en forme de thalles ou de haricots de 300 µm de hauteur) sur l'interface liquide/solide[22].
Formation
(Informations tirées du Center for Biofilm Engineering, Montana State University [1])
Considérant le biofilm au sens « embryologique » c'est-à-dire comme une entité/unité fonctionnelle de structure multicellulaire organisée, on peut également parler de cycle de développement ou de cycle de vie car le modèle en cinq étapes proposé ci-après peut se répéter indéfiniment:
- La première étape est l'adhésion (réversible) de micro-organismes mobiles à une surface, principalement par des liaisons chimiques non covalentes ou faibles. Ces liaisons entre la cellule (surtout ses protéines : les curlis) et la surface d'attachement sont de type van der Waals, électrostatique, ou encore acide-base de Lewis.
- Vient ensuite l'adhésion permanente par la formation de molécules protéiques appelées ligands, et de structures telles que les pili. Ces premiers points fixes augmentent la capacité d'ancrage d'autres micro-organismes en accroissant et en variant les surfaces d'ancrage. Noter que certaines espèces ne sont pas capables de s'ancrer elles-mêmes et s'intègrent à d'autres espèces déjà installées en colonies en s'attachant à leur biofilm. On a ici les prémices de la structure du biofilm: sa diversité de natures et de structures laisse envisager une diversité de fonctions.
- Les micro-organismes se divisent, commençant ainsi des microcolonies. À partir d'une concentration suffisamment dense d'individus, les microcolonies commencent la sécrétion du biofilm proprement dit.
- Le biofilm grandit et mûrit, s'épaississant jusqu'à devenir macroscopique, voire géant en conditions optimales.
- La cinquième étape est la phase de dispersion, dite phase planctonique : induits par le vieillissement du biofilm, certains stress ou carences, les micro-organismes peuvent activement se séparer du biofilm, parfois consommant la matrice qui représente une source d'énergie. Ces micro-organismes retournent à l'état dit « planctonique » de libre circulation et peuvent aller coloniser de nouvelles surfaces, complétant ainsi le cycle. Dans le mode de vie du biofilm et selon ce modèle en cinq étapes, la phase "planctonique" peut alors être vue comme une phase de dispersion.
Chez l'animal et chez l'Homme
Tous les organes internes creux communiquant avec l'environnement extérieur (bouche, tube digestif, vagin..) sont une niche écologique abritant un film d'organismes vivants plus ou moins riche. Ces organismes, bactériens notamment, co-évoluent avec leur hôte et son système immunitaire. Ils jouent un rôle fonctionnel important pour l'organisme, dans la digestion par exemple (et tout particulièrement chez les ruminants). Ce sont parfois des symbiotes (mutualistes), ce sont parfois des pathogènes ou parasites, ou ils le deviennent lorsque des conditions de déséquilibre leur permettent de pulluler (ex : mycose survenant après traitement antibiotique). Chez l'animal on parle alors de « flore » (flore intestinale, flore vaginale...) ou de microbiote.
Certains animaux sont également extérieurement couverts d'un biofilm (le paresseux a les poils qui verdissent en raison d'une algue qui y vit).Chez la flore
Surtout en zone tropicale, mais aussi en climat tempéré, un biofilm algual et bactérien, fongique et/ou lichénique existe sur les feuilles des arbres, les écorces et les racines. Certaines des bactéries qui le forment deviennent dans certaines circonstances (stress, gel, piqure d'insectes, etc) pathogènes, c'est le cas par exemple d'un pseudomonas commun (Pseudomonas syringae) dont certaines souches provoquent une maladie mortelle chez le marronnier (maladie émergente). Le biofilm bactérien et fongique se développe en été « en épiphyte » et prépare la bonne décomposition des feuilles avant même qu'elles ne tombent (à l'automne en climat tempéré, toute l'année en zone équatoriale).
Utilisation
Si les biofilms sont une source de contamination dans des secteurs tels que l'agro-alimentaire ou le médical, ils peuvent également être utilisés positivement dans les procédés de traitement d'eaux usées. Ces procédés utilisent des supports fixes (lit fixe, biofiltre) ou mobiles (moving bed, lit fluidisé) sur lesquels peuvent se développer des biofilms qui participent au traitement de la pollution. Dans le traitement des eaux résiduaires urbaines, ce type de procédé peut remplacer le procédé à boues activées en réduisant la taille des bassins d'aération et en supprimant l'étape de décantation. Les biofiltres aérés sont cependant des procédés intensifs et les coûts énergétiques associés peuvent être plus élevés pour la même quantité de pollution traitée. On peut également utiliser les procédés à biofilm en digestion anaérobie (méthanisation), pour le traitement des eaux usées industrielles riches en matière organique (agro-alimentaire, papeterie, pharmacie...).
D'autres usages sont envisageables dans le domaine de la lubrification sous l'eau ou des piles microbiennes (Ex : Projet BAGAM : Biofilms Amazonien issus de la biodiversité Guyanaise pour Applications en pile Microbiennes [23].
Biofilms et pathogènes
Presque tous les biofilms peuvent abriter (ou piéger) des organismes pathogènes pour d'autres espèces, y compris dans les tuyaux d'eau chaude où l'on trouve des Legionella d'origine hydro-telluriques qui survivent au chlore dans les biofilms[24],[25] qui la protègent de la chloration et semble jouer un rôle important pour sa survie dans les installations[26]. On en trouve y compris dans les biofilms de réseaux d'eau domestiques, parfois associée à Pseudomonas aeruginosa[27]. Outre la nature de l'eau (acidité, minéralisation, teneur en matières organiques et nutriments), la température et le type de matériaux utilisés en plomberie jouent aussi un rôle important dans la formation des biofilms[28],[29]. En conditions difficiles (chaleur élevée, biocide, etc.), les Legionelles croissent mieux et plus vite quand elles sont co-cultivées avec des amibes et en présence de cyanobactéries (qui modifient la teneur en nutriments du milieu)[24].
En outre, les biofilms peuvent se développer sur des surfaces inertes du corps humains : les dents où ils forment la plaque dentaire chez tous; mais aussi sur des prothèses (ce qui justifie les très strictes conditions des opérations d'implantation de celles-ci), ou des séquestres osseuses. Toute bactérie (même considérée comme n'étant pas pathogène en général) peut y former un biofilm et causer des fièvres (avec bactériémie) périodiques lors des phases de dispersion.
Articles connexes
Liens externes
Bibliographie
- (fr) C. Klingler, A. Filloux et A. Lazdunski (2005) « Les biofilms, forteresses bactériennes », La Recherche, 389.
- (en) Combating biofilms and antibiotic resistance using synthetic biology, Massacusetts Institute of technology Fev2008
Références
- Bridier A, Le Coq D, Dubois-Brissonnet F, Thomas V, Aymerich S, Briandet R. ; The spatial architecture of Bacillus subtilis biofilms deciphered using a surface-associated model and in situ imaging. PLoS One. 2011 Jan 18; 6(1):e16177. Epub 2011 Jan 18. (Résumé)
- Programme de recherche VASIREMI, soutenu par l'ANR Blanc coordonné par l'université de La Rochelle (C. Dupuy) 2006-2010. Trophic web linked to microbial biofilm in intertidal mud flats
- Costerton J. W., Geesey G. G., Cheng K. J., 1978, How bacteria stick. Scientific American 238 86-95
- Uhlich GA, Cooke PH, Solomon EB. ; Analyses of the red-dry-rough phenotype of an Escherichia coli O157:H7 strain and its role in biofilm formation and resistance to antibacterial agents. ; Appl Environ Microbiol. 2006 Apr;72(4):2564-72. (Résumé)
- Biofilm formation by Escherichia coli O157:H7 on stainless steel: effect of exopolysaccharide and Curli production on its resistance to chlorine. Ryu JH, Beuchat LR. Appl Environ Microbiol. 2005 Jan; 71(1):247-54. ([Résumé])
- Uhlich GA, Cooke PH, Solomon EB ; Analyses of the red-dry-rough phenotype of an Escherichia coli O157:H7 strain and its role in biofilm formation and resistance to antibacterial agents ; Appl Environ Microbiol. 2006 Apr;72(4):2564-72. . (Résumé)
- Uhlich GA, Rogers DP, Mosier DA Escherichia coli serotype O157:H7 retention on solid surfaces and peroxide resistance is enhanced by dual-strain biofilm formation ; Foodborne Pathog Dis. 2010 Aug;7(8):935-43. (Résumé)
- Ghigo J. M., 2001, Natural conjugative plasmids induce bacterial biofilm development. Nature 412 442-5
- Costerton, J. W., 2001, Cystic fibrosis pathogenesis and the role of biofilms in persistent infection. Trends Microbiol. 9:50-52
- G.A. O'Toole, L. A. Pratt, P. I. Watnick, D. K. Newman, V. B. Weaver, and R. Kolter, 1999, Genetic approaches to study of biofilms. Methods Enzymol. 310:91-109
- Drenkard, E. 2003, Antimicrobial resistance of Pseudomonas aeruginosa biofilms. Microb. Infect. 5:1213-1219
- Aeschlimann, J. R. 2003, The role of multidrug efflux pumps in the antibiotic resistance of Pseudomonas aeruginosa and other Gram-negative bacteria: insights from the Society of Infectious Diseases Pharmacists. Pharmacotherapy 23:916-924
- De Kievit, T. R., M. D. Parkins, R. J. Gillis, R. Srikumar, H. Ceri, K. Poole, B. H. Iglewski, and D. G. Storey, 2001, Multidrug efflux pumps: expression patterns and contribution to antibiotic resistance in Pseudomonas aeruginosa biofilms. Antimicrob. Agents Chemother. 45:1761-1770
- Poole, K. 2001, Multidrug efflux pumps and antimicrobial resistance in Pseudomonas aeruginosa and related organisms. J. Mol. Microbiol. Biotechnol. 3:255-264
- Davies, D. G., M. R. Parsek, J. P. Pearson, B. H. Iglewski, J. W. Costerton, and E. P. Greenberg, 1998, The involvement of cell-to-cell signals in the development of a bacterial biofilm. Science 280:295-298
- Hall-Stoodley, L., J. W. Costerton, and P. Stoodley, 2004, Bacterial biofilms: from the natural environment to infectious diseases. Nat. Rev. Microbiol. 2:95-108
- Mah, T.-F., B. Pitts, B. Pellock, G. C. Walker, P. S. Stewart, and G. A. O'Toole, 2003, A genetic basis for Pseudomonas aeruginosa biofilm antibiotic resistance. Nature 426:306-310
- Parsek, M. R., and P. K. Singh, 2003, Bacterial biofilms: an emerging link to disease pathogenesis. Annu. Rev. Microbiol. 57:677-701
- Smith, R. S., and B. H. Iglewski, 2003, P. aeruginosa quorum sensing systems and virulence. Curr. Opin. Microbiol. 6:56-60
- W.C. Fuqua, S.C. Winans, E.P. Greenberg, 1994. Quorum sensing in bacteria: the LuxR-LuxI family of cell density-responsive transcriptional regulators. J Bacteriol 176: 269-275
- La qualité de l'eau et assainissement en France : Rapport de l'OPECST n° 2152 (2002-2003) de M. Gérard MIQUEL, fait au nom de l'Office parlementaire d'évaluation des choix scientifiques et techniques (PDF,2,2 Moctets), déposé le 18 mars 2003, Voir Annexe 69 - Les membranes et l'eau potable, consulté 2011/02/27
- illustration en microscopie confocale à balayage laser (PLoS One. 2011 Jan 18;6(1):e16177., in The spatial architecture of Bacillus subtilis biofilms deciphered using a surface-associated model and in situ imaging déjà cité)
- P. Salvin (Univ. Des Antilles et de la Guyane), Présentation du projet BAGAM : Biofilms Amazonien issus de la biodiversité Guyanaise pour Applications en pile Microbiennes – AAP FRB 2009
- Declerck P (2010) Biofilms: the environmental playground of Legionella pneumophila. Environ Microbiol 12, 557-566.
- Lee HJ, Ho MR, Bhuwan M, Hsu CY, Huang MS, Peng HL, Chang HY (2010) Enhancing ATP-based bacteria and biofilm detection by enzymatic pyrophosphate regeneration. Analytical Biochemistry 399, 168-173
- Murga R, Forster TS, Brown E, Pruckler JM, Fields BS, Donlan RM (2001) Role of biofilms in the survival of Legionella pneumophila in a model potable-water system. Microbiology 147, 3121-3126.
- Moritz MM, Flemming HC, Wingender J (2010) Integration of Pseudomonas aeruginosa and Legionella pneumophila in drinking water biofilms grown on domestic plumbing materials. Int J Hyg Environ Health 213, 190-197.
- Rogers J, Dowsett AB, Dennis PJ, Lee JV, Keevil CW (1994) Influence of temperature and plumbing material selection on biofilm formation and growth of Legionella pneumophila in a model potable water system containing complex microbial flora. Applied and Environmental Microbiology 60, 1585-1592.
- Van der Kooij D, Veenendaal HR, Scheffer WJH (2005) Biofilm formation and multiplication of Legionella in a model warm water system with pipes of copper, stainless steel and cross-linked polyethylene. Water Research 39, 2789-2798
- Composition
Wikimedia Foundation. 2010.