- Dioxyde de carbone
-
Dioxyde de carbone 
Structure du dioxyde de carbone.Général Nom IUPAC Dioxyde de carbone Synonymes gaz carbonique
anhydride carboniqueNo CAS No EINECS PubChem ChEBI No E E290 SMILES InChI Apparence gaz comprimé liquéfié, incolore, inodore[1]. Propriétés chimiques Formule brute CO2 [Isomères] Masse molaire[2] 44,0095 ± 0,0014 g·mol-1
C 27,29 %, O 72,71 %,Propriétés physiques T° fusion -78,48 °C (sublimation, 760 mmHg)[3] T° ébullition -56,6 °C (5,12 atm)[3] Solubilité dans l'eau à 20 °C : 88 mL/100 mL[1] sous 1 bar de CO2, soit 1,69 g par kg d'eau (3,35 g à 0°C ; 0,973 g à 40°C ; 0,576 g à 60°C)[4] Masse volumique 1,87 kg·m-3 (gaz à 25 °C 1,013 bar)
plus dense que l'airPression de vapeur saturante 5 720 kPa (20 °C)[1]
569,1 mmHg (-82 °C);
104,2 mmHg (-100 °C);
10,5 mmHg (-120 °C)[3]Viscosité dynamique 0,07 mPa·s à -78 °C Point critique 31,3 °C ; 72,9 atm; 0,464 g·cm-3 [3] Point triple -56,6 °C à 5,11 atm [3] Conductivité thermique 3,840×10-5 cal·cm-1·s-1·K-1 à 20 °C Vitesse du son 259 m·s-1 (0 °C,1 atm) [6] Thermochimie ΔfH0gaz -393,52 kJ·mol-1 [7] Cp Propriétés électroniques 1re énergie d'ionisation 13,773 ± 0,002 eV (gaz)[9] Cristallographie Classe cristalline ou groupe d’espace P42/mnm Paramètres de maille a = 3,535 Å
b = 3,535 Å
γ = 90,00 ° [10]
c = 4,140 Å
α = 90,00 °
β = 90,00 °Volume 51,73 Å3 [10] Propriétés optiques Indice de réfraction  1,00045 (1 atm)
1,00045 (1 atm)Précautions Directive 67/548/EEC[11] Phrases S : 9, 23, Transport 20 1013
22 2187
- 1845 [11]SIMDUT[12] 
SGH[13] 
AttentionUnités du SI & CNTP, sauf indication contraire. Le dioxyde de carbone, aussi appelé gaz carbonique ou anhydride carbonique, est un composé chimique dont la formule est CO2, la molécule ayant une structure linéaire de la forme O=C=O. Il se présente, sous les conditions normales de température et de pression, comme un gaz incolore, inodore, à la saveur piquante.
Le CO2 est utilisé par l'anabolisme des végétaux pour produire de la biomasse à travers la photosynthèse, processus qui consiste à réduire le dioxyde de carbone par l'eau, grâce à l'énergie lumineuse reçue du Soleil et captée par la chlorophylle, en libérant de l'oxygène pour produire des oses, et en premier lieu du glucose par le cycle de Calvin. Le CO2 est libéré, à travers la chaîne respiratoire, par le catabolisme des plantes, des animaux, des fungi (mycètes, ou champignons) et des micro-organismes. Ce catabolisme consiste notamment à oxyder les lipides et les glucides en eau et en dioxyde de carbone grâce à l'oxygène de l'air pour produire de l'énergie et du pouvoir réducteur, sous forme respectivement d'ATP et de NADH + H+. Le CO2 est par conséquent un élément fondamental du cycle du carbone sur notre planète. Il est également produit par la combustion des énergies fossiles telles que le charbon, le gaz naturel et le pétrole, ainsi que par celle de toutes les matières organiques en général. Des quantités significatives de CO2 sont par ailleurs rejetées par les volcans et autres phénomènes géothermiques tels que les geysers.
Le dioxyde de carbone est naturellement présent dans l'atmosphère terrestre à une concentration de près de 0,039 % en volume au début des années 2010[14], c'est-à-dire 390 ppmv (parties par million en volume) ou 591 ppmm (parties par million en masse). En 2009, cette concentration atteignait précisément 386 ppmv[15], contre seulement 283,4 ppmv en 1839 d'après les carottes de glace prélevées dans la région du cap Poinsett dans l'Antarctique[16], soit une augmentation globale de 36,2 % en 170 ans[17].
Le CO2 est un gaz à effet de serre bien connu, transparent en lumière visible mais absorbant dans le domaine infrarouge, de sorte qu'il tend à bloquer la réémission vers l'espace de l'énergie thermique reçue au sol sous l'effet du rayonnement solaire ; il serait responsable de 26 % de l'effet de serre à l'œuvre dans notre atmosphère (la vapeur d'eau en assurant 60 %)[18], où l'augmentation de sa concentration serait en partie responsable du constaté à l'échelle de notre planète depuis les dernières décennies du XXe siècle [19] . Non seulement le dioxyde de carbone réchaufferait l'atmosphère de la planète, mais il se dissout aussi en partie dans les océans et les acidifie. Au cours du XXIe siècle, cette acidification pourrait devenir si importante que les coraux seront dans l'incapacité de constituer des récifs[réf. souhaitée].
Sommaire
Caractéristiques physico-chimiques
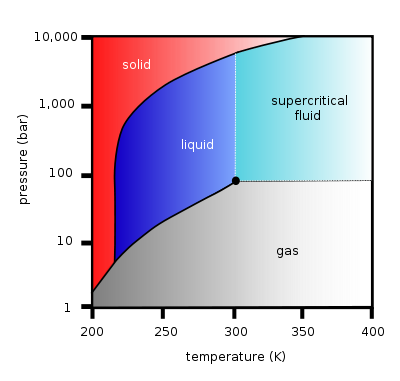 (en) Diagramme de phase pression-température du dioxyde de carbone, montrant le point triple et le point critique.
(en) Diagramme de phase pression-température du dioxyde de carbone, montrant le point triple et le point critique.
À pression atmosphérique, il se sublime à -78,5 °C[11] (passage de l'état solide à l'état gazeux), mais ne fond pas (passage de l'état solide à l'état liquide).
La phase liquide ne peut exister qu'à une pression minimale de 519 kPa (soit 5,12 atm), et dans un intervalle de température allant de -56,6 °C (point triple) à 31,1 °C au maximum à 7,38 MPa (soit 72,8 atm) (point critique).
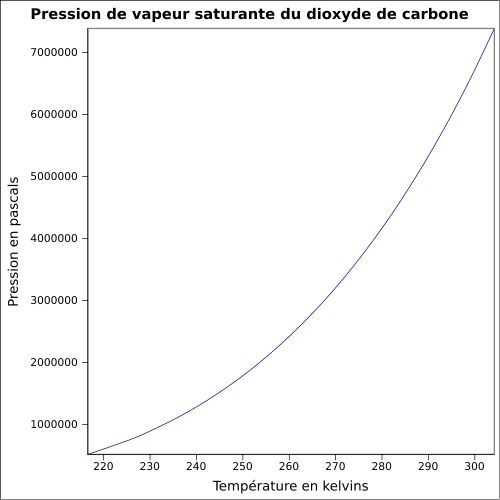
Pression de vapeur saturante[20]Température Pression État -138,15 °C 0,1 kPa solide -133,15 °C 0,2 kPa solide -128,15 °C 0,4 kPa solide -123,15 °C 0,8 kPa solide -118,15 °C 1,7 kPa solide -113,15 °C 3,1 kPa solide -108,15 °C 5,7 kPa solide -103,15 °C 9,9 kPa solide -98,15 °C 16,8 kPa solide -93,15 °C 27,6 kPa solide -88,15 °C 44,0 kPa solide -83,15 °C 68,4 kPa solide -78,15 °C 104 kPa solide -73,15 °C 155 kPa solide -68,15 °C 227 kPa solide -63,15 °C 327 kPa solide -58,15 °C 465 kPa solide -56,6 °C 518 kPa point triple[3] Température Pression État -53,15 °C 599 kPa liquide -48,15 °C 734 kPa liquide -43,15 °C 893 kPa liquide -38,15 °C 1 075 kPa liquide -33,15 °C 1 283 kPa liquide -28,15 °C 1 519 kPa liquide -23,15 °C 1 785 kPa liquide -18,15 °C 2 085 kPa liquide -13,15 °C 2 419 kPa liquide -8,15 °C 2 790 kPa liquide -3,15 °C 3 203 kPa liquide 1,85 °C 3 658 kPa liquide 6,85 °C 4 161 kPa liquide 11,85 °C 4 714 kPa liquide 16,85 °C 5 318 kPa liquide 21,85 °C 5 984 kPa liquide 26,85 °C 6 713 kPa liquide 31,3 °C 7 387 kPa point critique[3] Chaleurs latentes de transition d’état Transition Température Chaleur latente Vaporisation 0 °C 234,5 kJ.kg−1 Vaporisation -16,7 °C 276,8 kJ.kg−1 Vaporisation -28,9 °C 301,7 kJ.kg−1 Fusion -56,6 °C 199 kJ.kg−1 Solubilité aqueuse
Le CO2 se dissout dans l’eau et y forme de l’acide carbonique H2CO3 :
- CO2 (aq) + H2O(l)
 H2CO3 (aq), avec Kh = [H2CO3] / [CO2] ≈ 1,70×10-3 à 25 °C.
H2CO3 (aq), avec Kh = [H2CO3] / [CO2] ≈ 1,70×10-3 à 25 °C.
Il est également liposoluble.
L’acide carbonique n’est que modérément stable et il se décompose facilement en H2O et CO2. En revanche, lorsque le dioxyde de carbone se dissout dans une solution aqueuse basique (soude, potasse...), la base déprotone l’acide carbonique pour former un ion hydrogénocarbonate (HCO3–), aussi appelé ion bicarbonate, puis un ion carbonate (CO32–). De cette façon, la solubilité du CO2 est considérablement augmentée.
Par exemple, une solution aqueuse saturée de carbonate de potassium (K2CO3) a une concentration de 112 % (en masse) en carbonate à 20 °C.C'est ainsi que le calcaire se dissout dans l'eau, dans la plage de pH dans laquelle l'hydrogénocarbonate acide est stable, en produisant une solution d'hydrogénocarbonate(s) (de calcium et de magnésium...). Il est donc susceptible de précipiter lorsque le CO2 dissous est dégazé, comme dans la formation des stalagmites et des stalactites. Ainsi, en présence de CO2, le calcaire a une solubilité suivant celle des gaz (qui diminue avec la température) et non de celle des solides (qui augmente avec la température).
Histoire
Le dioxyde de carbone est l'un des premiers gaz (avec la vapeur d'eau) à avoir été décrit comme étant une substance distincte de l'air. Au XVIIe siècle, le chimiste et médecin flamand Jean-Baptiste Van Helmont observa qu'en brûlant du charbon de bois en vase clos, la masse des cendres résultantes est inférieure à celle du charbon. Son interprétation était que la masse manquante s'était transmutée en une substance invisible qu'il nomme « gas » ou spiritus sylvestre (« esprit sauvage »)[21].
Les propriétés du dioxyde de carbone furent étudiées plus en détail dans les années 1750 par le chimiste et physicien écossais Joseph Black. Il découvrit qu'en chauffant ou en versant un acide sur du calcaire (roche composée de carbonate de calcium), il en résultait l'émission d'un gaz, qu'il nomma « air fixe », mettant à mal la théorie du phlogiston encore enseignée à cette époque. Il observa que celui-ci est plus dense que l'air et qu'il ne peut ni entretenir une flamme, ni la vie d'un animal. Black découvrit également que lorsque le dioxyde de carbone est introduit dans une solution calcaire (hydroxyde de calcium), il en résulte un précipité de carbonate de calcium. Il utilisa ce phénomène pour illustrer le fait que le dioxyde de carbone est produit par la respiration animale et la fermentation microbienne[22].
En 1772, le chimiste anglais Joseph Priestley publia un ouvrage intitulé Impregnating Water with Fixed Air dans lequel il décrivit un processus consistant à verser de l'acide sulfurique (ou « huile de vitriol » comme on la nommait à cette époque) sur de la craie afin de produire du dioxyde de carbone, puis forçant le gaz à se dissoudre dans un bol d'eau. Il vint en fait d'« inventer » l'eau gazeuse[23]. Le procédé est ensuite repris par Johann Jacob Schweppe qui fonda, en 1790, à Londres une usine de production de soda connue sous le nom de Schweppes.
En 1781, le chimiste français Antoine Lavoisier mit en évidence le fait que ce gaz est le produit de la combustion du carbone avec le dioxygène.
Le dioxyde de carbone fut liquéfié pour la première fois en 1823 par Humphry Davy et Michael Faraday[24]. La première description du dioxyde de carbone en phase solide fut écrite par Charles Thilorier, qui en 1834 ouvrit un container pressurisé de gaz carbonique liquéfié et découvrit que le refroidissement produit par la rapide évaporation du liquide générait de la « neige » de CO2[25],[26].
Utilisations
Sous forme gazeuse
Le CO2 a beaucoup d’utilisations, dont :
- l’extinction des feux : beaucoup de datacenters (salles de serveurs d’ordinateurs) ou de salles des archives sont équipées d’un système qui, en cas d’incendie, remplit la salle de CO2 ce qui a pour effet d’éteindre le feu ;
- composant pétillant dans les boissons gazeuses ;
- en aquariophilie et culture sous serre pour une meilleure croissance des plantes ;
- en emballages à atmosphère contrôlée comme élément neutralisant ;
- en distribution d’eau potable, associé au carbonate, pour relever la dureté de l'eau (TH) des eaux trop agressives ;
- solubilisation du calcaire dans les eaux dures (TH > 25 °F) ;
- les pompes à bière : en étant en contact avec la surface de la bière, il évite son oxydation et prolonge sa conservation, contrairement à un compresseur utilisant de l'air (ambiant) ;
- on se sert aussi parfois du CO2 dans les grands abattoirs de porcs afin de les insensibiliser avant de les saigner ; il a été utilisé pour la conservation de la viande.
- l'extraction de la caféine du café (pour produire du café décaféiné d'une part et de la caféine d'autre part).
Sous forme liquide
Sous forme liquide, il est utilisé comme :
- réfrigérant pour congeler certains aliments ;
- réfrigérant dans l’industrie électronique ;
- agent d’extinction dans les extincteurs dits « au dioxyde de carbone », on parle parfois de neige carbonique parce que le CO2 liquide se solidifie immédiatement à la sortie de l’extincteur en produisant une poudre blanche ;
- agent propulseur (et parfois également carbonatant) pour les boissons servies à la pression.
Quand il est utilisé comme fluide frigorigène, le CO2 porte la dénomination R744.
À pression atmosphérique, le dioxyde de carbone n’est jamais sous forme liquide. Il passe directement de la forme solide à la forme gazeuse (sublimation).
Sous forme solide
 Granulats de « glace sèche » se sublimant à l'air.
Granulats de « glace sèche » se sublimant à l'air.
Le dioxyde de carbone sous forme solide a de nombreuses appellations : « glace carbonique », « neige carbonique », « carboglace », « glace sèche ». Il est issu de la solidification du CO2 liquide. On obtient de la neige carbonique qui est ensuite comprimée pour obtenir de la glace carbonique.
Dans sa phase solide, cette glace carbonique se sublime en ne laissant aucun résidu, selon une chaleur latente de fusion de 196,104 kJ/kg (soit 8,63 kJ/mol), à -78,5 °C et à 1 atm[27],[28]. On lui a donc rapidement trouvé de multiples utilisations en tant que réfrigérant.
Il est commercialisé sous différentes présentations selon son usage :
- en granules (de la taille d'un grain de riz de 3 mm de diamètre) : essentiellement pour le nettoyage et le décapage cryogénique ;
- en bâtonnets (d'une longueur d'environ 16 mm) : pour la conservation, le transport des produits sous température dirigée (produits pharmaceutiques, transport de surgelés, transport d'échantillons, etc.) ;
- pour la recherche fondamentale ou appliquée ;
- pour la vinification : il ralentit la fermentation et évite l'oxydation ;
- en plaquette ou en blocs :
- pour le ravitaillement aérien (catering), les traiteurs, les pompes funèbres, etc.
- en pains :
- pour faire de la fumée épaisse (effets spéciaux, cinéma, vidéo).
Le dioxyde de carbone sous forme solide est également présent en abondance aux pôles de la planète Mars, où il forme de véritables calottes glaciaires.
En phase supercritique
Au-delà de son point critique, le dioxyde de carbone entre dans une phase appelée supercritique. La courbe d'équilibre liquide-gaz est interrompue au niveau du point critique, assurant à la phase supercritique un continuum des propriétés physico-chimiques sans changement de phase. C'est une phase aussi dense qu'un liquide mais assurant des propriétés de transport (viscosité, diffusion) proches de celles d'un gaz. Le dioxyde de carbone supercritique est utilisé comme solvant vert, les extraits étant exempts de trace de solvant.
Sous cette forme, il sert :- à la décaféination du café ;
- à l'élimination de la 2,4,6-trichloroanisole (TCA) des bouchons de liège traités au chlore (ou à l'hypochlorite) pour éviter de donner un goût bouchonné au vin après sa mise en bouteille ;
- à la mise en forme de principes actifs micronisés et sous forme nanométrique ;
- à l'extraction de composés chimiques ou biologiques ;
- à la purification de composés chimiques (phase mobile en chromatographie, notamment en SFC) ;
- pour le transport et le stockage lors de la séquestration géologique du dioxyde de carbone (dans de rares applications industrielles).
Réactivité
L'électronégativité des atomes d'oxygène rend le carbone central très électrophile. De très nombreux nucléophiles peuvent donc réagir avec le dioxyde de carbone mais le produit de la réaction n'est pas forcément stable. En général, on place de la carboglace dans un récipient fermé muni d'un tuyau ; la carboglace se sublime et on fait buller le dioxyde de carbone gazeux dans le milieu réactionnel.
Quelques exemples de réaction :
- avec une amine : on appelle cette réaction une carbonatation. Le produit est un hydrogénocarbonate d'ammonium (R3N + CO2 + H2O → R3NH+HCO3–).
- avec un carbanion : on forme un acide carboxylique après hydrolyse.
- avec l'eau.
Toxicité
L'air contient aujourd'hui environ 0,04 % de CO2. À partir d'une certaine concentration dans l'air, ce gaz s'avère dangereux voire mortel à cause du risque d'asphyxie par privation d'oxygène, bien que le CO2 ne soit pas chimiquement toxique. La valeur limite d'exposition est de 3 % sur une durée de 15 minutes[réf. nécessaire]. Cette valeur ne doit jamais être dépassée. Au-delà, les effets sur la santé sont d'autant plus graves que la teneur en CO2 augmente. Ainsi, à 2 % de CO2 dans l’air, l'amplitude respiratoire augmente. À 4 %, la fréquence respiratoire s'accélère. À 10 %, peuvent apparaître des troubles visuels, des tremblements et des sueurs. À 15 %, c'est la perte de connaissance brutale. À 25 %, un arrêt respiratoire entraîne le décès.
Gaz à effet de serre
Le CO2 serait le deuxième gaz à effet de serre le plus important dans l'atmosphère après la vapeur d'eau, contribuant respectivement à hauteur de 26 % et 60 % à ce phénomène[18]. Si la réalité du réchauffement climatique observé à l'échelle planétaire depuis le siècle dernier n'est aujourd'hui plus guère contestée d'un point de vue scientifique[29], l'importance exacte du dioxyde de carbone dans ce processus demeure encore à clarifier[30]. La réduction des émissions anthropiques est visée par le protocole de Kyōto ainsi que par la directive 2003/87/CE ; sa séquestration géologique à long terme fait l'objet de recherches en cours.
Recherche
Le comportement et les impacts de ce gaz dans l'air font l'objet d'une recherche active. 500 scientifiques ont été conviés à Iéna, en Allemagne, du 13 au 19 septembre 2009 pour faire le point sur la connaissance, lors de la 8e conférence internationale de recherche sur le dioxyde de carbone (la première s'est tenue en 1981)[31].
Notes et références
- DIOXYDE DE CARBONE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Carbon dioxide sur Hazardous Substances Data Bank. Consulté le 8 mars 2010
- Bernard M. é Busnot F. (1996). Usuel de chimie générale et minérale. Ed. Dunod, Paris, p.229.
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, 1997, 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- (en) W. M Haynes, Handbook of chemistry and physics, CRC, 2010-2011, 91e éd., 2610 p. (ISBN 9781439820773), p. 14-40
- (en) Irvin Glassman, Richard A. Yetter, Combustion, Elsevier, 2008, 4e éd., 773 p. (ISBN 978-0-12-088573-2), p. 6
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, 2 et 3, Huston, Texas, Gulf Pub. Co., 1996 (ISBN 0-88415-857-8, ISBN 978-0-88415-858-5, ISBN 978-0-88415-859-2)
- (en) David R. Lide, Handbook of chemistry and physics, CRC, 2008, 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 10-205
- Carbon Dioxide sur www.reciprocalnet.org. Consulté le 12 décembre 2009
- Entrée du numéro CAS « 124-38-9 » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 6 décembre 2008 (JavaScript nécessaire)
- « Dioxyde de carbone » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- SIGMA-ALDRICH
- (en) NOAA Earth System Research Laboratory « Recent Mauna Loa CO2. »
- Données du NOAA et du Mauna Loa Observatory (MLO).
- (en) Carbon Dioxide Information Analysis Center – juin 1998 « Historical CO2 record derived from a spline fit (20 year cutoff) of the Law Dome DE08 and DE08-2 ice cores. », par D. M. Etheridge, L. P. Steele, R. L. Langenfelds, R. J. Francey (Division of Atmospheric Research, CSIRO, Aspendale, Victoria, Australia), J.-M. Barnola (Laboratoire de glaciologie et géophysique de l'environnement, Saint-Martin-d'Hères Cedex, France) et V. I. Morgan (Antarctic CRC and Australian Antarctic Division, Hobart, Tasmania, Australia).
- Le taux de CO2 atmosphérique attendu à la fin du XXIe siècle est estimé entre 540 et 970 ppmv selon les simulations retenues (modèle ISAM et modèle Bern-CC) :
(en) United Nations Environment Programme (UNEP) – Third Assessment Report "Climate Change 2001" « Climate Change 2001: Working Group I: The Scientific Basis – Chapter 3. The Carbon Cycle and Atmospheric Carbon Dioxide, » Executive Summary. - (en) J. T. Kiehl et Kevin E. Trenberth, « Earth’s Annual Global Mean Energy Budget », dans Bull. Am. Meteorol. Soc., vol. 78, no 2, février 1997, p. 197-208 [texte intégral, lien DOI (pages consultées le 28 novembre 2010)]
- Climate Change: A Summary of the Science (Sept 2010), Royal Society (UK)
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, 2009, 90e éd., Relié, 2804 p. (ISBN 978-1-4200-9084-0), p. 6-107
- (en) « Carbon Dioxide : Spiritus Sylvestre »Ebbe Almqvist, History of industrial gases, Springer, 2003 (ISBN 978-0-306-47277-0), p.
- Sigaud de La Fond, Essai sur différentes espèces d'air-fixe ou de gaz …, Paris, Chez P. Fr. Gueffier, 1785
- Joseph Priestley, « Observations on Different Kinds of Air », dans Phil. Trans., vol. 62, 1772, p. 147–264 (ISSN 0260-7085) [texte intégral, lien DOI]
- Humphry Davy, « On the Application of Liquids Formed by the Condensation of Gases as Mechanical Agents », dans Phil. Trans., vol. 113, 1823, p. 199–205 (ISSN 0261-0523) [texte intégral [PDF], lien DOI]
- Charles Thilorier, « Solidification de l'Acide carbonique », dans C.R. Hebd. Séances Acad. Sci., vol. 1, 1835, p. 194-196 [texte intégral]
- H.D. Roller Duane, « Thilorier and the First Solidification of a "Permanent" Gas (1835) », dans Isis, vol. 43, no 2, 1952, p. 109–113 (ISSN 0021-1753) [lien DOI]
- http://encyclopedia.airliquide.com/encyclopedia.asp?CountryID=19&GasID=26&LanguageID=2
- http://hydroland.pagesperso-orange.fr/CO2.htm
- (en) Climate change: How do we know? - NASA
- (en) Temperature and CO2 Correlations Found in Ice Core Records - MIT
- (en) 8th International Carbon Dioxide Conference (ICDC8) - Site officiel
Articles connexes
- Émissions de CO2
- Gaz à effet de serre
- Cycle du carbone
- Liste des pays par émissions de dioxyde de carbone
- Puits de carbone
- Lac Monoun
- Lac Nyos
- Lac Kivu
- Portail de la chimie
- Portail du froid et de la climatisation
Catégories :- Oxyde de carbone
- Composé inorganique du carbone
- Gaz inorganique
- Réfrigérant
- Gaz à effet de serre
- Pollution de l'air
- CO2 (aq) + H2O(l)
Wikimedia Foundation. 2010.