- Dioxyde d'uranium
-
Dioxyde d'uranium 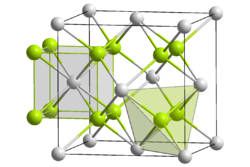
__ U4+ __ O2-
Structure du dioxyde d'uraniumGénéral Nom IUPAC Dioxyde d'uranium No CAS No EINECS No RTECS SMILES InChI Apparence cristaux noirs à bruns ou poudre noire à brune[1] Propriétés chimiques Formule brute UO2 Masse molaire[2] 270,0277 ± 0,0006 g·mol-1
O 11,85 %, U 88,15 %,Propriétés physiques T° fusion 2 865 °C[1] Solubilité dans l'eau : nulle[1] Masse volumique 11,0 g·cm-3[1] Cristallographie Structure type fluorite (CaF2)[3] Précautions 
Composé radioactifDirective 67/548/EEC[4] 
T+
NPhrases R : 26/28, 33, 51/53, Phrases S : (1/2), 20/21, 45, 61, SGH[4] 


DangerUnités du SI & CNTP, sauf indication contraire. Le dioxyde d'uranium est l'oxyde d'uranium de formule UO2. C'est un solide noir dont la maille cristalline est constituée d'atomes d'uranium en sous-réseau cubique à faces centrées et d'atomes d'oxygène en sous-réseau cubique.
Sommaire
Production et propriétés chimiques
C'est le constituant naturel de la pechblende, qui est le principal minerai d'uranium.
On le prépare industriellement à partir du trioxyde d'uranium UO3 lors des processus d'enrichissement de l'uranium et de traitement des déchets nucléaires :
Le dioxyde d'uranium a la même structure cristalline que la fluorine CaF2, qui est également celle des dioxydes de neptunium et de plutonium.
Il s'oxyde en octaoxyde de triuranium U3O8 par chauffage au contact de l'oxygène de l'air :Conductivité thermique
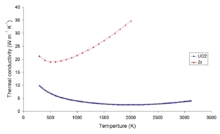
L'une des propriétés remarquables du dioxyde d'uranium est sa très faible conductivité thermique, qui peut engendrer des surchauffes locales au cœur du combustible nucléaire.
Utilisations
Le dioxyde d'uranium est essentiellement utilisé dans les barres de combustible nucléaire, principalement sous forme UO2 ou mélangé au dioxyde de plutonium PuO2 pour donner du combustible MOX.
Il peut également être employé comme catalyseur, notamment dans la dégradation des composés organiques volatils en phase gazeuse, l'oxydation du méthane en méthanol et la désulfuration des pétroles. Dans cet usage, il se montre plus efficace et plus stable que les catalyseurs du marché employés dans le retraitement des COV, tels que les métaux précieux, le rutile TiO2 et l'oxyde de cobalt(II,III) CoO•Co2O3.
À partir d'uranium appauvri, il peut être utilisé à des fins de radioprotection, notamment en entrant dans la composition de bétons où il sert de grave.
Le dioxyde d'uranium est un matériau semiconducteur aux propriétés particulièrement intéressantes[5] :
- il a une largeur de bande interdite de 1,3 eV, intermédiaire entre celles du silicium et de l'arséniure de gallium GaAs, proche de l'optimum d'efficacité pour l'absorption du rayonnement solaire. Il a un spectre d'absorption assez large, incluant l'infra-rouge, ce qui accroît encore son efficacité, et une conductivité électrique intrinsèque à température ambiante voisine de celle du silicium monocristallin. Il peut ainsi être utilisé pour réaliser des cellules solaires de type Schottky ;
- sa constante diélectrique est voisine de 22, contre seulement 11,2 pour le silicium et 14,1 pour le GaAs, ce qui rend possible la réalisation de circuits intégrés ayant une plus forte densité d'intégration avec UO2 qu'avec Si et GaAs ; ces circuits ont également une tension de claquage plus élevée et une moins grande susceptibilité à l'effet tunnel CMOS ;
- son coefficient Seebeck à température ambiante est de l'ordre de 750 µV/K, près du triple de celui de la plupart des matériaux étudiés pour les applications thermoélectriques ;
- tout comme l'octaoxyde de triuranium U3O8, le dioxyde d'uranium UO2 est une céramique résistante aux températures élevées, jusqu'à pas moins de 2 300 °C, ce qui le rend apte à servir pour des applications à haute température ;
- le dioxyde d'uranium a également une bonne tenue aux radiations, ce qui permet de l'utiliser pour réaliser des composants électroniques durcis aux radiations.
Les propriétés électriques du dioxyde d'uranium sont très sensibles à sa stœchiométrie. Ainsi, la conductivité électrique du UO1,994 est inférieure de plusieurs ordres de grandeur à celle du UO2,001. Ceci, avec la difficulté à maîtriser le dopage de ce matériau, constitue un obstacle au développement du dioxyde d'uranium comme matériau semiconducteur.
Notes et références
- DIOXYDE D'URANIUM, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) Bodie E. Douglas, Shih-Ming Ho, Structure and Chemistry of Crystalline Solids, Pittsburgh, PA, USA, Springer Science + Business Media, Inc., 2006, 346 p. (ISBN 0-387-26147-8)
- Entrée de « Uranium compounds » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 14 septembre 2011 (JavaScript nécessaire)
- [PDF] Semiconductive Properties of Uranium Oxides
Catégories :- Composé de l'uranium
- Produit chimique très toxique
- Produit chimique dangereux pour l'environnement
- Oxyde
- Matériau nucléaire
- Matériau semi-conducteur
Wikimedia Foundation. 2010.