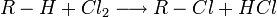- 13465-05-9
-
Acide chlorhydrique
 Cet article concerne le chlorure d’hydrogène en solution. Pour le gaz, voir Chlorure d'hydrogène.
Cet article concerne le chlorure d’hydrogène en solution. Pour le gaz, voir Chlorure d'hydrogène.Acide chlorhydrique 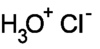
Général Nom IUPAC acide chlorhydrique Synonymes solution de chlorure d'hydrogène No CAS No EINECS No E E507 Apparence Liquide incolore Propriétés chimiques Formule brute HCl [Isomères] Masse molaire 36,461 g∙mol-1
H 2,76 %, Cl 97,23 %,pKa acide fort dans l'eau Propriétés physiques T° fusion -30 °C, 37 % HCl[1] T° ébullition 48 °C, 38 % HCl Solubilité 700 g par litre d'eau Masse volumique 1,19 g/cm³ (solution à 37%)[1] T° d’auto-inflammation N/A Viscosité dynamique 1,53 mPa.s à 25 °C Thermochimie S0gaz, 1 bar 186 9 kJ∙K-1∙mol-1 ΔfH0gaz -92 31 kJ∙mol-1 Précautions Directive 67/548/EEC 
CPhrases R : 34, 37, Phrases S : 26, 36, 45, Transport 80 1789 NFPA 704 Classification du CIRC Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[2] Inhalation Les vapeurs peuvent être mortelles Peau Peut provoquer de graves blessures Yeux Très dangereux Ingestion Toxique, parfois mortelle Unités du SI & CNTP, sauf indication contraire. L'acide chlorhydrique est une solution aqueuse ayant pour solutés des ions oxonium H3O+ et des ions chlorure Cl-. On peut l'obtenir par dissolution de chlorure d'hydrogène HCl qui est un gaz. Ce dernier est un acide fort qui s'ionise totalement en solution aqueuse. L'acide chlorhydrique est le principal constituant des acides gastriques. C'est un acide couramment utilisé comme réactif dans l'industrie chimique. L'acide chlorhydrique étant un liquide très corrosif, il doit être manié avec précaution. L'acide chlorhydrique concentré peut avoir un pH inférieur à 1.
L'acide chlorhydrique, connu également dans l'histoire sous le nom d'acide muriatique (ce nom est antérieur à la découverte du chlore et de la formule chimique HCl) a été découvert par l'alchimiste Jabir Ibn Hayyan au voisinage de l'an 800. C'est une espèce chimique qui a été fréquemment utilisée dans l'histoire depuis les débuts de la chimie. Au Moyen Âge, il était utilisé par les alchimistes dans leur quête de la pierre philosophale (sous le nom d'« esprit de sel » ou acidum salis). Il fut ensuite utilisé par de nombreux scientifiques, parmi lesquels Glauber, Priestley ou Davy, qui contribuèrent à établir la chimie moderne.
Au cours de la révolution industrielle, l'acide chlorhydrique devint un réactif chimique industriel important utilisé dans de nombreuses applications, notamment pour la production à grande échelle de composés organiques comme le chlorure de vinyle pour le PVC, ou comme le 4,4'-MDI/Diisocyanate de toluène pour le polyuréthane, ainsi que pour des applications à plus petite échelle comme la production de gélatine ou le traitement du cuir. La production d'acide chlorhydrique est voisine à l'heure actuelle de 20 millions de tonnes par an.
Sommaire
Histoire
L'acide chlorhydrique a été découvert au voisinage de l'an 800 par l'alchimiste arabo-yéménite Jabir Ibn Hayyan, qui l'obtint en mélangeant du sel (NaCl) et du vitriol (acide sulfurique H2SO4 en solution[3]. Jabir découvrit et inventa un grand nombre de produits chimiques, et relata ses découvertes dans plus de vingt ouvrages qui permirent la propagation de ses connaissances sur l'acide chlorhydrique et d'autres produits chimiques pendant plusieurs siècles. Son invention de l'eau régale, mélange d'acide chlorhydrique et d'acide nitrique permettant de dissoudre l'or, participa à la quête de la pierre philosophale.
Au Moyen Âge, les alchimistes européens connaissaient l'acide chlorhydrique sous le nom d'esprit de sel ou acidum salis. La vapeur, le chlorure d'hydrogène, était appelée gaz acide marin. L'ancien nom acide muriatique possède la même origine (muriatique signifie "appartenant au sel ou à l'eau de mer"), et le nom est parfois encore utilisé. Basilius Valentinus, l'abbé-alchimiste de l'abbaye d'Erfurt (Allemagne), en produisit une quantité importante au XVe siècle.
Au XVIIe siècle, Johann Rudolf Glauber de Karlstadt am Main (Allemagne) utilisa du sel (NaCl) et de l'acide sulfurique pour préparer du sulfate de sodium (Na2SO4), produisant ainsi du chlorure d'hydrogène gazeux (HCl). Joseph Priestley de Leeds prépara du chlorure d'hydrogène pur en 1772, et en 1818 Humphry Davy de Penzance (Royaume-Uni) démontra que ce produit chimique est constitué d'hydrogène et de chlore.
Au cours de la révolution industrielle, la demande de substances alcalines, et notamment de carbonate de sodium, augmenta fortement en Europe, et le nouveau procédé industriel mis au point par Nicolas Leblanc permettait une production bon marché à grande échelle. Dans le procédé Leblanc, du sel est transformé en carbonate de sodium, en utilisant comme réactifs de l'acide sulfurique, de la craie et du charbon, avec également une production secondaire de chlorure d'hydrogène gazeux. Jusqu'à ce que la promulgation en 1863 de l'Alkali Act l'interdise au Royaume-Uni, le chlorure d'hydrogène était relâché dans l'air. À la suite de cette interdiction, les producteurs de carbonate de sodium furent contraints de dissoudre le gaz dans l'eau, produisant ainsi de l'acide chlorhydrique à l'échelle industrielle.
Lorsque le procédé Leblanc fut remplacé au début du XXe siècle par le procédé Solvay, sans production secondaire d'acide chlorhydrique, celui-ci s'était d'ores et déjà imposé comme un réactif chimique important pour un grand nombre d'applications. Son intérêt commercial contribua à l'émergence d'autres techniques de production, qui sont toujours utilisées à l'heure actuelle (voir dans la suite).
L'acide chlorhydrique est cité comme un précurseur dans la Table 2 de la Convention contre le trafic illicite de stupéfiants et de substances psychotropes de 1988 contre le trafic de drogues, du fait de son utilisation dans la synthèse d'héroïne et de cocaïne.
Chimie
Le chlorure d'hydrogène (HCl(g)) est un monoacide, qui se dissocie (s'ionise) pour donner un ion H+ (un proton). L'autre ion formé lors de la dissociation est l'ion chlorure Cl-. En solution aqueuse, l'ion H+ se lie à une molécule d'eau pour former un ion oxonium H3O+.
-
- HCl(g) + H2O(l) → H3O+(aq) + Cl-(aq)
L'acide chlorhydrique peut donc être utilisé pour préparer des sels dits chlorures, comme par exemple le chlorure de sodium NaCl(s). L'acide chlorhydrique est un acide fort : il est totalement dissocié dans l'eau.
Les monoacides possèdent une seule constante de dissociation acide, Ka, qui est liée au taux de dissociation de l'acide dans l'eau. Pour un acide fort comme HCl, le Ka est très élevé (>1). Des tentatives ont été faites pour assigner une constante Ka à HCl. Lorsqu'un sel de chlorure comme NaCl(s) est ajouté à HCl aqueux, il n'a pratiquement aucun effet sur le pH, ce qui indique que l'ion Cl- est une base conjuguée extrêmement faible et que HCl est totalement dissocié en solution aqueuse. Pour des solutions d'acide chlorhydrique concentrées ou intermédiaires, l'hypothèse que la molarité des ions H+ est égale à la molarité d'HCl est excellente, avec un accord de quatre chiffres significatifs.
Parmi les acides forts courants en chimie, tous inorganiques, l'acide chlorhydrique est le monoacide le moins susceptible de subir une réaction parasite d'oxydo-réduction. Il est l'un des acides les moins dangereux à manipuler : en dépit de son acidité, il produit des ions chlorure très peu réactifs et non toxiques. Les solutions d'acide chlorhydrique moyennement concentrées sont stables et leur concentration ne varie pas dans le temps. Ces propriétés, alliées au fait qu'il est disponible comme réactif pur, font de l'acide chlorhydrique un très bon réactif acide ou un très bon acide pour le titrage de solutions basiques de concentrations inconnues. Les acides forts sont utiles pour le titrage parce qu'ils donnent des points d'équivalence plus marqués, rendant les résultats plus précis. L'acide chlorhydrique est fréquemment utilisé en analyse chimique ou pour dissoudre des échantillons en vue d'analyse. Les solutions d'acide chlorhydrique concentrées peuvent dissoudre certains métaux en formant des chlorures d'oxydes métalliques et de l'hydrogène gazeux. Il est également utilisé comme catalyseur acide dans certaines réactions chimiques.
Propriétés physiques
Les propriétés physiques de l'acide chlorhydrique, telles que les points d'ébullition ou de fusion, dépendent de la concentration ou de la molarité d'HCl en solution aqueuse. Elles varient depuis les propriétés physiques de l'eau pour 0 % de HCl jusqu'à celles de l'acide chlorhydrique fumant pour des fractions supérieures à 40 % de HCl.
Les température et pression de référence pour les valeurs données dans la table sont 20 °C et 1 atmosphère (101 kPa).Pourcentage massique
(%)Concentration massique
(kg·m-3)Masse volumique
(kg/L)Molarité pH Viscosité
(mPa·s)Chaleur spécifique
(kJ·kg-1·K-1)Pression de vapeur
(Pa)Point d'ébullition
(°C)Point de fusion
(°C)10 104,80 1,048 2,87 M -0,5 1,16 3,47 0,527 103 -18 20 219,60 1,098 6,02 M -0,8 1,37 2,99 27,300 108 -59 30 344,70 1,149 9,45 M -1,0 1,70 2,60 1,410 90 -52 32 370,88 1,159 10,17 M -1,0 1,80 2,55 3,130 84 -43 34 397,46 1,169 10,90 M -1,0 1,90 2,50 6,733 71 -36 36 424,44 1,179 11,64 M -1,1 1,99 2,46 14,100 61 -30 38 451,82 1,189 12,39 M -1,1 2,10 2,43 28,000 48 -26 L'acide chlorhydrique en tant que mélange binaire de HCl et H2O possède un azéotrope en ébullition à 108,6 °C pour une fraction de 20,2 % HCl. En cristallisation, il possède quatre eutectiques pour former les cristaux de HCl·H2O (68 % HCl), HCl·2H2O (51 % HCl), HCl·3H2O (41 % HCl) et HCl·6H2O (25 % HCl) et de glace (0% HCl).
Production
Synthèse directe
La production à grande échelle d'acide chlorhydrique est presque toujours liée à d'autres productions industrielles de composés chimiques. Par exemple, dans la production de dichlore, une solution de sel (NaCl) est électrolysée pour produire le dichlore, ainsi que de la soude et du dihydrogène. Le dichlore gazeux peut être recombiné avec le dihydrogène, ce qui conduit à la production de chlorure d'hydrogène HCl gazeux pur. Cette réaction étant exothermique, l'installation est appelée four à HCl.
-
- Cl2 (g) + H2 (g) → 2HCl(g)
Le chlorure d'hydrogène formé est dissous dans de l'eau distillée, ce qui permet de produire de l'acide chlorhydrique pur.
Synthèse organique
La majeure partie de la production d'acide chlorhydrique est intégrée dans des installations de production de composés organiques chlorés ou fluorés, par exemple le téflon, le fréon ou d'autres CFC, le chlorure d'acyle dérivé de l'acide acétique ou le PVC. Il s'agit souvent d'une production intégrée, avec une réutilisation directe sur le site. Au cours de la réaction chimique, des atomes d'hydrogène des composés organiques de départ sont remplacés par des atomes de chlore issus du dichlore, tandis que les atomes d'hydrogène ainsi libérés se recombinent avec le second atome de la molécule de dichlore conduisant à la formation de chlorure d'hydrogène.
La fluoration est ensuite une réaction au cours de laquelle l'atome de chlore est substitué par un atome de fluor, ce qui conduit de nouveau à la formation de chlorure d'hydrogène.
Le chlorure d'hydrogène gazeux obtenu est soit réutilisé directement, soit dissous dans de l'eau pour former de l'acide chlorhydrique.
Marché industriel
L'acide chlorhydrique est produit en solution jusqu'à des concentrations de 38 % HCl. Des concentrations plus élevées sont possibles d'un point de vue chimique, mais l'évaporation est alors importante et tant le stockage que la manipulation demandent des précautions supplémentaires, telles des températures basses ou une mise sous pression. Les solutions produites pour l'industrie ont donc des concentrations voisines de 30 % à 34 % HCl, optimisées pour le transport de manière à limiter les pertes par évaporation. Les solutions pour un usage domestique (principalement dans les produits d'entretien) ont généralement des concentrations de l'ordre de 10 % à 12 % HCl, pour lesquelles il est toutefois recommandé de diluer de nouveau avant utilisation.
Les principaux fabricants d'acide chlorhydrique dans le monde sont notamment Dow Chemical avec 2 millions de tonnes par an, ainsi que Formosa plastics, Georgia gulf corporation, Tosoh corporation, Akzo Nobel et Tessenderlo avec des productions comprises entre 0,5 et 1,5 millions de tonnes par an. La production mondiale totale est estimée à 20 millions de tonnes par an, dont environ 3 millions de tonnes par synthèse directe et le complément comme produit secondaire de réactions organiques. La plus grande partie de la production est utilisée directement par le producteur : le marché mondial « externe » est estimé à 5 millions de tonnes par an.
Utilisations
L'acide chlorhydrique est un acide inorganique fort, utilisé dans un grand nombre de procédés industriels. La qualité du produit utilisé dépend généralement de l'application envisagée.
Productions de composés organiques
La majeure partie de l'acide chlorhydrique est utilisée pour la production de composés organiques tels que le chlorure de vinyle pour le PVC ou le 4,4'-MDI/Diisocyanate de toluène pour le polyuréthane. Cette utilisation fonctionne fréquemment sur un mode captif, c'est-à-dire avec une utilisation d'acide chlorhydrique fabriqué localement. Parmi les autres composés organiques dont la fabrication nécessite de l'acide chlorhydrique, on peut citer le bisphénol A pour les polycarbonates, le charbon actif et l'acide ascorbique (vitamine C), ainsi que de nombreux produits pharmaceutiques.
Régénération d'échangeurs d'ions
Une utilisation importante de l'acide chlorhydrique de haute qualité est la régénération de résines échangeuses d'ions. L'échange de cations est couramment utilisé pour retirer des ions dont notamment Na+ ou Ca2+ de solutions aqueuses pour produire de l'eau déminéralisée :
-
- Na + est remplacé par H3O +
- Ca2 + est remplacé par 2H3O +
Les résines échangeuses d'ions et l'eau déminéralisée ainsi obtenue sont très utilisées dans l'industrie chimique, la production d'eau potable ou l'industrie agroalimentaire.
Neutralisation et contrôle du pH
L'acide chlorhydrique est couramment utilisé pour réguler l'acidité (pH) de solutions :
-
- OH-(aq) + (H3O+ + Cl-(aq)) → 2H2O(l) + Cl-(aq)
Dans les industries nécessitant une pureté élevée (industrie pharmaceutique, agroalimentaire, ou de production d'eau potable), le contrôle du pH de l'eau utilisée dans les procédés est effectué avec de l'acide chlorhydrique de haute qualité. Dans les industries moins sensibles, de l'acide chlorhydrique de qualité technique est utilisé pour neutraliser l'eau rejetée, ou pour les traitements de piscines.
Décapage des aciers
Le décapage est une étape essentielle dans le traitement de surface d'un métal, le plus souvent du fer ou de l'acier, pour retirer la couche d'oxyde avant de lui faire subir une extrusion, une galvanisation ou tout autre procédé. Le réactif le plus couramment utilisé pour le décapage des aciers carbone est l'acide chlorhydrique de qualité technique, de concentration généralement voisine de 18% HCl.
-
- Fe2O3 (s) + Fe(s) + 6 (H3O+ + Cl-(aq)) → 3 (Fe2+(aq) + 2Cl-(aq)) + 9 H2O(l)
Le produit de la réaction a longtemps été réutilisé en tant que solution de chlorure de fer (II), mais les concentrations importantes de métaux lourds tendent à faire disparaître cette utilisation.
L'industrie métallurgique a développé dans les dernières années un procédé de régénération de l'acide chlorhydrique permettant de récupérer l'acide utilisé lors du décapage. L'un des procédé de régénération les plus courants est le procédé Dependeg :
-
- 4 (Fe2+(aq) + 2Cl-(aq)) + 12 H2O(l) + O2 (g) → 8 (H3O+ + Cl-(aq)) + 2 Fe2O3 (s)
De cette manière, l'acide chlorhydrique est utilisé en circuit fermé. L'oxyde de fer produit par le procédé de régénération constitue par ailleurs un produit secondaire valorisable dans l'industrie.
L'acide chlorhydrique n'est pas un réactif de décapage couramment utilisé dans le cas des aciers inoxydables (on utilise plutôt des solutions à base d'acide fluorhydrique).
Production de composés inorganiques
L'acide chlorhydrique peut être utilisé pour produire un grand nombre de composés inorganiques au cours de réactions de type acido-basique, notamment des produits de traitement de l'eau tels que le chlorure de fer (III) ou le chlorure d'aluminium .
-
- Fe2O3 (s) + 6 (H3O+ + Cl-(aq)) → 2 (Fe3+(aq) + 3Cl-(aq)) + 9 H2O(l)
Le chlorure de fer (III) et le chlorure d'aluminium sont utilisés comme agents coagulant ou floculant dans des traitements d'effluents, la production d'eau potable ou la production de papier.
Parmi d'autres composés inorganiques produits avec de l'acide chlorhydrique, on peut citer le chlorure de calcium (CaCl2) pour le salage des routes, le chlorure de nickel (II) (NiCl2) pour l'électrodéposition, ou le chlorure de zinc (ZnCl2) pour la galvanisation ou la production de batteries.
Autres utilisations
L'acide chlorhydrique est une espèce chimique fondamentale utilisée également dans un grand nombre d'applications à petite échelle, telles que le traitement du cuir ou la construction, ou en tant que nettoyant domestique. De plus, la production de pétrole peut être facilitée en injectant de l'acide chlorhydrique dans les formations rocheuses constituant le puits de pétrole, ce qui permet de dissoudre une partie de la roche et de former une structure poreuse. L'acidification est un procédé couramment utilisé pour la production pétrolière en mer du Nord.
De nombreuses transformations chimiques mettant en œuvre de l'acide chlorhydrique sont également utilisées pour la production d'ingrédients alimentaires ou d'additifs alimentaires. On peut notamment citer l'aspartame, le fructose, l'acide citrique, la lysine, les protéines hydrolysées et la gélatine. L'acide chlorhydrique utilisé est alors de qualité extra-pure.
L'acide chlorhydrique et les organismes vivants
Physiologie
L'acide chlorhydrique est le principal constituant des acides gastriques. Il est donc présent dans l'estomac où il contribue à la digestion des aliments. Il est sécrété par les cellules pariétales (également connues sous le nom de cellules oxyntiques) au cours d'un mécanisme complexe mettant en jeu une importante quantité d'énergie. Ces cellules contiennent un réseau de sécrétion important (appelé canaliculi), depuis lequel l'acide chlorhydrique est sécrété dans l'estomac. Elles font partie des glandes épithéliales de l'estomac.
Pathophysiologie et pathologie
Les mécanismes qui préviennent les dommages de l'épithélium digestif par l'acide chlorhydrique sont les suivants :
- une rétroaction négative des sécrétions d'acide
- une fine couche de mucus couvrant l'épithélium gastrique
- la sécrétion de bicarbonate de sodium par les cellules épithéliales de l'estomac et du pancréas
- la structure même de l'épithélium gastrique
- un afflux sanguin adéquat
- les prostaglandines (elles stimulent les sécrétions de mucus et de bicarbonate, maintiennent l'intégrité de la barrière épithéliale, permettent l'afflux sanguin adéquat et stimulent la réparation des membranes muqueuses endommagées)
Lorsque ces mécanismes de protections ne fonctionnent pas, il peut se développer des brûlures d'estomac (ou ulcère). Des médicaments appelés inhibiteur de la pompe à protons permettent d'empêcher la production excessive d'acide dans l'estomac, tandis que des antiacides permettent de neutraliser les acides présents.
Dans certains cas, la production d'acide chlorhydrique dans l'estomac peut être insuffisante. Cet état pathologique est connu sous le nom d'achlorhydrie (ou hypochlorhydrie). Il peut potentiellement conduire à des gastro-entérites.
Armes chimiques
Au cours de la Première Guerre mondiale, le phosgène (COCl2) était une arme chimique couramment utilisée. Le principal effet du phosgène résulte de la dissolution du gaz dans les membranes muqueuses des poumons où il est convertit par hydrolyse en acide carbonique et en acide chlorhydrique. Celui-ci contribue à rompre les membranes alvéolaires et les poumons se remplissent de fluide (œdème pulmonaire).
L'acide chlorhydrique est également en partie responsable des effets du gaz moutarde. En présence d'eau, par exemple à la surface des yeux ou dans les poumons, le gaz moutarde réagit en formant de l'acide chlorhydrique.
Sécurité
Toxicité
L'acide chlorhydrique fortement concentré forme des vapeurs acides. Ces vapeurs et la solution d'acide ont toutes deux un effet corrosif sur les tissus humains, et peuvent endommager les organes respiratoires, les yeux, la peau et les intestins. Le dichlore, un gaz très toxique, est produit lorsque l'acide chlorhydrique est mélangé avec des produits chimiques oxydants courants tels que l'eau de Javel (Na+(aq) + ClO-(aq)) ou le permanganate de potassium (KMnO4). Pour minimiser les risques lors de l'utilisation d'acide chlorhydrique, il convient de prendre les précautions appropriées. Par exemple, il ne faut jamais ajouter de l'eau dans l'acide : pour éviter les projections de gouttelettes acides, il convient d'ajouter l'acide dans l'eau. Il est également recommandé de toujours porter des lunettes de sécurité et des gants.
Voir aussi
Notes et références
- ↑ a et b Entrée de « Hydrochloric acid solution » dans la base de données de produits chimiques GESTIS de la BGIA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 5 juillet 2009 (JavaScript nécessaire)
- ↑ IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme » sur http://monographs.iarc.fr, 16 janvier 2009, CIRC. Consulté le 22 août 2009
- ↑ Jâbir Ibn Hayyân - Un grand chimiste, consulté le 7 mai 2008
Sources
- Chemicals Economics Handbook, Hydrochloric Acid, SRI International, 2001, p. 733.4000A-733.3003F
- Van Dorst, W.C.A., et al., technical product brochure Hydrochloric Acid, Akzo Nobel Base Chemicals, 2004 (public document)
- Van Dorst, W.C.A., various technical papers, Akzo Nobel Base Chemicals, 1996-2002 (not for open publication)
- Lide, David, NIST, CRC Handbook of Chemistry and Physics, CRC Press, 61st edition, 1980-1981
- Aspen Technology, Aspen Properties, binary mixtures modelling software, calculations by Akzo Nobel Engineering, 2002-2003
- Evison D, Hinsley D, Rice P. Chemical weapons. 2002;324(7333):332-5. PMID 11834561
- Arthur C., M.D. Guyton, John E. Hall, Textbook of Medical Physiology, W.B. Saunders Company; 10th edition (August 15, 2000), ISBN 072168677X
Liens externes
- (fr)Fiche toxicologique de l’INRS
- (fr) Densités des solutions d'acide chlorhydrique (HCl aq) dans les CSTP de 0,36% à 40% en masse
- Portail de la chimie
Catégories : Produit chimique corrosif | Article de qualité | Acide halohydrique -
Wikimedia Foundation. 2010.