- Acier
-

Cet article est lié aux
composés du fer et du carbonePhases - Austénite
- Bainite
- Carbure de fer
- Cémentite
- Ferrite
- Graphite
- Lédéburite
- Martensite
- Perlite
Acier Autre produits ferreux L’acier est un alliage métallique utilisé dans les domaines de la construction métallique (voir aussi l’article sur la théorie du soudage de l’acier) et de la construction mécanique.
L’acier est constitué d’au moins deux éléments, le fer, très majoritaire, et le carbone, dans des proportions comprises entre 0,02 % et 2 % en masse[1].
C’est essentiellement la teneur en carbone qui confère à l’alliage les propriétés du métal qu’on appelle « acier ». Il existe d’autres métaux à base de fer qui ne sont pas des aciers comme les fontes et les ferronickels par exemple.
Constitution des aciers
Les aciers sont élaborés pour résister à des sollicitations mécaniques ou des agressions chimiques ou une combinaison des deux.
Pour résister à ces sollicitations et/ou agressions, des éléments chimiques peuvent être ajoutés en plus du carbone. Ces éléments sont appelés éléments d’additions, les principaux sont le manganèse (Mn), le chrome (Cr), le nickel (Ni), le molybdène (Mo).
Les éléments chimiques présents dans l’acier peuvent être classés en 3 catégories :
- Les impuretés, originellement présentes dans les ingrédients de haut fourneau qui serviront à produire la fonte qui servira à fabriquer l’acier. Ce sont le soufre (S) et le phosphore (P) présent dans le coke mais aussi le plomb (Pb) et l’étain (Sn) qui peuvent être présents dans les aciers de récupération ainsi que nombre d’autres éléments à bas point de fusion comme l’arsenic (As), l’antimoine (Sb) ;
- Les éléments d’addition mentionnés plus haut et qui sont ajoutés de manière intentionnelle pour conférer au matériau les propriétés recherchées, et enfin ;
- Les éléments d’accompagnement que l’aciériste utilise en vue de maîtriser les diverses réactions physico-chimiques nécessaires pour obtenir en final un acier conforme à la spécification. C’est le cas d’éléments comme l’aluminium, le silicium, le calcium.
Aperçu de la composition, des avantages et des inconvénients
La teneur en carbone a une influence considérable (et assez complexe) sur les propriétés de l’acier : en dessous de 0,008 %, l’alliage est plutôt malléable et on parle de « fer » ; au-delà de 2,1 %[2], on entre dans le domaine de l'eutectique fer/carbure de fer ou bien fer/graphite, ce qui modifie profondément la température de fusion et les propriétés mécaniques de l'alliage, et l'on parle de fonte.
Entre ces deux valeurs, l’augmentation de la teneur en carbone a tendance à améliorer la dureté de l’alliage et à diminuer son allongement à la rupture ; on parle d’aciers « doux, mi-doux, mi-durs, durs ou extra-durs » (classification traditionnelle).
Dans les manuels de métallurgie un peu anciens, on peut trouver comme définition de l'acier un alliage fer-carbone où le carbone varie de 0,2 à 1,7 % ; la limite actuelle a été établie à partir du diagramme binaire fer/carbone. Toutefois, il y a des aciers avec des concentrations de carbone supérieures à ces limites (acier lédéburitiques), obtenus par frittage.
On modifie également les propriétés des aciers en ajoutant d’autres éléments, principalement métalliques, et on parle d’aciers alliés. De plus, on peut encore améliorer grandement leurs caractéristiques par des traitements thermiques (notamment les trempes ou la cémentation) prenant en surface ou à cœur de la matière ; on parle alors d’aciers traités.
Outre ces diverses potentialités, et comparativement aux autres alliages métalliques, l’intérêt majeur des aciers réside d’une part dans le cumul de valeurs élevées dans les propriétés mécaniques fondamentales :
- raideur, résistance à la déformation élastique : module d’élasticité E ;
- dureté, résistance à la déformation irréversible, à la rupture : limite élastique Re, résistance minimale à la rupture Rm, dureté H ;
- résistance aux chocs : résilience K.
D’autre part, leur coût d’élaboration reste relativement modéré, car le minerai de fer est abondant sur terre (environ 5 % de l’écorce) et sa réduction assez simple (par addition de carbone à haute température). Enfin les aciers sont pratiquement entièrement recyclables grâce à la filière ferraille.
On peut néanmoins leur reconnaître quelques inconvénients, notamment leur mauvaise résistance à la corrosion à laquelle on peut toutefois remédier, soit par divers traitements de surface (peinture, brunissage, zingage, galvanisation à chaud, etc.), soit par l’utilisation de nuances d’acier dites « inoxydables ». Par ailleurs, les aciers sont difficilement moulables, donc peu recommandés pour les pièces volumineuses de formes complexes (bâtis de machines, par exemple). On leur préfère alors des fontes. Enfin, lorsque leur grande masse volumique est pénalisante (dans le secteur aéronautique par exemple), on se tourne vers des matériaux plus légers (alliages à base d’aluminium, titane,composites, etc.), qui ont l’inconvénient d’être plus chers.
De ce fait, les aciers restent privilégiés dans presque tous les domaines d’application technique : équipements publics (ponts et chaussées, signalisation), industrie chimique, pétrochimique, pharmaceutique et nucléaire (équipements sous pression, équipements soumis à l’action de la flamme, capacités de stockage, récipients divers), agro-alimentaire (conditionnement et stockage), bâtiment (armatures, charpentes, ferronnerie, quincaillerie), industrie mécanique et thermique (moteurs, turbines, compresseurs), automobile (carrosserie, équipements), ferroviaire, aéronautique et aérospatial, construction navale, médical (instruments, appareils et prothèses), composants mécaniques (visserie, ressorts, câbles, roulements, engrenages), outillage de frappe (marteaux, burins, matrices) et de coupe (fraises, forets, porte-plaquette), mobilier, design et équipements électroménagers, etc.
Histoire de l'acier
Article détaillé : Histoire de la production de l’acier. Fabrication d’acier au Moyen Âge dans un bas-fourneau.
Fabrication d’acier au Moyen Âge dans un bas-fourneau.
Depuis l’Âge du fer, on utilisait les bas fourneaux pour produire des massiots composés de fer et d’acier, qui devaient ensuite être travaillés à la main par les forgerons. La coulée de la fonte dans les hauts fourneaux et l'affinage à l'air pour obtenir de l'acier a été découvert par les chinois durant la période des Royaumes combattants (entre -453 et -221). En Europe et en Asie, durant l'Antiquité, on produisait également de l'acier en laissant le fer dans des gaz de combustion (cémentation).
On considère souvent Réaumur comme le fondateur de la sidérurgie scientifique moderne. En effet, il réalisa de très nombreuses expériences afin d’améliorer la fabrication de l’acier et publia les résultats de ses observations en 1712.
L’acier industriel est apparu, avec l’évolution de la métallurgie, vers 1786. Cette année-là, trois savants français, Berthollet, Monge et Vandermonde[3], caractérisèrent trois types de produits obtenus à partir de la coulée des hauts-fourneaux : le fer, la fonte et l’acier. L’acier était alors obtenu à partir du fer, lui-même produit par affinage de la fonte issue du haut-fourneau. L’acier était plus dur que le fer et moins fragile que la fonte. La méthode était identique à la méthode chinoise, mais a bénéficié d'un développement important en raison de la forte demande liée à la révolution industrielle.
Au XIXe siècle sont apparues des méthodes de fabrication avec conversion directe de la fonte, avec les convertisseurs Bessemer en 1856 (Henry Bessemer); le procédé Thomas-Gilchrist de déphosphoration de la fonte en 1877 (Sidney Gilchrist Thomas et Percy Carlyle Gilchrist) et la méthode Siemens-Martin. Ces découvertes, permettant la fabrication en masse d’un acier de « qualité » (pour l’époque), participent à la Révolution industrielle. Enfin, vers la seconde moitié du XIXe siècle, Dmitry Chernov découvre les transformations polymorphes de l’acier et établit le diagramme binaire fer/carbone, faisant passer la métallurgie de l’état d’artisanat à celui de science.
Fabrication de l'acier
Article détaillé : Fabrication de l’acier.Composition et structure des aciers
Teneur en carbone
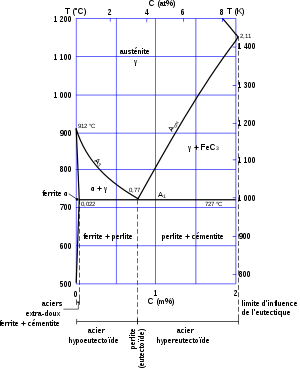
On distingue plusieurs types d’aciers selon le pourcentage massique de carbone qu’ils contiennent :
- les aciers hypoeutectoïdes (de 0,0101 à 0,77 % de carbone) qui sont les plus malléables ;
- les aciers extra-doux ont une teneur inférieure à 0,022 % de carbone ; ils sont hors de la « zone d’influence » de l’eutectoïde (perlite) et n’ont donc pas de perlite ; ils sont durcis par des précipités de cémentite en faible quantité ;
- entre 0,022 et 0,77 % de carbone, la cémentite est présente dans la perlite mais n’existe pas sous forme « seule » ;
- l’acier eutectoïde (0,77 % de carbone) appelé perlite ;
- les aciers hypereutectoïdes (de 0,77 à 2,11 % de carbone) qui sont les plus durs et ne sont pas réputés soudables.
La limite de 2,11 % correspond à la zone d’influence de l’eutectique (lédéburite) ; il existe toutefois des aciers lédéburitiques.
La structure cristalline des aciers à l’équilibre thermodynamique dépend de leur concentration (essentiellement en carbone mais aussi d’autres éléments d’alliage), et de la température. On peut aussi avoir des structures hors équilibre (par exemple dans le cas d’une trempe).
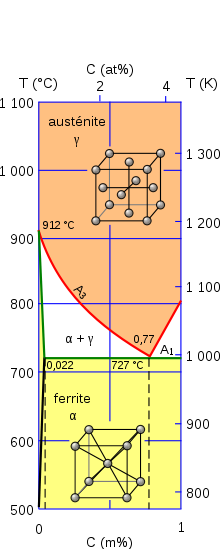
La structure du fer pur dépend de la température :
- jusqu’à 912 °C, le fer (fer α) a une structure cristalline cubique centrée appelée ferrite
- entre 912 °C et 1 394 °C, le fer (fer γ) a une structure cristalline cubique à faces centrées appelée austénite
- entre 1 394 °C et jusqu’à son point de fusion à 1 538 °C, le fer (fer δ) retrouve une structure cristalline cubique centrée appelée ferrite delta (cette ferrite joue un rôle essentiel dans la mise en œuvre et surtout le soudage des aciers duplex).
La structure du fer + carbone évolue d’une façon plus complexe en fonction de la température et de la teneur en carbone. Les règles diffèrent selon que l’on est hors de la « zone d’influence » de l’eutectoïde (entre 0 % et 0,022 %), entre 0,022 % et 0,77 % (hypoeutectoïde) ou entre 0,77 % et 2,11 % (hypereutectoïde ; au-delà, il s’agit de fonte). Voir l’étude du diagramme fer-carbone.
D’une manière simplifiée, pour un carbone compris entre 0,022 % et 2,11 % :
- jusqu’à 727 °C on trouve un mélange de ferrite et de cémentite ;
- à partir de 727 °C le fer α se transforme en fer γ (changement de phase appelé austénitisation) ; La température de fin de transformation dépend de la teneur en carbone.
Les aciers non alliés (au carbone) peuvent contenir jusqu’à 2,11 % en masse de carbone. Certains aciers alliés peuvent contenir plus de carbone par l’ajout d’éléments dits « gammagènes ».
Les différentes phases de l’acier Austénite • Bainite • Cémentite • Ferrite • Martensite • Perlite
Éléments d'alliage
Le carbone a une importance primordiale car c'est lui qui, associé au fer, confère à l'alliage le nom d'acier. Son influence sur les propriétés mécaniques de l'acier est prépondérante. Par exemple, en ce qui concerne l'amélioration de la propriété de dureté, l'addition de carbone est trente fois plus efficace que l'addition de manganèse.
L’aluminium : excellent désoxydant. Associé à l’oxygène, réduit la croissance du grain en phase austénitique. Peut rendre l’acier inapte à la galvanisation à chaud.
Le chrome : c’est l’élément d’addition qui confère à l’acier la propriété de résistance mécanique à chaud et à l’oxydation (aciers réfractaires). Il joue aussi un rôle déterminant dans la résistance à la corrosion lorsqu’il est présent à une teneur de plus de 12 à 13 % (selon la teneur en carbone). Additionné de 0,5% à 9% il augmente la trempabilité (famille des aciers au chrome). Il a un rôle alphagène.
Le cobalt : utilisé dans de nombreux alliages magnétiques. Provoque une résistance à l’adoucissement lors du revenu.
Le manganèse : forme des sulfures qui améliorent l’usinabilité. Augmente modérément la trempabilité.
Le molybdène : augmente la température de surchauffe, la résistance à haute température et la résistance au fluage. Augmente la trempabilité.
Le nickel : rend austénitiques (role gammagène) les aciers à forte teneur en chrome. Sert à produire des aciers de trempabilité modérée ou élevée (selon les autres éléments présents), à basse température d’austénitisation et à ténacité élevée après traitement de revenu. C’est l’élément d’alliage par excellence pour l'élaboration des aciers ductiles à basses températures (acier à 9% Ni pour la construction des réservoirs cryogéniques, acier à 36%Ni dit INVAR pour la construction des cuves de méthaniers).
Le niobium : même avantage que le titane mais beaucoup moins volatil. Dans le domaine du soudage il le remplace donc dans les métaux d’apport.
Le phosphore : augmente fortement la trempabilité. Augmente la résistance à la corrosion. Peut contribuer à la fragilité de revenu.
Le silicium : favorise l’orientation cristalline requise pour la fabrication d’un acier magnétique, augmente la résistivité électrique. Améliore la résistance à l’oxydation de certains aciers réfractaires. Utilisé comme élément désoxydant.
Le titane : pouvoir carburigène élevé (comme le niobium) et réduit donc la dureté de la martensite. Élimine le carbone en solution à haute température et réduit le risque de corrosion intergranulaire (TiC se forme avant Cr23C6 évite donc l’appauvrissement en chrome au joint de grain).
Le tungstène : améliore la dureté à haute température des aciers trempés revenus. Fonctions sensiblement identiques à celles du molybdène.
Le vanadium : augmente la trempabilité. Élève la température de surchauffe. Provoque une résistance à l’adoucissement par revenu (effet de durcissement secondaire marqué).
Structure des aciers
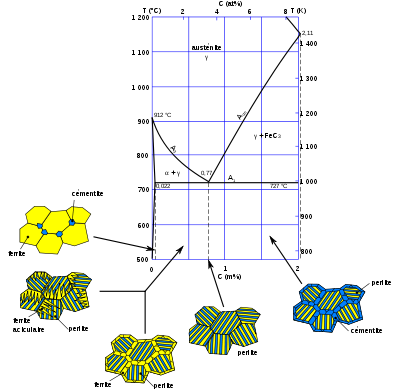
Lors du refroidissement d’un lingot, l’acier se solidifie à l’état austénitique. Au cours du refroidissement, à 727 °C, l’austénite se décompose, soit en ferrite + perlite, soit en perlite + cémentite. La vitesse de refroidissement ainsi que les éléments d’alliage ont une importance capitale sur la structure obtenue, et donc sur les propriétés de l’acier. En effet :
- les joints de grain bloquent les dislocations, donc augmentent la dureté et la limite élastique ; or, plus les grains sont petits, plus il y a de joints de grain…
- la cémentite est un carbure, une céramique très dure ; sa présence augmente la dureté et la limite élastique, mais diminue la ductilité.
De manière générale :
- un refroidissement rapide donne de petits grains, alors qu’un refroidissement lent donne de gros grains ;
- la réorganisation des atomes pour passer de la structure austénitique (cubique à faces centrées) à la structure ferritique (cubique centrée) se fait par des mouvements d’atomes de faible ampleur (quelques distances interatomiques) ;
- la ferrite pouvant contenir moins de carbone dissout (voir Solution solide et Site interstitiel), le carbone doit migrer sur de plus grandes distances pour former de la cémentite ; la distance à parcourir est moins grande dans le cas de la perlite (eutectoïde), puisque la cémentite s’intercale entre des « tranches » de ferrite ;
- la germination des nouveaux cristaux se fait de manière préférentielle aux défauts, et notamment aux joints de grain de l’austénite ; ainsi, la structure de solidification de l’austénite joue un rôle important (voir Solidification).
Certains éléments chimiques peuvent « piéger » le carbone pour former des carbures (par exemple le titane ou l’aluminium). Ils empêchent ainsi la formation de cémentite.
On peut modifier la structure de l’acier par des traitements thermomécaniques :
- déformations : écrasement du lingot, laminage à froid ou à chaud, forgeage…
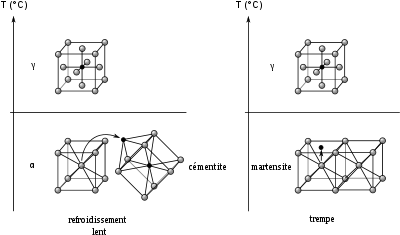
- traitements thermiques, qui permettent de « rejouer » le refroidissement :
- trempe, éventuellement suivie d’un revenu : la rapidité de la transformation ne permet pas au carbone de diffuser et le « piège » dans la maille cubique centrée, qui se déforme pour donner de la martensite ; les cristaux forment de petites aiguilles ;
- une trempe plus lente, ou bien une trempe étagée, permet la formation de bainite ;
- recuit, permettant la diffusion des éléments, la réorganisation des atomes et l’élimination des dislocations.
La métallurgie des poudres consiste à compacter de la poudre d’acier et de la chauffer en dessous de la température de fusion, mais suffisamment pour que les grains se « soudent » (frittage). Cela permet de maîtriser la structure de l’acier et son état de surface (en particulier pas de retrait ni de retassure[Quoi ?]), mais introduit de la porosité.
Différentes « familles » d'aciers
Il existe des aciers faiblement alliés, à faible teneur en carbone, et au contraire des aciers contenant beaucoup d’éléments d’alliage (par exemple, un acier inoxydable typique contient 8 % de nickel et 18 % de chrome en masse).
Différentes classifications
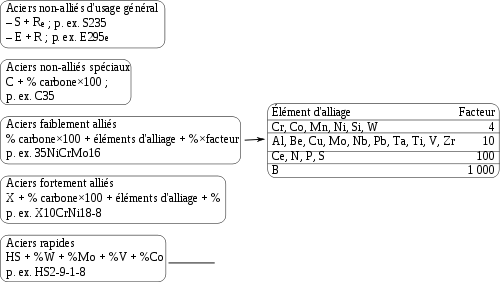
Article détaillé : Désignation normalisée des aciers.Chaque pays a son mode de désignation des aciers. Le schéma ci-contre indique la désignation européenne selon la norme EN10027. Cette norme distingue quatre catégories :
- les aciers non-alliés d’usage général (construction) ;
- les aciers non-alliés spéciaux, pour traitement thermique, malléables, soudables, forgeables… ;
- les aciers faiblement alliés, pour trempe et revenu ; les éléments d’alliage favorisent la trempabilité et permettent d’avoir des structures martensitiques ou bainitiques, donc des aciers à haute dureté, à haute limite élastique, pour les outils, les ressorts, les roulements…
- les aciers fortement alliés :
- les aciers inoxydables,
- les aciers rapides, pour les outils à forte vitesse de coupe comme les forets.
Aciers non alliés
Aciers non alliés d’usage général
Ils sont destinés à la construction soudée, à l’usinage, au pliage… On distingue :
- Le type S qui correspond à un usage général de base (construction de bâtiment…)
- Le type E qui est utilisé dans la construction mécanique
La désignation de ces aciers comprend la lettre du type d’acier suivi de la valeur de la limite élastique (Re) en méga-pascal (MPa). S’il s’agit d’un acier moulé, la désignation est précédée de la lettre G. La désignation peut être complétée par des indications supplémentaires (pureté, application dédiée…)
Exemples :
- S185 (anciennement A33), Re = 185 MPa
- E295 (anciennement A50), Re = 295 MPa
- GE295, acier moulé, Re = 295 MPa
- S355 J2 WP, Re = 355 MPa, à grain fin et auto-patinable (c’est l’acier Corten A)
Aciers non alliés spéciaux (type C)
Leur composition est plus précise et plus pure et correspond à des usages définis à l’avance.
Leurs applications courantes sont les forets (perceuses), ressorts, arbres de transmission, matrices (moules)…
Leur désignation comprend la lettre C suivie de la teneur en carbone multipliée par 100. S’il s’agit d’un acier moulé, on précède la désignation de la lettre G. Exemples :
- C45, acier non allié comportant un taux de 0,45 % de carbone ;
- GC22, acier moulé non allié comportant un taux de 0,22 % de carbone.
Aciers faiblement alliés
Aucun élément d’addition ne dépassant 5 % en masse, ils sont utilisés pour des applications nécessitant une haute résistance.
Exemples de désignation normalisée :
- 35NiCrMo16 : contient 0,35 % de carbone, 4 % de nickel, du chrome et molybdène en plus faible teneur. Cet acier présente une bonne tenue aux chocs ainsi qu’une haute résistance mécanique jusque 600 °C ;
- 100Cr6 : 1 % de carbone et 1,5 % de Chrome. C’est l’acier typique utilisé dans les roulements à billes.
Aciers fortement alliés
Au moins un élément d’addition dépasse les 5 % en masse, destinés à des usages bien spécifiques, on y trouve des aciers à outils, réfractaires, maraging (très haute résistance, utilisés dans l’aéronautique), Hadfields (très grande résistance à l’usure), Invar (faible coefficient de dilatation)
Un exemple de désignation normalisée : X2CrNi18-9 (c’est un acier inoxydable).
Les aciers rapides spéciaux (ARS, ou high speed steels, HSS) font partie de cette famille.
Aciers inoxydables
Ces aciers présentent une grande résistance à la corrosion, à l’oxydation à chaud et au fluage (déformation irréversible). Ils sont essentiellement alliés au chrome, élément qui confère la propriété d’inoxydabilité, et au nickel, élément qui confère de bonnes propriétés mécaniques. Les aciers inoxydables sont classés en quatre familles : ferritique, austénitique, martensitique et austéno-ferritique. Les aciers inoxydables austénitiques sont les plus malléables et conservent cette propriété à très basse température (-200 °C).
Leurs applications sont multiples : chimie, nucléaire, alimentaire, mais aussi coutellerie et équipements ménagers. Ces aciers contiennent au moins 10,5 % de chrome et moins de 0,12 % de carbone.
Aciers multiphasés
Ces aciers sont conçus suivant les principe des composites : par des traitements thermiques et mécaniques, on parvient à enrichir localement la matière de certains éléments d’alliage. On obtient alors un mélange de phases dures et de phases ductiles, dont la combinaison permet l’obtention de meilleures caractéristiques mécaniques. On citera, par exemple :
- les aciers Dual Phase qui sont la déclinaison moderne de l’acier damassé, mais où la distinction entre phase dure (la martensite) et phase ductile (la ferrite), se fait plus finement, au niveau du grain ;
- Les aciers duplex formés de ferrite et d’austénite dans des proportions sensiblement identiques ;
- les aciers TRIP (TRansformation Induced Plasticity), où l'austénite se transforme partiellement en martensite après une sollicitation mécanique. On débute donc avec un acier ductile, pour aboutir à un acier de type Dual Phase.
- les aciers damassés où des couches blanches ductiles pauvres en carbone absorbent les chocs, et les noires, plus riches en carbone, garantissent un bon tranchant perso.orange.fr ;
Propriétés et caractéristiques des aciers
L’acier est un alliage essentiellement composé de fer, sa densité varie donc autour de celle du fer (7,32 à 7,86), suivant sa composition chimique et ses traitements thermiques. La densité d’un acier inox austénitique est typiquement un peu supérieure à 8, en raison de la structure cristalline. Par exemple, la densité d’un acier inoxydable de type AISI 304 (X2CrNi18-10) est environ 8,02.
Ils ont un module de Young d’environ 210 000 MPa, indépendamment de leur composition. Les autres propriétés varient énormément en fonction de leur composition, du traitement thermo-mécanique et des traitements de surface auxquels ils ont été soumis.
Le traitement thermo-mécanique est l’association :
- d’un traitement thermique, sous la forme d’un cycle chauffage-refroidissement (trempe, revenu…) ;
- d’un traitement mécanique, une déformation provoquant de l’écrouissage (laminage, forgeage, tréfilage…).
Le traitement de surface consiste à modifier la composition chimique ou la structure d’une couche extérieur d’acier. Cela peut être :
- une réaction en phase liquide (chromatation, carburation, nitruration en bain de sel, galvanisation, parkerisation…) ;
- une réaction en phase gazeuse (nitruration en phase liquide) ;
- une projection d’ions (implantation ionique) ;
- un recouvrement (peinture, émail).
Voir aussi l’article détaillé traitements anti-usure.
Symbolique et expression
- L’acier est le 7e niveau dans la progression de la sarbacane sportive ;
- selon certaines sources, l’acier peut désigner le 11e anniversaire de mariage ;
- le terme « acier » sert à caractériser ce qui est solide, par exemple un moral d’acier ;
- le « poumon d’acier » désigne un ancien modèle de respirateur artificiel (respirateur à pression négative).
- Le gris acier[4] est une couleur[5] gris neutre reproduisant la couleur de l’alliage.
- La couleur acier, en héraldique[6], désigne le gris.
Soudabilité des aciers
La soudabilité des aciers est inversement proportionnelle à la teneur en carbone. Toutes les nuances d’acier n’ont pas la même aptitude au soudage et affichent des degrés de soudabilité différents (voir l’article sur le soudage). Certains aciers sont d’ailleurs intrinsèquement non soudables. Pour qu’un acier soit soudable il est primordial que les aciéristes se préoccupent de la soudabilité des aciers qu'ils produisent dès l’élaboration dans le souci d’optimiser la mise en œuvre ultérieure. À titre d’exemple, on signalera que le code ASME (American Society of Mechanical Engineer), dans son volume spécifique à la construction d’équipements sous pression, exige que l’attestation de conformité d’un acier utilisé ne serait-ce que comme pièce provisoire soudée à titre temporaire sur un ouvrage soumis au dit code mentionne sans ambiguïté la qualité d’« acier soudable ».
Ce qui influence le coût de production de l'acier
Sept facteurs au moins déterminent le coût de production d’un acier :
- La composition de l’acier selon sa teneur en éléments nobles (chrome, nickel, manganèse, cobalt…) et le niveau de pureté chimique (basse teneur en soufre, phosphore, éléments à bas point de fusion comme le plomb, l’arsenic, l’étain, le zinc…),
- Les exigences particulières liées à la règlementation (Directives, décrets, loi…) et les spécifications techniques des donneurs d’ordres,
- Les choix d’option(s) proposée(s) par des normes ou des standards internationaux comme ; par exemple des aptitudes au pliage, à l’emboutissage, à l’usinage ; et qui ont un coût,
- Les exigences dimensionnelles (tolérance de planéité, classe d’épaisseur…). On remarquera que chez les aciéristes, la densité de l’acier n’est pas une constante ! Par exemple, dans le cas de l’acier de construction, elle n’est pas égale à 7,85. Les aciéristes considèrent une densité de facturation différente de la densité physique tout simplement pour tenir compte du fait que le poids réel livré (pesé) est toujours supérieur au poids théorique (calculé) du produit commandé,
- Les examens et essais effectués sur échantillons prélevés sur coulée ou directement sur produit ainsi que le mode de réception du produit. Il existe 3 principaux modes de réception classés ci-après dans l’ordre de coût croissant :
- par le vendeur (la réception du produit est donc effectuée par la première partie),
- par l’acheteur (la réception du produit est effectuée par la seconde partie), et
- par une entité administrative extérieure (bureau de contrôle, compagnie d’assurance, ministère, association…) autre que le vendeur ou l’acheteur (la réception du produit est effectuée par ce que l’on appelle une tierce partie).
- Les exigences internes (et donc supplémentaires) requises par les procédés de fabrication de l’utilisateur (planéité, limitations de teneurs en éléments chimiques, marquage), et
- La loi de l’offre et de la demande qui conditionne bien sûr le prix du marché.
L’impact des 6 premières exigences peut avoir une incidence de quelques dizaines d’euros la tonne à plus de 50 % du prix de base (le prix de base étant le prix d'un acier standard conforme à la norme et sans option), d’où l’importance de consulter les aciéristes (qu’on appelle aussi « forges » ou « fonderies ») sur les bases d’une spécification technique en accord avec les exigences contractuelles. Le 7e point quant à lui n’a pas de limite rationnelle.
Notes et références
- Valeur supérieure de la teneur en carbone :
« Les alliages fer-carbone contenant plus de 2 % de carbone constituent les fontes. »
— Philibert et coll. , Métallurgie du minerai au matériau (Dunod, 2002), p. 660
« Les fontes sont des alliages de fer et de carbone en quantité supérieure à 2 %. »
— Hazard et coll. , Mémotech — Structures métalliques (Casteilla, 2000), p. 14
Cependant, les valeurs retenues varient selon les auteurs, entre 1,67 et 2,11 %, selon que l'on se base sur les teneurs habituellement utilisées par les fabricants ou les valeurs des diagrammes obtenus en laboratoire - Les sources diffèrent, nous avons donc retenu la valeur de 2,1% ; quoi qu'il en soit, cette valeur est théorique car on n'utilise dans la pratique aucun acier non allié avec une telle teneur en carbone. Pour le diagramme métastable fer/carbure de fer :
- (en) William F. Smith et Javad Hashemi, Foundations of Materials Science and Engineering, Boston, McGraw-Hill, 2006, 4e éd. (ISBN 978-0-07-295358-9) (LCCN 2005043865), p. 363 : 2,08 % ;
- J. Philibert, A. Vignes, Y. Bréchet, P. Combrade, Métallurgie, du minerai au matériau, Paris, Dunod, 2002, 2e éd. (ISBN 978-2-10-006313-0), p. 655 : 2,11 % ;
- (en) E. Paul Degarmo, J. T. Black et Ronald A. Kohser, Materials and Processes in Manufacturing, Hoboken, Wiley, 2003, 9e éd. (ISBN 978-0-471-65653-1), p. 75 : 2,11 % ;
- Michael F. Ashby et David Rayner Hunkin Jones, An introduction to microstructures, processing and design, Butterworth-Heinemann, 1992 : 2,14%.
- Science&Vie N° 1106 de novembre 2009, p.130-131
- Gris acier (couleur).
- Liste de couleurs.
- Couleurs héraldiques.
Voir aussi
Articles connexes
- Théorie du soudage
- ArcelorMittal, numéro un mondial de la sidérurgie
- Liste de producteurs d’acier
- Aciérie électrique
- Thyssen, grande famille allemande de l’acier
Liens externes
- Qu’est-ce que l’acier ?
- (fr)(nl) Infosteel (Centre information acier)
- Nuances d’acier
Bibliographie
- J. Barralis, G. Maeder, Précis de métallurgie, Paris, Afnor, Nathan, 1991, 4e éd. (ISBN 978-2-09-194017-5)
- J. Philibert, A. Vignes, Y. Bréchet, P. Combrade, Métallurgie, du minerai au matériau, Paris, Dunod, 2002, 2e éd. (ISBN 978-2-10-006313-0), p. 8-10, 150-186, 617-623, 651, 654-661, 681-700, 744-752
- J.-L. Fanchon, Guide des sciences et technologies industrielles, Paris, Afnor, Nathan, 2001 (ISBN 978-2-09-178761-9 et 2-12-494112-7) (OCLC 47854031), p. 161-166
Catégories :- Acier
- Construction métallique
Wikimedia Foundation. 2010.