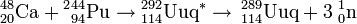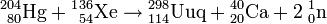- Élément 114
-
Ununquadium

Ununquadium 
Ununtrium ← Ununquadium → Ununpentium Pb
114Uuq ↑ Uuq ↓ Uhq Table complète • Table étendue Informations générales Nom, Symbole, Numéro Ununquadium, Uuq, 114 Série chimique métaux pauvres Groupe, Période, Bloc 14, 7, d Masse volumique ? kg/m3 Couleur ? N° CAS Propriétés atomiques Masse atomique 289 u Configuration électronique probablement
[Rn] 5f14 6d10 7s2 7p2
Électrons par niveau d'énergie 2, 8, 18, 32, 32, 18, 4 Propriétés physiques État ordinaire Présumé solide Divers 1e Énergie d'ionisation {{{potentiel_ionisation1}}} kJ/mol 2e Énergie d'ionisation {{{potentiel_ionisation2}}} kJ/mol 3e Énergie d'ionisation {{{potentiel_ionisation3}}} kJ/mol 4e Énergie d'ionisation {{{potentiel_ionisation4}}} kJ/mol 5e Énergie d'ionisation {{{potentiel_ionisation5}}} kJ/mol 6e Énergie d'ionisation {{{potentiel_ionisation6}}} kJ/mol 7e Énergie d'ionisation {{{potentiel_ionisation7}}} kJ/mol 8e Énergie d'ionisation {{{potentiel_ionisation8}}} kJ/mol 9e Énergie d'ionisation {{{potentiel_ionisation9}}} kJ/mol 10e Énergie d'ionisation {{{potentiel_ionisation10}}} kJ/mol Isotopes les plus stables iso AN Période MD Ed PD MeV 286Uuq {syn.} 0,13 s 60 % FS
40 % α—
10,19—
282Uub287Uuq {syn.} 0,48 s α 10,02 283Uub 288Uuq {syn.} 0,8 s α 9,94 284Uub 289Uuq {syn.} 2,6 s α 9,82
9,48285Uub Unités du SI & CNTP, sauf indication contraire. L'ununquadium est le nom provisoire attribué par l'UICPA à l'élément chimique de numéro atomique 114 (symbole provisoire Uuq), parfois encore appelé eka-plomb (« en-dessous du plomb » dans le tableau périodique des éléments) en référence à la désignation provisoire des éléments par Dmitri Mendeleïev avant qu'ils ne soient isolés et nommés, et généralement élément 114 dans la littérature scientifique.
Formellement classé dans la série des métaux pauvres, il n'aurait en fait aucunement des propriétés chimiques similaires à celles du plomb mais au contraire un comportement de gaz rare induit par une configuration électronique modifiée par des effets quantiques de couplage spin-orbite et d'électrodynamique quantique[1].
Selon la théorie MM (Microscopic-Macroscopic) décrivant le noyau atomique, son isotope 298Uuq, avec le « nombre magique » de 184 neutrons, pourrait être au centre d'un îlot de stabilité prédit par le modèle en couches de la structure nucléaire des atomes.
Sommaire
Synthèse
Une équipe de l'Institut unifié de recherches nucléaires (JINR) à Doubna en Russie a publié[2] en janvier 1999 avoir bombardé une cible de plutonium 244 avec des ions calcium 48, produisant un unique atome identifié comme du 289114 avec une désintégration α à 9,67 MeV en 30 s. Cette observation n'a toutefois pas pu être renouvelée, et on suppose qu'il pourrait s'agir d'un isomère métastable 289m114.
La même équipe a publié[3] en juillet 1999 avoir remplacé la cible de plutonium 244 par du plutonium 242 afin de produire d'autres isotopes et obtenu deux atomes de 287114 avec une désintégration α à 10,29 MeV en 5,5 s. Là encore, l'observation n'a pu être renouvelée, et on l'attribue à un possible isomère métastable 287m114.
La synthèse à présent confirmée des premiers noyaux d'ununquadium a été réalisée en juin 1999 lorsque la même équipe a repris l'expérience réalisée avec le plutonium 244 : deux atomes de l'élément 114 ont été à nouveau produits, avec une désintégration α à 9,82 MeV en 2,6 s[4]. Cette observation a été attribuée dans un premier temps à du 288114 en raison des observations précédentes, mais une analyse approfondie a permis de l'attribuer de façon certaine à du 289114[5].
La période radioactive théorique de la désintégration α des isotopes de l'élément 114 sont conformes aux observations[6],[7]. L'isotope 298Uuq aurait une période radioactive théorique de 17 jours[8],[9].
La synthèse du 283112, publiée en mai 2009[10], est venue confirmer indirectement les résultats obtenus précédemment sur le 287114 (ainsi que sur le 291116).
Propriétés
Des expériences assez complexes d'adsorption de l'ununquadium 287 sur de l'or ont été réalisée au printemps 2007 par des équipes du Flerov Laboratory for Nuclear Reactions (FLNR, au sein de l'Institut unifié de recherches nucléaires) et de l'Institut Paul Scherrer (PSI), qui ont suggéré un comportement en accord avec celui attendu pour un gaz rare volatile[11] ; ces résultats viennent appuyer des études théoriques indiquant que l'ununquadium pourrait avoir le comportement d'un gaz rare en raison d'effets relativistes dans son cortège électronique qui en modifieraient la configuration[1].
Îlot de stabilité : ununquadium 298
La théorie MM (Microscopic-Macroscopic) décrivant la structure nucléaire suggère de rechercher l'hypothétique « îlot de stabilité » autour du nucléide 298Uuq, qui serait « doublement magique » avec 114 protons et 184 neutrons. Cela pousse à créer des isotopes d'ununquadium plus riches en neutrons que ceux synthétisés jusqu'à présent, qui demeurent très instables et se désintègrent par fission spontanée (produisant une variété de radionucléides), désintégration α, émission de positon ou capture électronique (donnant de l'ununtrium). La difficulté est alors de trouver la combinaison de l'ion lourd et de la cible qui permettra de synthétiser un noyau comportant exactement 184 neutrons pour 114 protons : il faudrait par exemple utiliser des ions calcium 50 sur une cible plutonium 248 pour avoir le compte juste, ce qui n'est pas envisageable compte tenu de l'extrême difficulté à obtenir des quantités suffisantes de 50Ca et surtout de 248Pu. L'idée alternative serait alors de procéder à la quasi-fusion de noyaux massifs, en misant sur le caractère stabilisateur des couches nucléaires saturées qui tendrait à orienter les réactions nucléaires vers la production de noyaux « doublement sphériques », via par exemple la réaction :
dans laquelle les nucléides 298Uuq et 40Ca sont « doublement magiques » — du moins si 114 est bien un nombre magique de protons dans un noyau ayant 184 neutrons comme l'affirme la théorie MM.
Références
- ↑ a et b Gas Phase Chemistry of Superheavy Elements : Conférence de Heinz W. Gäggeler, Novembre 2007 — Page consultée le 07/07/2009.
- ↑ Oganessian et al., « Synthesis of Superheavy Nuclei in the 48Ca + 244Pu Reaction », dans Phys. Rev. Lett., vol. 83, 1999, p. 3154-3157(4). Lien direct consulté le 03/03/2008
- ↑ Oganessian et al., « Synthesis of nuclei of the superheavy element 114 in reactions induced by 48Ca », dans Nature, vol. 400', 15/07/1999, p. 242-245(4). Lien direct consulté le 03/03/2008.
- ↑ Oganessian et al., « Synthesis of superheavy nuclei in the 48Ca+244Pu reaction: 288114 » dans Phys. Rev. C, vol. 62, 2000, p. 041604. Lien direct consulté le 03/03/2008.
- ↑ Oganessian et al., « Measurements of cross sections for the fusion-evaporation reactions 244Pu(48Ca,xn)292−x114 and 245Cm(48Ca,xn)293−x116 » dans Phys. Rev. C, vol. 6, n° 9, 2004, p. 054607. Lien direct consulté le 03/03/2008.
- ↑ P. Roy Chowdhury, C. Samanta, D. N. Basu, « α decay half-lives of new superheavy elements », dans Phys. Rev. C, vol. 73, 26 January 2006, p. 014612 [texte intégral lien DOI]
- ↑ C. Samanta, P. Roy Chowdhury, D. N. Basu, « Predictions of alpha decay half lives of heavy and superheavy elements », dans Nucl. Phys. A, vol. 789, 2007, p. 142–154 [texte intégral lien DOI]
- ↑ P. Roy Chowdhury, C. Samanta, D. N. Basu, « Search for long lived heaviest nuclei beyond the valley of stability », dans Phys. Rev. C, vol. 77, 2008, p. 044603 [texte intégral lien DOI]
- ↑ P. Roy Chowdhury, C. Samanta, D. N. Basu, « Nuclear half-lives for α-radioactivity of elements with 100 ≤ Z ≤ 130 », dans At. Data & Nucl. Data Tables, vol. 94, 2008, p. 781–806 [texte intégral lien DOI]
- ↑ R.C.Barber; H.W.Gaeggeler;P.J.Karol;H. Nakahara; E.Verdaci; E. Vogt, « Discovery of the element with atomic number 112 », dans Pure Appl. Chem., 2009 [texte intégral lien DOI]
- ↑ Rapport 2008 du FLNR au JINR : « Chimie des éléments 112 et 114 », p. 87, accédé le 08/07/2009.
Articles liés
Liens externes
s1 s2 g f1 f2 f3 f4 f5 f6 f7 f8 f9 f10 f11 f12 f13 f14 d1 d2 d3 d4 d5 d6 d7 d8 d9 d10 p1 p2 p3 p4 p5 p6 1 H He 2 Li Be B C N O F Ne 3 Na Mg Al Si P S Cl Ar 4 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 5 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 6 Cs Ba La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 7 Fr Ra Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr Rf Db Sg Bh Hs Mt Ds Rg Cn Uut Uuq Uup Uuh Uus Uuo 8 Uue Ubn * Ute Uqn Uqu Uqb Uqt Uqq Uqp Uqh Uqs Uqo Uqe Upn Upu Upb Upt Upq Upp Uph Ups Upo Upe Uhn Uhu Uhb Uht Uhq Uhp Uhh Uhs Uho ↓ g1 g2 g3 g4 g5 g6 g7 g8 g9 g10 g11 g12 g13 g14 g15 g16 g17 g18 * Ubu Ubb Ubt Ubq Ubp Ubh Ubs Ubo Ube Utn Utu Utb Utt Utq Utp Uth Uts Uto Métalloïdes Non-métaux Halogènes Gaz rares Métaux alcalins Métaux alcalino-terreux Métaux de transition Métaux pauvres Lanthanides Actinides Superactinides Éléments non classés - Portail de la chimie
Catégories : Élément chimique | Métal pauvre | Transactinide
Wikimedia Foundation. 2010.