- A.R.N.
-
Acide ribonucléique
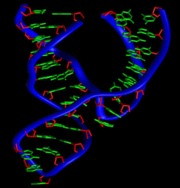
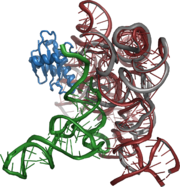
 Structure 3D d'un ARN régulateur (riboswitch)[1]
Structure 3D d'un ARN régulateur (riboswitch)[1]
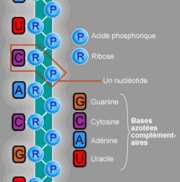
L'Acide ribonucléique ou ARN est un polymère linéaire constitué d'un enchaînement de nucléotides. Chaque nucléotide contient un groupement phosphate, un sucre, le ribose et une base azotée. Les nucléotides sont liés les uns aux autres par des liaisons phosphodiester. On trouve quatre bases azotées dans l'ARN, l'adénine, la guanine, la cytidine et l'uracile. L'ARN a de nombreuses similarités avec l'ADN, avec cependant quelques différences importantes : sur le plan de la structure, l'ARN contient un ribose à la place du désoxyribose de l'ADN, ce qui rend l'ARN chimiquement plus instable et la thymine de l'ADN y est remplacée par l'uracile, qui possède les mêmes propriétés d'appariement de base avec l'adénine. Sur le plan fonctionnel, l'ARN est le plus souvent trouvé dans les cellules sous forme de simple brin, tandis que l'ADN est présent sous forme de deux brins complémentaires, formant une double hélice. Enfin les molécules d'ARN trouvées dans les cellules sont plus courtes (de quelques dizaines à quelques milliers de nucléotides) que l'ADN du génome (de quelques millions à quelques milliards de nucléotides).
Dans la cellule, l'ARN est produit par transcription à partir de l'ADN situé dans le noyau. L'ARN est donc une copie d'une région de l'un des brins de l'ADN. Les enzymes qui effectuent cette copie ADN→ARN s'appellent des ARN polymérases. Les ARN ainsi produits peuvent avoir trois grands types de fonctions, ils peuvent être support de l'information génétique d'un ou plusieurs gènes codant pour des protéines (on parle alors d'ARN messagers), ils peuvent adopter une structure secondaire et tertiaire stable et accomplir des fonctions catalytiques (par exemple l'ARN ribosomique), ils peuvent enfin servir de guide ou de matrice pour des fonctions catalytiques accomplies par des facteurs protéiques (par exemple les microARN)
Sommaire
Structure de l'ARN
Article détaillé : Structure de l'ARN.Les ribonucléotides
Structure chimique
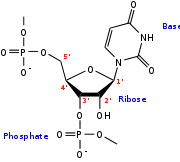 Structure d'un brin d'ARN. Les atomes du ribose sont numérotés. La base représentée est l'uracile, qui n'est présente naturellement que dans l'ARN, à la place de la thymine, présente dans l'ADN
Structure d'un brin d'ARN. Les atomes du ribose sont numérotés. La base représentée est l'uracile, qui n'est présente naturellement que dans l'ARN, à la place de la thymine, présente dans l'ADN
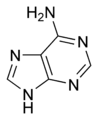
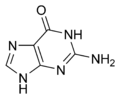
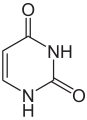
L'ARN est un acide nucléique c'est à dire une molécule constituée d'un enchainement de nucléotides . Chaque nucléotide de l'ARN est constitué d'un pentose, le ribose, dont les atomes de carbone sont numérotés de 1' à 5', d'une base azotée et d'un groupement phosphate. La base azotée est reliée par un atome d'azote au carbone 1' du ribose. Les nucléotides sont liés les uns aux autres par des groupements phosphate, par l'intermédiaire de liaisons phosphodiester au niveau des carbones 3' et 5'. L'ARN possède quatre bases azotées différentes : l'adénine (notée A), l'uracile (noté U), la cytosine (notée C) et la guanine (notée G). La thymine de l'ADN est remplacée par l'uracile dans l'ARN. La différence entre ces deux bases est le remplacement d'un groupement méthyle en position 5 de la thymine par un hydrogène dans l'uracile. Cette modification de structure ne modifie pas les propriétés d'appariement avec l'adénine[2],[3]. Les quatre bases azotées qui assurent la variabilité de la molécule d'ARN, ainsi que la complémentarité des deux brins.
Stéréochimie
Sur le plan structural, la présence d'un oxygène sur la position 2' du ribose influence la conformation du cycle furanose du ribose. Ce cycle à cinq atomes n'est pas plan, ce qui conduit à deux conformères principaux du sucre, appelés C2'-endo ou C3'-endo. Dans l'ARN qui comporte un oxygène en position 2', la position C3'-endo est privilégiée[4], ce qui modifie profondément la structure des doubles hélices comportant des brins ARN. Ces duplex d'ARN forment une hélice de type A, différente de celle qui est observée de façon majoritaire dans l'ADN classique qui est une hélice de type B, où le désoxyribose est en conformation C2'-endo[5].
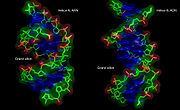
Double hélice d'ARN
L'hélice de type A, qu'adopte l'ARN lorsqu'il forme un duplex, a des propriétés géométriques assez différentes de celles de l'hélice de type B. Tout d'abord le nombre de paires de bases par tour d'hélice est de 11 au lieu de 10 pour l'ADN en forme B. Le plan des paires de bases n'est plus perpendiculaire à l'axe de l'hélice, mais forme un axe d'environ 75 degrés avec celui-ci[8]. Il en résulte un déplacement de l'axe de l'hélice qui ne passe plus par le centre de l'appariement des bases, mais à l'intérieur du grand sillon. Ceci induit une augmentation du diamètre de l'hélice qui passe d'environ 20 Å pour l'ADN en forme B à environ 26 Å pour l'ARN en forme A[9]. Enfin la géométrie des deux sillons est profondément affectée : le petit sillon devient très accessible, tandis que le grand sillon devient très profond, étroit et pincé. Ceci a un impact sur la manière dont l'ARN en duplex apparié peut interagir avec des protéines, car l'étroitesse du grand sillon est une barrière à l'accessibilité de ligands protéiques.
Structure in vivo
La plupart des ARN naturels sont présents sous forme simple brin dans la cellule, contrairement à l'ADN qui est sous forme d'un double-brin apparié. Les ARN simple brin se replient le plus souvent sur eux-mêmes, formant une structure intramoléculaire qui peut être très stable et très compacte. La base de cette structure est la formation d'appariements internes, entre bases complémentaires (A avec U, G avec C et, parfois, G avec U).
La description des appariements internes entre les bases d'un ARN s'appelle la structure secondaire. Cette structure secondaire peut être complétée par des interactions à longue distance qui définissent alors une structure tridimensionnelle ou structure tertiaire.La formation de la structure des ARN est très souvent dépendante des conditions physico-chimiques environnantes et en particulier de la présence de cations divalents, comme le magnésium Mg2+, dans la solution. Ces cations interagissent avec les groupements phosphate du squelette et stabilisent la structure, en particulier en faisant écran à la répulsion électrostatique entre les charges négatives de ces phosphates. [10]
L'existence de structure tertiaire dans les ARN est à la base de la richesse de ses fonctions et en particulier de sa capacité à catalyser des réactions chimiques (ribozymes).
Structure secondaire
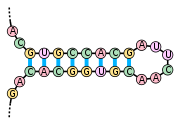
La structure secondaire d'un ARN est la description de l'ensemble des appariements internes au sein d'une molécule simple brin[11]. Cet ensemble d'appariements induit une topologie particulière, composée de région en hélice (tiges) et de régions non-appariées (boucles). Par extension, la structure secondaire recouvre également la description de cette topologie.
L'élément moteur de la formation de structures secondaires au sein d'un ARN simple-brin est l'existence de régions contenant des séquences répétées inversées, qui peuvent s'apparier pour former localement une structure en double hélice. Par exemple, si l'ARN contient les deux séquences suivantes : --GUGCCACG----CGUGGCAC--, celles-ci forment un motif répété inversé, les nucléotides du second segment étant les complémentaires de ceux du premier, après inversion de leur sens de lecture. Ces deux segments peuvent donc s'apparier de manière antiparallèle pour former une région localement en duplex. La région entre les deux segments forme alors une boucle reliant les deux brins du duplex. On parle alors de structure en tige et boucle ou en épingle à cheveux.
Dans des ARN de longueur plus importante, il peut exister des structures plus complexes, qui résultent de l'appariement de plusieurs régions complémentaires ou séquences répétées inversées. En fonction de la manière dont sont "emboîtées" ces différentes régions, on obtient des éléments topologiques variés, avec des tiges ou régions appariées, et divers types de boucles :
- Les boucles terminales, situées à l'extrémité d'une tige.
- Les boucles internes, qui connectent deux tiges.
- Les boucles multiples, qui connectent trois tiges ou plus et constituent des points de branchement de la structure.
- Les hernies (en anglais bulge) ou boucles latérales qui sont sur un seul des deux brins d'une hélice. La continuité de l'hélice n'est en général pas affecté et l'ensemble des bases reste empilé de manière coaxiale, de part et d'autre de la hernie.
Il n'existe pas toujours une structure unique stable pour une séquence donnée et il arrive que certains ARN puissent adopter plusieurs conformations alternatives en fonction de la liaison d'un ligand (protéine, petite molécule...) ou des conditions physico-chimiques (force ionique, pH). On peut en général suivre la formation ou la fusion de la structure secondaire d'un ARN par des mesures spectroscopiques. Ainsi par exemple, l'absorption dans l'UV des bases de l'ARN est plus importante à l'état déplié qu'à l'état replié (phénomène d'hyperchromicité).
Structure tertiaire
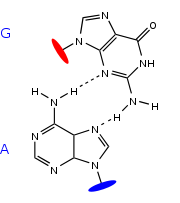 Exemple d'appariement non-canonique : la paire G:A en cisaille (sheared). Celle-ci est par exemple présente dans la structure de l'ARN ribosomique 5S
Exemple d'appariement non-canonique : la paire G:A en cisaille (sheared). Celle-ci est par exemple présente dans la structure de l'ARN ribosomique 5S
Appariements non-canoniques
Au-delà de la topologie des boucles et des hélices composées de paires de bases standard, un ARN peut adopter une structure tridimensionnelle compacte, ou structure tertiaire, comme une protéine. A l'intérieur de cette structure, les hélices canoniques sont complétées par des appariements non canoniques, c'est à dire distincts des d'appariements de base classiques, de type Watson-Crick (A-U et G-C) et bancals (wobble, G-U). On a observé une grande variété de ces appariements dans les structures tridimensionnelles d'ARN résolues par cristallographie ou par RMN. On trouve par exemple des appariements Hoogsteen, des appariements "en cisaille" (sheared). Il existe également des interactions base-ribose.
Une nomenclature systématique de toutes ces interactions a été proposée par Eric Westhof et ses collaborateurs[12]. Plus de 150 types d'appariements ont été observés et ont été regroupés en douze grandes familles. Ces appariements non-canoniques impliquent toujours des liaisons hydrogènes entre les bases, qui sont coplanaires, comme dans les paires Watson-Crick.
Interactions à longue distance
Des appariements canoniques ou non-canoniques peuvent intervenir entre des régions distantes de la structure secondaire, souvent localisées dans des boucles, ce qui permet de stabiliser un repliement compact de la structure.
Parmi ces interactions non canoniques à longue distance, on peut citer :
- Les pseudonœuds : Structure formée par l'interaction d'une boucle avec une région située à l'extérieur de la tige qui la délimite.
- Les triplex de brin : Surviennent lorsqu'une région simple brin vient s'insérer dans le grand sillon d'une région en hélice.
- Les interactions tétraboucle-récepteur : interaction entre boucles hyperstables de quatre nucléotides (tetraboucles) et structures en duplex ou quasi duplex.
Similitudes et différences entre l'ADN et ARN
- l'ARN a pour composant un sucre ribose là où l'ADN a un désoxyribose ;
- la base uracile a un rôle pour l'ARN qui est rempli par la thymine dans l'ADN ;
- l'ARN existe généralement sous la forme d'un simple brin (monocaténaire), sauf chez quelques organismes tels les rétrovirus, tandis que l'ADN est double brin (bicaténaire) avec une structure en double hélice ; L'appariement de base complémentaire dans un brin d'ADN peuvent lui conférer des propriétés d'une structure double brin.
- l'ARN est court : de quelques dizaines à quelques milliers de nucléotides, contre quelques millions à quelques milliards dans l'ADN.
Les trois premières différences donnent à l'ARN une stabilité bien moindre que celle de l'ADN :
- les deux fonctions alcools géminés du ribose sont susceptibles d'hydrolyse alcaline et acide tandis que le désoxyribose de l'ADN, qui a perdu ce groupe fonctionnel y est insensible (D de ADN signifie Désoxyribonucléique, i.e. ayant perdu une fonction oxy(-OH), au niveau 2' du ribose)
Le ribose possède un groupement hydroxyle en position 2', qui est absent dans le désoxyribose de l'ADN. Cette fonction 2'-OH a des incidences multiples sur la structure de l'ARN. Tout d'abord sur le plan chimique, cette fonction alcool rend l'ARN sensible à l'hydrolyse alcaline. La présence des deux oxygènes en cis sur le positions 2' et 3' rend possible la cyclisation du phosphate sur les positions 2' et 3', qui se produit très rapidement lorsqu'une base vient arracher le proton du 2'-OH. Cette cyclisation du nucléotide provoque une coupure de la chaîne ribose-phosphate et libère des extrémités 5'-OH et 2',3' phosphate cyclique[13].
- L'uracile est moins ‘‘coûteux’’ à produire pour les organismes vivants que la thymine, mais se convertit lentement en cytosine. Ce serait pour cette raison que l'ARN a de l'uracile et l'ADN de la thymine : la cellule produit beaucoup d'ARN mais ne le conserve pas, c'est donc le coût de production qui prime sur la stabilité de l'information. À l'inverse, l'ADN doit conserver une information longtemps mais n'est produit que rarement (lors de la division cellulaire), c'est donc la stabilité qui prime sur le coût.
- si un brin d'ARN, monocaténaire, est endommagé, il se produira une erreur irrécupérable ; en revanche, si un des deux brins d'ADN est endommagé, la cellule peut utiliser le brin intact pour réparer.
D'un point de vue évolutif, certains éléments permettent de penser que l'ARN serait antérieur à l'ADN comme support de l'information génétique, ce qui expliquerait ses fonctions plus étendues et sa généralisation. L'ADN serait apparu plus tard et n'aurait supplanté l'ARN que pour le rôle de stockage à long terme, en raison de sa plus grande stabilité.
Synthèse de l'ARN à partir de l'ADN
Article détaillé : Transcription (biologie).Article connexe : ARN polymérase.La synthèse d'une molécule d'ARN à partir de l'ADN s'appelle la transcription. C'est un processus complexe qui fait intervenir une enzyme de la famille des ARN polymérases ainsi que des protéines associées. Les différentes étapes de cette synthèse sont l'initiation, l'élongation et la terminaison. Le processus de synthèse des ARN est sensiblement différent chez les organismes procaryotes et chez les cellules eucaryotes[14]. En fin, après la synthèse proprement dite, l'ARN peut subir un processus de maturation, qui conduit à la modification de la séquence et/ou de la structure chimique de l'ARN (voir plus bas).
L'initiation
Le démarrage de la transcription d'un ARN par une ARN polymérase s'effectue au niveau d'une séquence spécifique sur l'ADN, appelée promoteur. Ce promoteur comporte un ou plusieurs éléments de séquence conservés[15], qui sur lesquels se fixent en général des protéines spécifiques, les facteurs de transcription. Juste en amont du site de démarrage de la transcription, l'élément proximal est en général riche en nucléotides T et A, appelé boite TATA[16] chez les eucaryotes ou boite de Pribnow chez les bactéries[17]. Les facteurs de transcription favorisent le recrutement de l'ARN polymérase sur le promoteur et l'ouverture du duplex d'ADN. Il se forme alors ce qu'on appelle une "bulle de transcription" avec l'ADN ouvert, dont l'un des brin (la matrice) est hybridé avec l'ARN en cours de synthèse.
L'élongation
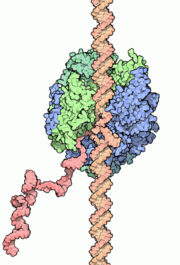
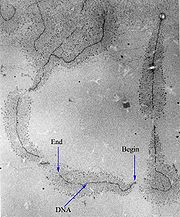 Vue en microscopie électronique des "arbres de Noël" produits par la transcription d'un gène actif. Le "tronc" de l'arbre est constitué de l'ADN et les branches sont les diiférentes molécules d'ARN en cours de synthèse. Celles-ci sont plus courtes vers le debut de la région transcrite et plus longues vers la fin
Vue en microscopie électronique des "arbres de Noël" produits par la transcription d'un gène actif. Le "tronc" de l'arbre est constitué de l'ADN et les branches sont les diiférentes molécules d'ARN en cours de synthèse. Celles-ci sont plus courtes vers le debut de la région transcrite et plus longues vers la fin
Une fois l'ARN polymérase fixée sur le promoteur et la bulle de transcription formée, elle synthétise les premiers nucléotides de manière statique sans quitter la séquence du promoteur. Les facteurs de transcription se détachent et l'ARN polymérase devient processive[18]. Elle transcrit alors l'ARN de 5' vers 3', en utilisant l'un des deux brin de l'ADN comme matrice et des ribonucléotides triphosphates (ATP, GTP, CTP et UTP) comme précurseurs. In vivo, chez Escherichia coli, la vitesse d'allongement de l'ARN polymérase est d'environ 50 à 90 nucléotides par seconde[19]
La terminaison
La terminaison de la transcription de l'ARN procède selon des mécanismes complètement différents chez les bactéries et chez les eucaryotes.
Chez les bactéries, le mécanisme principal de terminaison fait intervenir une structure particulière de l'ARN, le terminateur, composé d'une tige-boucle stable suivie d'une série d'uridines (U). Lorsque l'ARN polymérase synthétise cette séquence, le repliement de la tige d'ARN provoque une pause de la polymérase[20]. L'ARN qui n'est plus apparié à l'ADN matrice que par une série d'appariements A-U faibles et se détache, sans intervention d'autres facteurs protéiques. La terminaison peut aussi se faire via l'intervention d'un facteur protéique spécifique, le facteur Rho.
Chez les eucaryotes, la terminaison de la transcription par l'ARN polymérase II est couplée à la polyadénylation. Deux complexes protéiques, CPSF (Cleavage and Polyadenylation Specificity factor) et CStF (Cleavage Stimulation Factor) reconnaissent les signaux de polyadénylation (5'-AAUAAA-3') et de coupure de l'ARN. Ils clivent l'ARN, induisent le détachement de la polymérase de l'ADN et recrutent la poly-A polymérase qui va ajouter la queue poly-A (voir plus bas).
La maturation
La maturation des ARN comprend un ensemble de modifications chimiques postérieures à l'étape de transcription proprement dite par l'ARN polymérase. Ces modifications sont principalement observées chez les eucaryotes et jouent un rôle important dans le devenir de l'ARN maturé. Les principales modifications sont, l'adjonction d'une coiffe en 5', la polyadénylation en 3', l'épissage, l'introduction de modifications chimiques au niveau de la base ou du ribose et enfin l'édition.
La coiffe
Article détaillé : Coiffe (biologie).La coiffe ou 5'-cap est un nucléotide modifié qui est ajouté à l'extrémité 5' de l'ARN messager, dans les cellules eucaryotes. Elle se compose d'une guanosine méthylée reliée par une liaison 5'-5' diphosphate au premier nucléotide transcrit par l'ARN polymérase[21]. Cette modification est introduite dans le noyau de la cellule, par l'action successive de plusieurs enzymes : triphosphatase, guanylyltransférase, méthyltransférases.
La coiffe joue plusieurs rôles : elle augmente la stabilité de l'ARN en le protégeant contre la dégradation par des exonucléases 5'-3', elle permet aussi le recrutement de facteurs d'initiation de la traduction nécessaires à la fixation du ribosome sur les ARN messagers cellulaires. La coiffe est donc essentielle à la traduction de la plupart des ARNm.
La polyadénylation
Article détaillé : Polyadénylation.La polyadénylation consiste en l'addition d'une extension à l'extrémité 3' de l'ARN composée exclusivement de ribonucléotides de type adénosine (A). Pour cette raison, l'extension est appelée queue poly (A). Bien que composée de nucléotides standard, cette queue poly (A) est ajoutée post-transcriptionnellement par une enzyme spécifique appelée poly (A) polymérase[22] et n'est pas codée dans l'ADN génomique. La queue poly (A) est trouvée principalement à l'extrémité des ARN messagers. Chez les eucaryotes, la polyadénylation des ARNm est nécessaire à leur traduction par le ribosome et participe à leur stabilisation. La queue poly (A) est en particulier reconnue par la PABP (poly (A) binding protein).
Chez les bactéries et dans certaines mitochondries, la polyadénylation des ARN est au contraire un signal de dégradation[23].
L'épissage
Article détaillé : Épissage.L'épissage est une modification post-transcriptionnelle qui consiste en l'élimination des introns et la suture des exons dans les ARN messagers et dans certains ARN structurés comme les ARNt. Présents chez les organismes eucaryotes, les introns sont des segments d'ARN qui sont codés dans le génome et transcrits dans l'ARN précurseur, mais qui sont éliminés du produit final. Dans la plupart des cas, ce processus fait intervenir une machinerie spécifique complexe appelée le splicéosome[24]. L'épissage se produit dans le noyau des cellules eucaryotes, avant l'export de l'ARN maturé vers le cytoplasme.
Bases modifiées
Après leur transcription par l'ARN polymérase, certains ARN subissent des modifications chimiques sous l'action d'enzymes spécifiques. Les principaux ARN subissant des modifications sont les ARN de transfert et les ARN ribosomiques.On peut également considérer que les méthylations intervenant dans la synthèse de la coiffe sont des modifications de base particulières. Dans le cas général, les modifications peuvent porter soit sur la base, soit sur le ribose. Les principales modifications rencontrées sont :
- Sur le ribose : des O-méthylations de la position 2'-OH.
- Sur la base :
- L'isomérisation des uridines qui donne des pseudouridines.
- Des méthylations, soit sur des atomes de carbone (ribothymidine), soit sur des atomes d'azote (7-méthyl-guanosine,...).
- Une réduction, qui transforme les uridines en dihydrouridine.
- Des thiolations
- Des modifications plus complexes (isopenténylation, thréonyl-carbamoylation...).
Dans les ARN de transfert, l'introduction de bases modifiées augmente la stabilité des molécules.
L'édition
Article détaillé : Édition (biologie).L'édition des ARN consiste en une modification de la séquence de l'acide rionucléique, postérieure à la transcription par l'ARN polymérase. A l'issue du processus d'édition, la séquence de l'ARN est donc différente de celle de l'ADN. Les changements opérés peuvent être la modification d'une base, la substitution d'une base ou encore l'ajout d'une ou plusieurs bases. Ces modifications sont effectuées par des enzymes qui agissent sur l'ARN, comme par exemple les cytidines déaminases, qui transforment chimiquement les cytidines en uridines.
Fonction dans la cellule
Article connexe : Liste d'ARN.
Dans les cellules, les ARN remplissent trois rôles distincts et complémentaires :- Support temporaire de l'information génétique. C'est l'ARN messager qui remplit ce rôle, il est utilisé par la cellule pour transmettre l'information correspondant à un gène donné à l'extérieur du noyau, puis pour synthétiser des protéines à partir de ces informations.
- Catalyseur enzymatique. Comme les protéines, les ARN peuvent se replier en trois dimensions pour former des structures complexes. Ces structures permettent à certains ARN de se comporter comme des enzymes, on parle alors de ribozyme. Le ribosome, la ribonucléase P et certains introns sont des ribozymes. On pense que la machinerie d'épissage des ARN messagers (le spliceosome), est également aussi un ribozyme, même si la démonstration formelle n'en a pas encore été apportée.
- Guide pour des enzymes. Certains ARN sont utilisés comme co-facteurs par des protéines pour permettre leur ciblage vers des séquences spécifiques. Parmi ceux-ci, on peut citer les petits ARN nucléolaires (snoARN), qui guident les enzymes de modification de l'ARN ribosomique, l'ARN télomérique, qui est un cofacteur de la télomérase, l'enzyme qui fabrique les extrémités des chromosomes, ou encore les ARN interférents.
Enfin, le génome de certains virus est exclusivement constitué d'ARN et pas d'ADN. C'est en particulier le cas des virus de la grippe, du SIDA, de l'hépatite C ou la poliomyélite. Suivant les cas, la réplication de ces virus peut passer par un intermédiaire ADN (rétrovirus), mais peut aussi se faire directement d'ARN en ARN.
L'ARN est donc une molécule très polyvalente, ce qui a conduit Walter Gilbert, co-inventeur du séquençage de l'ADN à proposer en 1986 une hypothèse selon laquelle l'ARN serait la plus ancienne de toutes les macromolécules biologiques[25]. Cette théorie, dite du "RNA World" (le monde de l'ARN), permet de s'affranchir d'un Paradoxe de l'œuf et de la poule qui survient lorsqu'on cherche à savoir qui des protéines (catalyseurs) et de l'ADN (information génétique) sont apparus en premier. Dans ce modèle, l'ARN, capable de combiner à la fois les deux types de fonctions serait le précurseur universel.
Les ARN messagers
Article détaillé : Acide ribonucléique messager.L'information génétique contenue au sein de l'ADN n'est pas utilisée directement par la cellule pour fabriquer des protéines. Celle-ci utilise pour cela des copies transitoires de l'information génétique qui sont les ARN messagers ou ARNm. Chaque ARN messager porte les instructions pour former le plus souvent une seule protéine, ce que l'on appelle un cistron, mais parfois il peut porter les instructions pour plusieurs protéines. Il correspond donc à la copie d'un seul des gènes du génome (on parle alors d'ARNm monocistronique) ou parfois de quelques uns (ARNm polycistronique).
L'ARN messager ne contient la copie que d'un seul des deux brins de l'ADN, celui qui est codant et pas la séquence complémentaire. Par rapport à la séquence du gène contenue dans l'ADN du génome, celle de l'ARNm correspondant peut contenir des modifications et en particulier l'épissage (voir plus haut), qui élimine les régions non-codantes. L'ARN messager synthétisé dans le noyau de la cellule est exporté dans le cytoplasme pour être traduit en protéine. Contrairement à l'ADN qui est une molécule pérenne, présente pendant toute la vie de la cellule, les ARN messagers ont une durée de vie limitée, de quelques minutes à quelques heures, après quoi ils sont dégradés et recyclés.
L'utilité des ARN messagers est multiple. Ils permettent de préserver l'original ADN qui n'est pas directement utilisé pour la traduction, la cellule ne travaillant que sur la copie ARNm. L'existence d'ARN messagers offre surtout à la cellule un mécanisme important de régulation de la production des protéines à partir du génome. Le besoin cellulaire en telle ou telle protéine peut varier en fonction de l'environnement, du type de cellule, du stade de développement. Il faut donc pouvoir déclencher ou arrêter la production de la protéine en fonction de ce besoin. La cellule ne déclenche donc la transcription de l'ARNm correspondant qu'en cas de nécessité. Lorsque la concentration de la protéine est suffisante, la transcription d'ARNm s'arrête, celui-ci est progressivement dégradé et la production s'arrête. Il est donc important que l'ARNm soit une molécule transitoire, afin de pouvoir réaliser cette régulation essentielle.
Les ARN catalytiques ou ribozymes
Article détaillé : Ribozyme.L'existence d'ARN doués de capacités catalytiques a été découverte dans les années 80, en particulier par l'équipe de Thomas Cech, qui travaillait sur les introns du gène de l'ARN ribosomique du protozoaire ciliié Tetrahymena[26] et celle de Sidney Altman qui étudiait la ribonuclease P, l'enzyme de maturation de l'ARNt[27]. Cech et Altman on été récompensés par le prix Nobel de chimie en 1989 pour cette découverte.
Dans ces deux cas, l'ARN seul est capable de catalyser une réaction de coupure ou de transestérification spécifique, en l'absence de protéine. Ces ARN catalytiques ont été appelés ribozymes, car ce sont des enzymes constituées d'acide ribonucléique. Dans le cas de l'intron de Tetrahymena, il s'agit d'un auto-épissage, l'intron étant sont propre substrat, tandis que pour la ribonuclease P, on a une véritable enzyme agissant en trans.
Depuis ces découvertes initiales, d'autres ribozymes naturels ont été identifiés :
- Les ARN de viroïdes ou de virus satellites (virusoïdes) qui sont capables de se cliver eux mêmes[28].
- Il existe aujourd'hui des arguments très forts, basés sur la résolution de sa structure 3D, pour affirmer que ribosome, la machinerie cellulaire responsable de la traduction de l'ARNm en protéines est lui-même un ribozyme[29]. Les deux sites actifs du ribosome, le centre de décodage sur la petite sous-unité et le centre peptidyl-transférase, qui forme les liaisons peptidiques sont en effet exclusivement composés de segments d'ARN ribosomique.
- Le splicéosome, qui catalyse l'épissage des ARNm cytoplasmiques eucaryotes, est probablement aussi un ribozyme [30].
- Certains riboswitchs, des régions régulatrices structurées portées par des ARN messagers ont une activité catalytique de coupure en présence d'un ligand.
- Il existe enfin des ribozymes synthétiques, qui ont été isolés par des méthodes d'évolution in vitro, capable de catalyser une grande diversité de réactions.
De manière générale, dans tous ces ribozymes, c'est leur repliement spécifique qui leur permet d'effecteur la reconnaissance de leur substrat et la catalyse, comme dans le cas des enzymes protéiques.
Les ARN guides
Les ARN guides sont des ARN qui s'associent à des enzymes protéiques et servent à en guider l'action sur des ARN ou des ADN de séquence complémentaire. L'ARN guide s'apparie à l'acide nucléique substrat et permet de cibler l'activité de l'enzyme. On a identifié plusieurs types :
- Les petits ARN nucléolaires. On trouve dans le nucléole des ARN guides appelés petits ARN nucléolaires ou ARNsno qui dirigent l'action d'enzymes de modification de l'ARN ribosomique, en particulier les 2'-O-méthylations et les pseudouridylations[31]. Ce mécanisme permet de à la cellule de modifier spécifiquement de multiples positions de l'ARNr, avec une seule enzyme mais plusieurs ARNsno utilisés comme guides. Les ARNsno sont souvent codés par des séquences introniques[32].
- Les microARN sont également des ARN guides qui interviennent dans le processus d'interférence ARN. Associé à un complexe protéique appelé RISC (RNA induced silencing complex), ces petits ARN provoquent soit une dégradation de l'ARNm cible auquel ils s'apparient, soit une répression de sa traduction[33].
- TERC (telomerase RNA component), la sous-unité ARN de la télomérase. Cet ARN structuré est associé à la transcriptase inverse qui synthétise les télomères, extrémités des chromosomes. Il contient une séquence qui sert de substrat à la télomérase pour synthétiser l'ADN télomérique de séquence complémentaire[34]. Il guide donc l'activité de l'enzyme, mais en servant de matrice, plutôt qu'en formant un appariement avec le substrat.
Références
- ↑ Montange R.K., Batey R.T., « Structure of the S-adenosylmethionine riboswitch regulatory mRNA element », dans Nature, vol. 441, 2006, p. 1172-1175 [lien PMID]
- ↑ (en) Saenger, W, Principles of nucleic acid structure, Springer (ISBN 0387907629)
- ↑ (en) Barciszewski J, Frederic B, Clark C, RNA biochemistry and biotechnology, Springer (ISBN 0792358627) (OCLC 52403776), p. 73–87
- ↑ Sudaralingam M., « Stereochemistry of nucleic acids and their constituents. IV. Allowed and preferred conformations of nucleosides, nucleoside mono-, di-, tri-, tetraphosphates, nucleic acids and polynucleotides », dans Biopolymers, vol. 7, 1969, p. 821-860
- ↑ Langridge R., Gomatos P.J., « The Structure of RNA. Reovirus RNA and transfer RNA have similar three-dimensional structures, which differ from DNA. », dans Science, vol. 141, 1963, p. 694-698 [lien PMID]
- ↑ Drew H.R., Wing R.M., Takano T., Broka C., Tanaka S., Itakura K., Dickerson R.E., « Structure of a B-DNA dodecamer: conformation and dynamics. », dans Proc. Natl. Acad. Sci. USA, vol. 78, 1981, p. 2179-2183 [lien PMID]
- ↑ Klosterman P.S., Shah S.A., Steitz T.A., « Crystal structures of two plasmid copy control related RNA duplexes: An 18 base pair duplex at 1.20 A resolution and a 19 base pair duplex at 1.55 A resolution. », dans Biochemistry, vol. 38, 1999, p. 14784-14792 [lien PMID]
- ↑ Rosenberg J.M., Seeman N.C., Kim J.J., Suddath F.L., Nicholas H.B., Rich A., « Double helix at atomic resolution. », dans Nature, vol. 243, 1973, p. 150-154 [lien PMID]
Day R.O., Seeman N.C., Rosenberg J.M., Rich A., « A Crystalline Fragment of the Double Helix: The Structure of the Dinucleoside Phosphate Guanylyl-3',5'-Cytidine. », dans Pro. Natl. Acad. Sci. USA, vol. 70, 1973, p. 849-853 [lien PMID] - ↑ Rich A.,Davies D.R., « A new two stranded helical structure: Polyadenylic acid and polyuridylic acid. », dans J. Am. Chem. Soc., vol. 78, 1956, p. 3548-3549 [lien DOI]
- ↑ Woodson S.A., « Metal ions and RNA folding: a highly charged topic with a dynamic future. », dans Curr. Opin. Chem. Biol., vol. 9, 2005, p. 104-109 [lien PMID]
- ↑ Doty P., Boedtker H., Fresco J. R. , Haselkorn R., Litt M., « Secondary Structure in Ribonucleic Acids », dans Proc. Natl. Acad. Sci. USA, vol. 45, 1959, p. 482-499
- ↑ Leontis N.B., Stombaugh J., Westhof E., « The non-Watson-Crick base pairs and their associated isostericity matrices. », dans Nucleic Acids Res., vol. 30, 2002, p. 3497-3531 [lien PMID]
- ↑ Markham R., Smith J.D., « The Structure of Ribonucleic Acids 1. Cyclic nucleotides produced by ribonuclease and by alkaline hydrolysis », dans Biochem. J., vol. 52, 1952, p. 552-557 [lien PMID]
- ↑ Biochimie de Harper, Harold A Harper,A Harold
- ↑ Smale S.T., Kadonaga J.T., « The RNA polymerase II core promoter. », dans Ann. Rev. Biochem., vol. 72, 2003, p. 449-479 [lien PMID]
- ↑ Lifton R.P., Goldberg M.L., Karp R.W., Hogness D.S., « The organization of the histone genes in Drosophila melanogaster: functional and evolutionary implications. », dans Cold Spring Harb. Symp. Quant. Biol., vol. 42, 1978, p. 1047-1051 [lien PMID]
- ↑ Lifton R.P., Goldberg M.L., Karp R.W., Hogness D.S., « Nucleotide sequence of an RNA polymerase binding site at an early T7 promoter. », dans Proc. Natl. Acad. Sci. USA, vol. 72, 1975, p. 784-788 [lien PMID]
- ↑ McClure W.R., Chow Y., « The kinetics and processivity of nucleic acid polymerases. », dans Methods Enzymol., vol. 64, 1980, p. 277-297 [lien PMID]
- ↑ H. Bremer, P.P. Dennis, « Modulation of chemical composition and other parameters of the cell by growth rate. », dans F.C Neidhardt, R Curtiss, III, J.L Ingraham, E.C.C Lin, K.B Low, B Magasanik, W.S Reznikoff, M Riley, M Schaechter, H.E Umbarger (dir.), Escherichia coli and Salmonella typhimurium Cellular and Molecular Biology 2nd edition, ASM Press, Washington, DC., 1996, p. 1553-1569.
- ↑ Adhya S., Gottesman M., « Control of transcription termination. », dans Annu. Rev. Biochem., vol. 47, 1978, p. 967-996 [lien PMID]
- ↑ Banerjee A.K., « 5'-terminal cap structure in eucaryotic messenger ribonucleic acids. », dans Microbiol. Rev, vol. 44, 1980, p. 175-205 [lien PMID]
- ↑ Edmonds M., Abrams R., « Polynucleotide biosynthesis: formation of a sequence of adenylate units from adenosine triphosphate by an enzyme from thymus nuclei. », dans J. Biol. Chem., vol. 235, 1960, p. 1142-1149 [lien PMID]
- ↑ Dreyfus M., Régnier P., « The poly(A) tail of mRNAs: bodyguard in eukaryotes, scavenger in bacteria. », dans Cell, vol. 111, 2002, p. 611-613 [lien PMID]
- ↑ Staley J.P., Guthrie C., « Mechanical devices of the spliceosome: motors, clocks, springs, and things. », dans Cell, vol. 92, 1998, p. 315-326 [lien PMID]
- ↑ Walter Gilbert, The RNA World Nature 319 (1986): 618
- ↑ Kruger K., Grabowski P.J., Zaug A.J., Sands J., Gottschling D.E., Cech T.R., « Self-splicing RNA: autoexcision and autocyclization of the ribosomal RNA intervening sequence of Tetrahymena. », dans Cell, vol. 31, 1982, p. 147-157 [lien PMID]
- ↑ Guerrier-Takada C., Gardiner K., Marsh T., Pace N., Altman S., « The RNA moiety of ribonuclease P is the catalytic subunit of the enzyme. », dans Cell, vol. 35, 1983, p. 849-857 [lien PMID]
- ↑ Forster A.C., Davies C., Hutchins C.J., Symons R.H., « Characterization of self-cleavage of viroid and virusoid RNAs. », dans Methods Enzymol., vol. 181, 1990, p. 583-607 [lien PMID]
- ↑ Cech T.R., « Structural biology. The ribosome is a ribozyme. », dans Science, vol. 289, 2000, p. 878-879 [lien PMID]
- ↑ Valadkhan S., Mohammadi A., Jaladat Y., Geisler S., « Protein-free small nuclear RNAs catalyze a two-step splicing reaction. », dans Proc. Natl. Acad. Sci. USA, vol. 106, 2009, p. 11901-11906 [lien PMID]
- ↑ Kiss-László Z., Henry Y., Bachellerie J.P., Caizergues-Ferrer M., Kiss T., « Site-specific ribose methylation of preribosomal RNA: a novel function for small nucleolar RNAs. », dans Cell, vol. 85, 1996, p. 1077-1088 [lien PMID]
- ↑ Liu J., « Novel intron-encoded small nucleolar RNAs. », dans Cell, vol. 75, 1993, p. 403-405 [lien PMID]
- ↑ Sollner-Webb B., « Control of protein synthesis and mRNA degradation by microRNAs. », dans Curr. Opin. Cell Biol., vol. 20, 2008, p. 214-221 [lien PMID]
- ↑ Shippen-Lentz D., Blackburn E.H., « Functional evidence for an RNA template in telomerase. », dans Science, vol. 247, 1990, p. 546-552 [lien PMID]
Voir aussi
Articles connexes
- Liste des différents types d'ARN
- Acide ribonucléique messager
- ARN double-brin
- microARN
- ARN interférent
- Liste de sigles de biologie moléculaire
- Portail de la biologie cellulaire et moléculaire
Catégorie : ARN
Wikimedia Foundation. 2010.