- Iode 131
-
L’iode 131, noté 131I, est l'isotope de l'iode dont le nombre de masse est égal à 131 : son noyau atomique compte 53 protons et 78 neutrons avec un spin 7/2+ pour une masse atomique de 130,9061242 ± 0,0000012 g/mol.
Il est caractérisé par un défaut de masse de 87 444 761 ± 1 145 eV/c2 et une énergie de liaison nucléaire de 1 103 323 318 ± 1 159 eV[1].
Son activité spécifique est de 4,6×1015 Bq/g.
Sommaire
Propriétés, utilisations et dangers
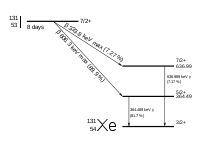
L'iode 131 donne du xénon 131 par désintégration β- selon une période d'un peu plus de 8 jours, en émettant des rayons γ d'au plus 364 keV et des rayons β- (électrons) d'au plus 606 keV[2] :
L'iode 131 trouve une utilisation essentiellement médicale et pharmaceutique, mais constitue également un risque important de contamination environnementale en cas d'explosion nucléaire ou d'accident nucléaire en raison de sa présence comme produit de fission dans les réacteurs nucléaires, car il représente près de 3 % des produits de fission de l'uranium.
Du fait du rayonnement β- émis lors de sa désintégration, l'iode 131 provoque des mutations génétiques dans les cellules où il pénètre, ainsi que dans les cellules voisines, mutations graves qui peuvent entraîner la mort de ces cellules. C'est la raison pour laquelle une dose élevée d'iode 131 peut s'avérer moins dangereuse qu'une dose plus faible, les cellules irradiées étant tuées au lieu de survivre comme germes d'un cancer. L'utilisation médicale de l'iode 131 tend de ce fait à privilégier les doses maximales pour un effet létal visant les tissus cancéreux de la thyroïde, organe où l'iode s'accumule préférentiellement, sous forme d'hormones thyroïdiennes, telles que la thyroxine.
Notes et références
- (en) Matpack – Periodic Table of the Elements « Properties of Nuclides: 53-I-131 ».
- (en) Health Physics Society – Nuclide Safety Data Sheet « Iodine-131 ».
Voir aussi
Articles connexes
- Iode
- Thyroïde
- Hormone thyroïdienne
- Triiodothyronine
- Thyroxine
- Cancer de la thyroïde
- Iodure de potassium
Liens externes
- (en) Argonne National Laboratory – Human Health Fact Sheet, août 2005 « Iodine ».
s1 s2 g f1 f2 f3 f4 f5 f6 f7 f8 f9 f10 f11 f12 f13 f14 d1 d2 d3 d4 d5 d6 d7 d8 d9 d10 p1 p2 p3 p4 p5 p6 1 H He 2 Li Be B C N O F Ne 3 Na Mg Al Si P S Cl Ar 4 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 5 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 6 Cs Ba La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 7 Fr Ra Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr Rf Db Sg Bh Hs Mt Ds Rg Cn Uut Uuq Uup Uuh Uus Uuo 8 Uue Ubn * Ute Uqn Uqu Uqb Uqt Uqq Uqp Uqh Uqs Uqo Uqe Upn Upu Upb Upt Upq Upp Uph Ups Upo Upe Uhn Uhu Uhb Uht Uhq Uhp Uhh Uhs Uho ↓ g1 g2 g3 g4 g5 g6 g7 g8 g9 g10 g11 g12 g13 g14 g15 g16 g17 g18 * Ubu Ubb Ubt Ubq Ubp Ubh Ubs Ubo Ube Utn Utu Utb Utt Utq Utp Uth Uts Uto Métalloïdes Non-métaux Halogènes Gaz rares Métaux alcalins Métaux alcalino-terreux Métaux de transition Métaux pauvres Lanthanides Actinides Superactinides Éléments non classés -
Wikimedia Foundation. 2010.

![\mathrm{^{131}_{\ 53}I\ \xrightarrow[8,02070 \ jours]{\beta^-\ 606\ keV}\ ^{131}_{\ 54}Xe^*\ \xrightarrow {\gamma\ 364\ keV}\ ^{131}_{\ 54}Xe}](a/e0a8f37b4b718c66c311d07243b226cc.png)