- Méthanal
-
Méthanal 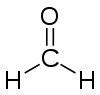
Représentation du méthanal Général Nom IUPAC méthanal Synonymes formaldéhyde
aldéhyde formique
formolNo CAS No EINECS PubChem No E E240 SMILES InChI Apparence gaz, d'odeur caractéristique,
ou liquide incolore (solution)[1]Propriétés chimiques Formule brute CH2O [Isomères] Masse molaire[4] 30,026 ± 0,0012 g·mol-1
C 40 %, H 6,71 %, O 53,29 %,pKa 13,27 à 25 °C[2] Moment dipolaire 2,332 ± 0,002 D [3] Propriétés physiques T° fusion -92 °C[1] T° ébullition -19,5 °C[2] ;
98 °C (solution à 37 %)[1]Solubilité 4,00.105 mg/L (eau, 20 °C) ;
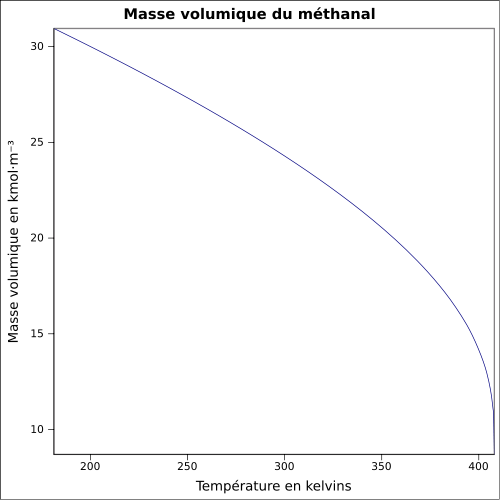
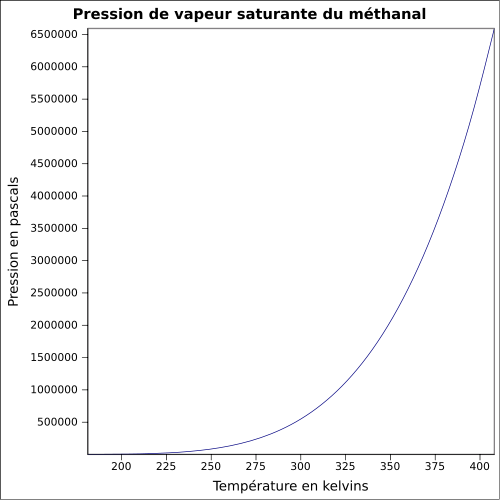
soluble dans l'alcool, l'éther diéthylique, l'acétone, le benzène[2]Masse volumique 0,8 g·cm-3[1] T° d'auto-inflammation 430 °C[1] Point d’éclair 53 °C Limites d’explosivité dans l’air 7–73 %vol[1] Pression de vapeur saturante 3 890 mmHg (25 °C)[2] Point critique 137,2 à 141,2 °C
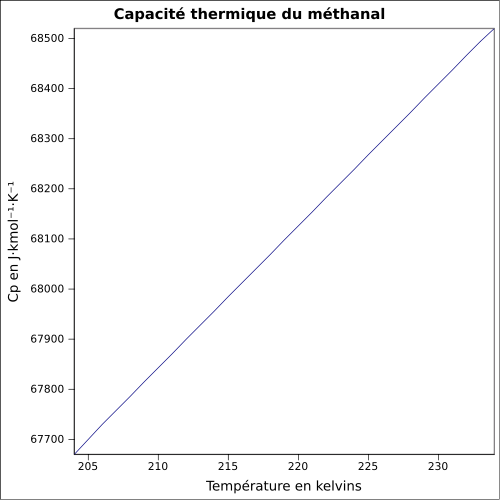
6,784–6,637 MPa[2]Thermochimie S0gaz, 1 bar 218,8 J/mol·K ΔfH0gaz -108,6 kJ/mol Cp 35,4 J/mol.K Propriétés électroniques 1re énergie d'ionisation 10,88 ± 0,01 eV (gaz)[7] Propriétés optiques Indice de réfraction  1,3746 (en solution)[2]
1,3746 (en solution)[2]Spectre d’absorption absorption max (gaz) :
155,5 nm (LOG E=4,37) ;
175 nm (LOG E=4,26)[2]Précautions Directive 67/548/EEC[9] 
T
CPhrases R : 23/24/25, 34, 40, 43, Phrases S : 1/2, 26, 36/37/39, 45, 51, Transport[10] 80 2209
38 1198 SIMDUT[11] 


SGH[12] 


DangerClassification du CIRC Groupe 1 : cancérogène pour l'homme[8] Inhalation potentiellement létal Yeux irritant Écotoxicologie DL50 100 mg·kg-1 (rats, oral)
220,1 mg·kg-1 (lapins, dermal)Valeur d'exposition 0,3 ml/m³ ; 0,37 mg·m-3 LogP 0,35 [2] Unités du SI & CNTP, sauf indication contraire. Le méthanal ou formaldéhyde ou aldéhyde formique ou formol est un composé organique de la famille des aldéhydes, de formule chimique CH2O. C'est d'ailleurs le plus simple des composés de cette famille. À température ambiante, c'est un gaz inflammable.
Il fut synthétisé pour la première fois par le Russe Alexandre Boutlerov en 1859, mais fut formellement identifié par l'Allemand August Wilhelm von Hofmann en 1867. Le terme « formol » est généralement réservé à ses solutions aqueuses.
On trouve du méthanal dans les produits d'une combustion incomplète de substances contenant du carbone. Il y en a dans la fumée des feux de forêt, dans les rejets des automobiles, et dans la fumée du tabac. Le méthanal est aussi produit dans l'atmosphère sous l'action des rayons solaires et du dioxygène sur le méthane atmosphérique ainsi que sur d'autres hydrocarbures. De petites quantités de méthanal sont produites par le métabolisme de la plupart des organismes, dont l'organisme humain.
Sommaire
Propriétés
Bien que le méthanal soit un gaz à température ambiante, il est très soluble dans l'eau, dans laquelle il forme une solution appelée formol. Le méthanal polymérise dans l'eau, ce qui fait que le formol contient peu de méthanal sous forme de monomères. Le méthanal polymérise sous forme de polyoxyméthylène (appelé paraformaldéhyde ; succession de groupements -O-CH2-) ou de 1,3,5-trioxane (trimère cyclique). La dépolymérisation est possible par distillation en présence de traces acides. Généralement, le formol vendu dans le commerce contient aussi du méthanol pour limiter la polymérisation du méthanal.
Le méthanal possède la plupart des propriétés chimiques des aldéhydes, mis à part le fait qu'il soit plus réactif. De plus, il est remarquablement électrophile, et peut réagir par substitution électrophile aromatique avec les composés aromatiques ou par addition électrophile sur les alcènes. En présence d'un catalyseur basique, le méthanal subit une réaction de Cannizzaro et se transforme en acide formique et en méthanol.
Enfin, le formol (methanal) est facilement oxydé par le dioxygène de l'air pour former de l'acide formique. C'est pourquoi il faut conserver le méthanal dans des récipients bien étanches.
Production
Le méthanal est produit industriellement par l'oxydation catalytique du méthanol. Les catalyseurs les plus employés sont l'argent métallique, ou un mélange d'oxyde de fer, de molybdène et de vanadium. Dans ce cas, le méthanol et le dioxygène réagissent à 400 °C selon l'équation :
CH3OH + ½ O2 → H2CO + H2O.
La catalyse à base d'argent réagit à des températures plus hautes, de l'ordre de 650 °C. Deux réactions produisent alors simultanément du méthanal : l'équation ci-dessus, et l'équation de déshydrogénation ci-dessous :
CH3OH → H2CO + H2.
L'oxydation prolongée du méthanal conduit à la formation d'acide formique, que l'on trouve en faible concentration dans les solutions industrielles de méthanal. À une échelle réduite, le formol peut être produit grâce à diverses réactions comme la conversion de l'éthanol.
Le méthanal peut également être produit lors de l'ozonolyse d'un alcène terminal.
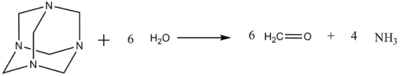
On peut également produire le formaldéhyde en ajoutant de l'hexaméthylènetétramine au milieu réactionnel suivant la réaction :
Production artisanale
Le méthanal est obtenu à partir de la formaline, solution aqueuse dans lequel le méthanal est dissous à 37 % en masse.
Le méthanal se dégage avec l'ajout de permanganate de potassium (KMnO4) dans les proportions de 1 g de permanganate pour 2 ml de formaline. C'est une réaction exothermique, dont la chaleur générée est importante.
Cette méthode est utilisée par certains aviculteurs pour les fumigations d'œufs.
Utilisation
Le méthanal est utilisé comme :
- désinfectant, notamment en médecine vétérinaire (pédiluves de désinfection) ;
- fixateur et conservateur de cadavres d'animaux ou d'humains (pour les dissections d'écoles de médecine par exemple) ou pour la conservation ou fixation d'échantillons ou de certains prélèvements biologiques, dont dans la cadre d'analyses IBGN, IBMR ou IOBS ;
- conservateur dans certains vaccins ;
- pour assécher ou tuer la peau (pour le traitement médical des verrues par exemple) ;
- en dentisterie ; sous forme directe (formaldéhyde) ou dérivée (paraformaldéhyde, polyoxyméthylène) intégrés dans un grand nombre de spécialités destinées à obturer les canaux des dents dévitalisées. Contrairement aux médicaments, les produits et matériaux employés en art dentaire ne sont pas soumis à une autorisation de mise sur le marché, ce qui explique qu'ils échappent à la réglementation évoquée au paragraphe suivant ;
- pour embaumer les corps, dont par thanatopraxie, par exemple en attente d'un enterrement ;
- pour produire des polymères et des produits chimiques (plus de 50 % du total des usages du méthanal) ;
- Utilisé également pour coller les tapisseries ;
- Il a été utilisé pour la conservation de la viande[réf. nécessaire] ;
- inhibiteur de corrosion dans l'industrie d'extraction du gaz de schiste, où le méthanal est dilué dans un mélange d'eau, à d'autres produits chimiques et de sable, pour l'injection dans les puits d'extraction du gaz de schiste comme liquide d'hydrofracturation.
Combiné au phénol (pour fabriquer des phénoplastes), à l'urée ou à la mélamine (fabrication d'aminoplastes), le méthanal forme des résines thermodurcissables.
Ces résines sont souvent utilisées dans les colles permanentes, comme celles utilisées dans la fabrication d'agglomérés, de contreplaqués, de la laine de verre, de tapis, ou bien pour former des mousses synthétiques.
On emploie le méthanal pour produire de nombreux autres produits chimiques, dont la plupart sont des polyols comme le pentaérythritol, utilisé dans la fabrication de peintures et d'explosifs. On compte aussi d'autres dérivés du méthanal comme le méthylène diphényle diisocyanate, un constituant important des peintures et des mousses de polyuréthane, ainsi que l'hexaméthylènetétramine, utilisée dans les résines phénol-méthanal et pour fabriquer du RDX (un explosif).
Réglementation
Plusieurs pays européens limitent ou interdisent l'utilisation de formaldéhyde (dont en thanatopraxie). L'importation de produits traités au formaldéhyde est alors soumise à réglementation ou interdiction.
Concernant les produits biocides (dont phytopharmaceutiques), sous le nom de formaldéhyde :
- pour l’Union européenne : cette substance active est interdite par la décision 2007/442/CE à la suite de l'examen relatif à l'inscription à l’annexe I de la directive 91/414/CEE[13] ;
- pour la France : cette substance active n'est pas autorisée dans la composition de préparations bénéficiant d’une autorisation de mise sur le marché. Les produits contenant du formaldéhyde ont un délai à la distribution fixé au 30 juin 2008, et un délai à l'utilisation fixé au 20 décembre 2008, par l'avis paru au Journal officiel du 31 octobre 2007.
Perspectives :
- l'Union européenne envisage une interdiction complète de l'utilisation du formaldéhyde en tant que biocide (y compris pour l'embaumement) en vertu de la Directive relative aux produits biocides (98/8/EC)[14],[15], mais certains pays où la thanatopraxie s'est développée (Irlande et quelques autres pays froids) ont manifesté des réserves à une telle interdiction. Malgré des rapports allant dans le sens d'une interdiction[16], aucune décision quant à l'inclusion du formaldéhyde dans l'annexe I de la directive pour les produits biocides du type 22 (fluides d'embaumement et pour la taxidermie) n'avait été prise en septembre 2009[17].
- La France, pour se mettre en conformité avec le droit européen et les recommandations de l'OMS, soumet à consultation en juin 2010 un projet de décret relatif à des valeurs-guides[18], après avis de l'Agence française de sécurité sanitaire de l'environnement et du travail. Il concerne les gestionnaires de certains établissements recevant du public (enseignement, accueil d'enfants de moins de six ans, établissements sanitaires et sociaux disposant d'une capacité d'hébergement, établissements sportifs couverts) et devrait entrer en vigueur le 1er janvier 2015 puis le 1er janvier 2022. Pour le décret, une valeur-guide pour l'air intérieur est « un niveau de concentration de polluants dans l'air intérieur fixé, pour un espace clos donné, dans le but d'éviter, de prévenir ou de réduire les effets nocifs sur la santé humaine, à atteindre, dans la mesure du possible, dans un délai donné. » La proposition[18] est :
- 30 μg/m3 en moyenne hebdomadaire à compter du 1er janvier 2015 ;
- 10 μg/m3 en moyenne hebdomadaire à compter du 1er janvier 2022.
Santé
Après avoir été d'abord considéré comme « cancérogène probable », le formaldéhyde a été classé comme « cancérogène certain » par le Centre international de recherche sur le cancer (CIRC), qui dépend de l'Organisation mondiale de la santé (OMS).
- Il est à l'origine de cancers du nasopharynx.
- Son implication dans les cancers des fosses nasales et des sinus est envisagée mais des biais de confusion présents dans les études en milieu professionnel ne permettent pas de pouvoir conclure[19]. En effet, les travailleurs exposés étaient en général exposés à un grand nombre de polluants potentiellement cancérogènes (poussières de bois dans l'industrie du bois – responsable de cancer des fosses nasales –, benzène – responsable de leucémies –, et d'autres aldéhydes comme l'acétaldéhyde) ; le rôle propre du formaldéhyde dans ces cancers est donc difficilement mis en évidence[20],[21].
- Son implication dans la survenue de leucémies est fortement suspectée[20].
Le formaldéhyde est employé dans nombre de matériaux synthétiques ; or ceux-ci relâchent au cours du temps des quantités non négligeables de formaldéhyde. Il s'agit d'un des polluants les plus répandus de l'air intérieur des habitations.
- Au-dessus d'une concentration de 0,1 mg/kg dans l'air, il peut irriter les yeux et les muqueuses, causant des conjonctivites, des maux de tête et des difficultés à respirer accompagnées de douleurs dans la gorge.
- Les animaux de laboratoire soumis à d'importantes doses de méthanal durant leur vie voient le risque de cancer du nez et de la gorge augmenter.
Toutefois, certaines études suggèrent que les concentrations de méthanal dans les bâtiments n'ont pas d'effet cancérogène : en effet, le potentiel cancérogène du formaldéhyde, à seuil, ne s'exprime que pour de très importantes concentrations (supérieures à 5 mg/m3), concentrations qui ne sont retrouvées qu'en milieu professionnel[22] et rarement dans l'habitat, où les taux moyens sont nettement plus bas (Exemple : moyennes françaises proches des 20 µg/m3, soit 250 fois moins que les taux déclenchant des cancers chez l'animal de laboratoire[23],[24].
- En dentisterie, les quantités faibles incorporées aux pâtes canalaires causent parfois des réponses allergiques graves (des cas d'urticaire et de réactions allergiques fortes allant jusqu'à l'œdème de Quincke, survenant dans les heures suivant l'introduction de la pâte dans les canaux dentaires, sont rapportées dans la littérature[25]).
Santé au travail
Le risque d'absorber du formaldéhyde semble plus élevé :
- dans la production de colles et de panneaux agglomérés, contreplaqués, de meubles et d’autres produits du bois recomposé ;
- dans la fabrication de diverses matières plastiques, certains fertilisants et résines utilisées dans les moules de fonderie en sable, ainsi que de certaines peintures et vernis ;
- parfois dans l’industrie du textile qui utilise ces résines comme apprêts pour rendre des tissus infroissables ;
- dans les processus de synthèse d'autres produits chimiques ;
- via l'utilisation de produits bactéricides en contenant (nombreuses formulations de produits désinfectants, de cosmétiques, de liquides d'embaumement et de solutions de conservation de tissus biologiques).
Voies d'exposition
En milieu de travail, l’exposition au formaldéhyde se produit par différentes voies.
Inhalation : le formaldéhyde gazeux est absorbé par les voies respiratoires. L’exposition professionnelle au formaldéhyde par inhalation provient principalement de trois types de sources :
- la décomposition thermique ou chimique des résines à base de formaldéhyde ;
- l’évaporation de formaldéhyde à partir de solutions aqueuses (par exemple, les liquides d’embaumement) ;
- la formation de formaldéhyde résultant de la combustion d’une variété de composés organiques (par exemple, via les gaz d'échappement).
Passage percutané et contact avec la peau.
- Ce risque est le plus élevé pour des métiers utilisant ou produisant des solutions aqueuses de formaldéhyde. Il cause des irritations, des dermites de contact (irritatives et allergiques).
Les symptômes sont des démangeaisons, des picotements et des rougeurs. Une sensibilisation cutanée est susceptible d’apparaître après un contact avec des solutions aqueuses de formaldéhyde de concentration égale ou supérieure à 2 %.
- Un contact fréquent avec des solides contenant du formaldéhyde libre ou avec des résines (surtout si elles sont mal polymérisées) peut entraîner une sensibilisation allergique. Ces effets sont a priori facilement évitables en protégeant les régions de la peau exposées, par exemple, en portant des gants et tenues appropriées.
Les effets sanitaires d'une exposition à cette substance varient selon la voie d’exposition et la concentration ou dose absorbée, et probablement selon l'âge du patient.
Lorsqu’une personne est sensibilisée, les manifestations de l’allergie cutanée (érythème) risquent de se produire à chaque contact avec des solutions de concentrations de plus en plus faibles (à partir de 0,5 % de formaldéhyde).
En situation d'accident, du formaldéhyde peut être présent dans l’air en fortes concentrations. Il constitue alors un danger immédiat considérable.
- Des concentrations égales ou supérieures à 20 ppm peuvent induire des œdèmes pulmonaires graves et éventuellement causer la mort.
- Par contact important et direct avec la peau, le formaldéhyde peut entraîner des lésions.
Alimentation
Le formaldéhyde peut être présent à faible dose dans l'alimentation humaine, comme additif (conservateur E240).
Prévention, traitement de l'air intérieur
 Le Chlorophytum, d'entretien facile, semble être un bon candidat pour épurer l'air intérieur du formaldéhyde (en faible quantité)
Le Chlorophytum, d'entretien facile, semble être un bon candidat pour épurer l'air intérieur du formaldéhyde (en faible quantité)
- Une ventilation suffisante et un renouvellement de l'air intérieur sont recommandés surtout dans les logements neufs ou contenant des planchers, murs ou plafonds ou meubles contenant de l'aggloméré, des moquettes ou dalles synthétiques collées.
- On commence à trouver sur le marché des colles, agglomérés et meubles ou planchers garantis sans formaldéhyde.
- Certaines plantes (chlorophytum par exemple) se sont montrées en laboratoire, dans le cadre du programme Phyt'air par exemple, capables de dégrader de façon modérée certains aldéhydes présents dans l'air intérieur.
Liens externes
- [PDF] INRS : Le point des connaissances sur le formaldéhyde, édition 2008 | Fiche toxicologique : Aldéhyde formique et solutions aqueuses, édition 2008
- Fiche internationale de sécurité (solution à 37 %)
- [PDF] Quelques guides et rapports sur le site www.irsst.qc.ca: [1], [2], [3], [4] et [5].
- Réactions allergiques au formaldéhyde en dentisterie
- (en) ChemSub Online : Formaldéhyde
- (en) How Senator Vitter Battled the EPA Over Formaldehyde's Link to Cancer
Notes et références
- FORMALDEHYDE et FORMALDEHYDE (SOLUTION A 37%, sans méthanol), fiches de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultées le 9 mai 2009
- Hazardous Substances Data Bank sur http://toxnet.nlm.nih.gov. Consulté le 17 septembre 2009
- (en) David R. Lide, Handbook of chemistry and physics, CRC, 16 juin 2008, 89e éd., 2736 p. (ISBN 142006679X et 978-1420066791), p. 9-50
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, 1997, 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, 2 et 3, Huston, Texas, Gulf Pub. Co., 1996 (ISBN 0-88415-857-8, ISBN 0-88415-858-6, ISBN 0-88415-859-4)
- (en) David R. Lide, Handbook of chemistry and physics, CRC, 2008, 89e éd., 2736 p. (ISBN 9781420066791), p. 10-205
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Évaluations Globales de la Cancérogénicité pour l'Homme, Groupe 1 : Cancérogènes pour l'homme » sur http://monographs.iarc.fr, CIRC, 16 janvier 2009. Consulté le 22 août 2009
- « Formaldéhyde » sur ESIS, consulté le 17 février 2009
- Entrée de « Formaldehyde solution » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 17 septembre 2009 (JavaScript nécessaire)
- « Formaldéhyde » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- 2007/442/CE: Décision de la Commission du 21 juin 2007 concernant la non-inscription de certaines substances actives à l’annexe I de la directive 91/414/CEE du Conseil et le retrait des autorisations de produits phytopharmaceutiques contenant ces substances [notifiée sous le numéro C(2007) 2576], Journal officiel no L 166 du 28/06/2007 p. 0016 - 0023.
- Directive 98/8/EC of the European Parliament and of the Council of 16 February 1998 concerning the placing of biocidal products on the market. OJEU L123, 24.04.1998, pp. 1–63. (consolidated version to 2008-09-26)
- Commission Regulation (EC) No 2032/2003 of 4 November 2003 on the second phase of the 10-year work programme referred to in Article 16(2) of Directive 98/8/EC of the European Parliament and of the Council concerning the placing of biocidal products on the market, and amending Regulation (EC) No 1896/2000. OJEU L307, 24.11.2003, p. 1–96. (consolidated version to 2007-01-04)
- Patel Alkesh ; Formaldehyde Ban set for 22 Sept 2007 Ed : WebWire ; Consulté 2007-07-04
- European chemical Substances Information System (ESIS) (Entry for formaldehyde), Consulté 2009-09-01
- Projet de décret relatif aux valeurs-guides pour l’air intérieur pour le formaldéhyde (PDF - 99 Ko)
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans. « Formaldehyde, 2-butoxyethanol and 1-tert-butoxypropan-2-ol », IARC Monogr Eval Carcinog Risks Hum. 2006;88:1-478.
- Cogliano VJ, Grosse Y, Baan RA, Straif K, Secretan MB, El Ghissassi F; Working Group for Volume 88. « Meeting report: summary of IARC monographs on formaldehyde, 2-butoxyethanol, and 1-tert-butoxy-2-propanol », Environ Health Perspect, 2005 Sep;113(9):1205-8.
- ARC, Monographie Volume 62 (1995) Wood Dust and Formaldehyde
- « Toxicological Assessment of Formaldehyde » (pdf), Opinion of BfR No. 023/2006, 30 mars 2006
- Dassonville C, Demattei C, Laurent AM, Le Moullec Y, Seta N, Momas I. « Assessment and predictor determination of indoor aldehyde levels in Paris newborn babies' homes », Indoor Air. 2009 Aug;19(4):314-23. Epub 2009 Jan 19.
- Rapport final de l'Observatoire de la qualité de l'air intérieur, novembre 2006 (pdf).
- Bibliographie - Réactions allergiques - pâtes d'obturation canalaire contenant du formaldéhyde - 1
Catégories :- Produit chimique toxique
- Produit chimique corrosif
- Cancérogène chimique
- Aldéhyde
Wikimedia Foundation. 2010.