- Pentaérythritol
-
Pentaérythritol 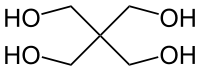
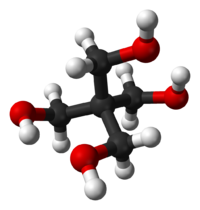
Général Nom IUPAC 2,2-bis(hydroxyméthyl)propane-1,3-diol Synonymes 2,2-bis(hydroxyméthyl)-1,3-propanediol
pentaérythrite
auxinutrilmaxinutril
monopentek
penetek
pentek
metab-Auxil
hercules P6
pentaerythrital
monopentaérythritol
tétraméthylolméthane
THME
PETPNo CAS No EINECS No RTECS PubChem SMILES InChI Propriétés chimiques Formule brute C5H12O4 [Isomères] Masse molaire[1] 136,1464 ± 0,006 g·mol-1
C 44,11 %, H 8,88 %, O 47,01 %,Propriétés physiques T° fusion 253 à 258 °C[2] T° ébullition 276 °C à 30 mmHg[2] Solubilité 5.6 g/100 mL à 15 °C dans l'eau, soluble in méthanol, éthanol, glycérol, éthylène glycol, formamide, insoluble in acétone, benzène, paraffine, éther, CCl4 Point d’éclair >150 °C[2] Pression de vapeur saturante <1 mmHg à 20 °C[2] Thermochimie Cp Unités du SI & CNTP, sauf indication contraire. Le pentaérythritol est un composé organique de formule semi-développée C(CH2OH)4. ce polyol blanc et cristallin avec un squelette néopentane est une brique versatile pour la préparation de beaucoup de composés multifonctionnalisés comme l'explosif PETN ou le tétraacrylate de pentaérythritol[4]. Les dérivés du pentaérythritol sont des composants des résines glycéro, tackifiantes, des vernis, des stabilisateurs du PVC, des esters de tallöl (en)[5] et des antioxydants d'oléfines
Les esters du pentaérythritol sans halogène sont aussi une alternative plus respectueuse de l'environnement que les autres liquides de transformateurs électriques en étant à la fois vraiment biodégradables et non dangereux dans l'eau. Ils replacent avantageusement les polychlorobiphényles (PCB) et même les liquides à base de silicone ou les hydrocarbures fluorés, comme fluides diélectriques dans les transformateurs. Leur faible volatilité et leur haut point éclair leur donne une excellente résistance à la inflammation en cas de panne d'électricité majeure et de rupture de transformateur.
Synthèse
Le pentaérythritol peut être préparé par condensation d' acétaldéhyde et de formaldéhyde en milieu basique[6]. Le processus inclut des aldolisations successives suivie d'une réaction de Cannizzaro. Les impuretés produites sont le dipentaérythritol et le tripentaérythritol[7]:
- 2 CH3CHO + 8 CH2O + Ca(OH)2 → 2 C(CH2OH)4 + (HCOO)2Ca
Notes
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Pentaerythritol » (voir la liste des auteurs)
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Pentaerythritol sur Sigma-Aldrich
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 2, Huston, Texas, Gulf Pub. Co. (ISBN 0-88415-858-6)
- S. F. Marrian,The Chemical Reactions of Pentaerythritol and its Derivatives, Chemical Reviews, 1948, vol. 43(1), pp. 149–202. DOI:10.1021/cr60134a004.
- définition tallöl sur Larousse.fr
- H. B. J. Schurink (1941). "Pentaerythritol". Org. Synth.; Coll. Vol. 1: 425.
- M. S. Peters, J. A. Quinn, Pentaerythritol Production Yields, Industrial & Engineering Chemistry, 1955, vol. 47(9), pp. 1710–1713. DOI:10.1021/ie50549a016.
Wikimedia Foundation. 2010.



