- Ozonolyse
-
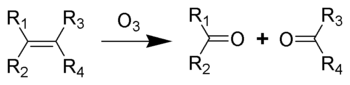
Une ozonolyse est la réaction d'un alcène avec une molécule d'ozone.
Sommaire
Historique
La réaction d'ozonolyse a été découverte par Harries en 1903. Elle a été largement utilisée pour localiser la position des doubles liaisons des composés éthyléniques dans les molécules organiques. Maintenant des techniques spectroscopiques permettent des analyses plus poussées avec des quantités de produit plus faibles, et sans dégradation. Cette réaction sert en synthèse organique, pour transformer des alcènes en cétone/aldéhyde/acide carboxylique/alcool.
Mécanisme
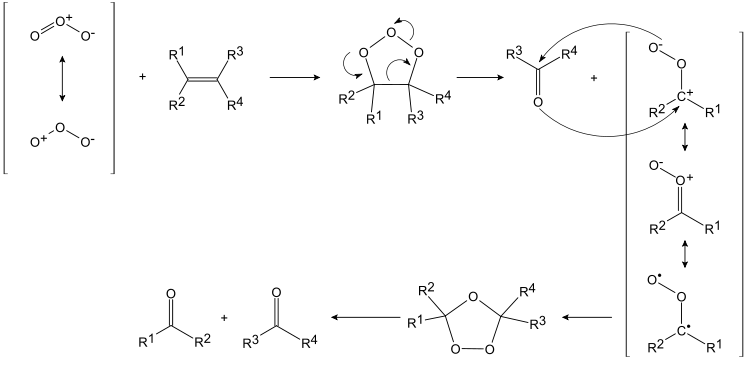
Le mécanisme de la réaction a été proposé par Rudolf Criegee en 1953,[1],[2],[3]. Il est le suivant :
La molécule d'ozone s'attache sur les carbones impliqués dans une double liaison carbone-carbone pour donner un molozonide, ou ozonide primaire. Cette réaction est une cycloaddition 1,3.
Ce molozonide, très instable, se scinde en deux molécules qui réagissent l'une sur l'autre pour donner un ozonide secondaire.
L'ozonide, explosif, est en général traité aux environs de -80 °C (193 K), et se sépare en deux cétones ou aldéhydes, en fonctions des substituants initiaux de l'oléfine, ainsi qu'un atome d'oxygène (qui pourra réagir avec les autres produits de réaction s'il n'est pas capté, par du diméthylsulfure, par exemple, qui sera oxydé en diméthylsulfoxyde (DMSO)).
Les réactions sont celles de réduction avec des catalyseurs de type hydrogène H2 ou platine Pt (métal), ou d'oxydation avec du peroxyde d'hydrogène/eau oxygénée H2O2.
Précaution
L'ozone est un composé assez dangereux. D'une part il est toxique, et d'autre part explosif. Il faut donc veiller à l'utilisation d'une sorbonne bien ventilée, et capter les effluents à la source pour destruction. D'autre part, concernant le caractère explosif, il ne faut pas avoir de haute concentration en ozone, et donc éviter de trop refroidir le milieu réactionnel, ce qui a pour effet d'augmenter la solubilité de l'ozone dans le solvant (voire de liquifier l'ozone, explosion assurée).
Ozonolyse des élastomères
C'est le "craquelage d'élastomères par l'ozone", qui même à l'état de traces dans une atmosphère (urbaine ou industrielle notamment) va attaquer et casser certaines liaisons chimiques qui permettaient la cohésion d'élastomères sensibles, dont le caoutchouc naturel (latex polymérisé), le polybutadiène, styrène-butadiène et le caoutchouc nitrile. Le craquelage par l'ozone crée de petites fissures typiques, à angle droit par rapport à la surface du polymère exposée au gaz. Les fissures croissent régulièrement et l'attaque se poursuit d'autant plus vite que des contraintes (tensions, compression ou tractions) sont exercées sur le polymère (pneu de vélo par exemple). Des additifs sont ajoutés au caoutchouc pour limiter le craquelage par l'ozone.
Le craquelage par l'ozone est un problème grave quand il affecte par exemple les durites ou conduites de carburants. Dans ce dernier cas, des fuites de gaz ou carburant peuvent conduire à des incendies ou des déversements de produits toxiques (essence, fuel dans le cas des véhicules). Le craquelage par l'ozone était autrefois communément observée dans les flancs des pneus, et l'est encore sur les pneus de cycles de mauvaise qualité. Il a été supprimé par des additifs dits "antiozonants", ou quand les teneurs en ozone ou la pollution de l'air par l'ozone est trop importante, on a remplacé les caoutchoucs sensibles par d'autres élastomères résistants tels que le polychloroprène, EPDM ou le Viton (fluoroélastomère). Les tapis monte charge en caoutchouc, les courroies de caoutchouc et autres tuyaux en certains élastomères sont particulièrement vulnérables à ce caquelage lorsqu'ils sont stockés ou utilisés près de machines électriques ou d'alternateurs produisant de l'ozone.
Voir aussi
Articles connexes
Bibliographie
Liens externes
Notes et références
- Criegee, R., « Mechanism of Ozonolysis », dans Angew. Chem. Int. Ed. Engl., vol. 14, 1975, p. 745–752 [lien DOI]
- http://www.organic-chemistry.org/namedreactions/ozonolysis-criegee-mechanism.shtm Ozonolysis mechanism on Organic Chemistry Portal site
- Li, Jie Jack: Criegee mechanism of ozonolysis Book: Name Reactions. 2006, 173-174, DOI:10.1007/3-540-30031-7_77
Catégories :- Réaction d'oxydo-réduction organique
- Test chimique
- Cycloaddition
Wikimedia Foundation. 2010.