- Xanthotoxine
-
Xanthotoxine 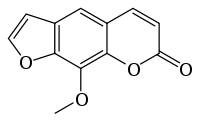
Général Nom IUPAC 9-m"thoxy-7H-furo[3,2-g]chromén-7-one Synonymes xanthotoxine, méthoxsalène, 8-méthoxypsoralène No CAS No EINECS No RTECS Code ATC AD02
BA02DrugBank PubChem SMILES InChI Propriétés chimiques Formule brute C12H8O4 [Isomères] Masse molaire[1] 216,1895 ± 0,0114 g·mol-1
C 66,67 %, H 3,73 %, O 29,6 %,Propriétés physiques T° fusion 148 à 150 °C[2] Solubilité 47,6 mg·l-1 (eau, 30 °C)[3] Précautions Directive 67/548/EEC[2],[4] 
XnPhrases R : 22, 41, 43, 45, 46, Phrases S : 20, 26, 36/39, 45, 53, SGH[2] 
Écotoxicologie DL50 423 mg·kg-1 (souris, oral)[5]
860 mg·kg-1 (souris, s.c.)[6]
250 mg·kg-1 (souris, i.p.)[5]LogP 2,140[3] Données pharmacocinétiques Demi-vie d’élim. ~2 heures Unités du SI & CNTP, sauf indication contraire. La xanthotoxine ou méthoxsalène (vendue sous les noms d'Oxsoralène, Deltasoralène, Méladinine, Uvadex) est un composé organique de la famille des furocoumarines. C'est le dérivé 8-méthoxylé du psoralène. Elle est utilisée comme traitement de certaines maladies de peau.
Sommaire
Occurrence naturelle
La xanthotoxine est naturellement présente dans une plante médicinale africaine, le fagarier (Fagara xanthoxyloïdes) ainsi que dans nombreuses plantes de la famille des Apiacés, notamment l'ammi élevé (Ammi majus) dont elle est extraite, l'angélique, le panais, la berce du Caucase, ou encore de la famille des Rutacées comme la bergamote.
Biosynthèse
La xanthotoxine est produite par une voie spécifique, la voie des furocoumarines linéaires[7] permettant de former les furocoumarines telles que le psoralène et ses dérivés à partir de l'ombelliférone, elle même biosynthétisée selon la voie des phénylpropanoïdes, et du pyrophosphate de diméthylallyle, obtenu lui par la voie du mévalonate.
Synthèse de l'ombelliférone
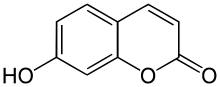
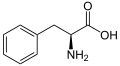
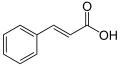
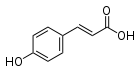
L'ombelliférone est une coumarine, l'un des nombreuse sous-famille des phénylpropanoïdes et est donc biosynthétisée comme ces dernier à partir de la L-phénylalanine selon la voie des phénylpropanoïdes (ou voie du shikimate). La phénylalanine est dans un premier temps transformée en acide cinnamique par l'action de la phénylalanine ammonia-lyase (PAL), celui-ci étant ensuite hydroxylé en acide paracoumarique par l'action de la cinnamate 4-hydroxylase (C4H). Ce dernier est une nouvelle fois hydroxylé par l'action de la cinnamate/coumarate 2-hydroxylase (C2H) pour former l'acide 2,4-dihydroxycinnamique, puis par une rotation de la liaison insaturée adjacente au groupe carboxyle de ce dernier. La réaction s'achève par une estérification intramoléculaire, le groupe hydroxyle en C2' étant attaqué par le groupe carboxyle, formant un cycle de lactone.
Synthèse de la xanthotoxine
La biosynthèse continue ensuite par l'activation du pyrophosphate de diméthylallyle (DMAPP), produit selon la voie du mévalonate, formant un carbocation par clivage du diphosphate. Une fois activé, l'enzyme ombelliférone 6-prényltransférase catalyse la C-alkylation entre le DMAPP et l'ombelliférone sur la position activée, en ortho du phénol, menant à la formation de la déméthylsubérosine. Cette réaction est suivie par une hydroxylation catalysée par l'enzyme marmésine synthase formant la marmésine, suivie d'une seconde hydroxylation avec départ d'acétone catalysée par la psoralène synthase formant le psoralène. Le psoralène est ensuite transformée par l'action de la psoralène 8-monooxygénase formant le xanthotoxol. Ce dernier voit son groupe phénol méthylé par réaction avec le S-adénosylméthionine, réaction catalysée par la xanthotoxol O-méthyltransférase formant la xanthotoxine[8].
Traitement des maladies de peau
De part sa capacité photosensibilisatrice de la peau (qu'elle partage avec les autre furocoumarines), la xanthotoxine est utilisée, accompagnée de l'exposition de la peau au soleil, comme médicament dans le traitement de maladies de peau telles que le psoriasis, l'eczéma ou le vitiligo et contre certains lymphomes cutanés. La xanthotoxine modifie la façon dont les cellules de la peau reçoivent les UV-A, ce qui permettrait de supprimer la maladie. On prescrit en général une dose de 10 mg de xanthotoxine à prendre avant un traitement PUVA (psoralène + UV-A) de 30 mg / 75 minutes.
Risques
Les personnes avec une pression artérielle élevée ou un historique de problèmes hépatiques risques à son contact des inflammations et des dommages irréversibles au foie et à la peau. Les effets secondaire comprennent des nausées, maux de tête, étourdissements et dans des rares cas des insomnies.
La xanthotoxine est toxique pour les animaux à sang froid.
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Fiche Sigma Aldrich, consultée le 15 juin 2011
- (en) « Methoxsalen » sur ChemIDplus, consulté le 15 juin 2011
- Fiche Alfa Aesar 15 juin 2011, consultée le
- Drug and Chemical Toxicology. Vol. 2, Pg. 309, 1979
- Drugs in Japan Vol. 6, Pg. 837, 1982
- linear furanocoumarin biosynthesis
- P. M. Dewick, Medicinal Natural Products: A Biosynthetic Approach, John Wiley & Sons, 2009, 3rde éd., p. 161, 164–165
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Methoxsalen » (voir la liste des auteurs)
Catégories :- Produit chimique nocif
- Cancérogène chimique
- Produit chimique mutagène
- Furocoumarine
- Méthoxybenzène
Wikimedia Foundation. 2010.