- Radiothérapie
-
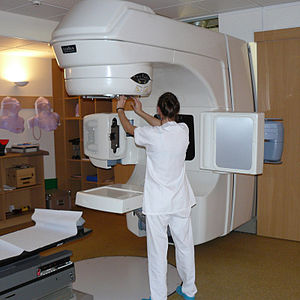
 Pour les articles homonymes, voir Radio.Accélérateur linéaire de radiothérapie Varian-Clinac 2100 C/D dans le Centre azuréen de cancérologie, Mougins, France
Pour les articles homonymes, voir Radio.Accélérateur linéaire de radiothérapie Varian-Clinac 2100 C/D dans le Centre azuréen de cancérologie, Mougins, France
La radiothérapie est une méthode de traitement locorégional des cancers, utilisant des radiations pour détruire les cellules cancéreuses en bloquant leur capacité à se multiplier. L'irradiation a pour but de détruire toutes les cellules tumorales tout en épargnant les tissus sains périphériques.
La radiothérapie est utilisée chez plus de la moitié des patients ayant un cancer. Elle est, avec la chirurgie, le traitement le plus fréquent des cancers et peut entraîner une guérison à elle seule. Elle peut être utilisée seule ou associée à la chirurgie et à la chimiothérapie. Ses indications sont liées au type de la tumeur, à sa localisation, à son stade et à l'état général du patient. Elle peut être faite en ambulatoire, c’est-à-dire sans hospitalisation, car les séances sont de courte durée et les effets secondaires moindres que lors d'une chimiothérapie.
On distingue quatre grandes techniques de radiothérapie :
- La radiothérapie externe : c'est la plus connue et la plus utilisée, la source de rayonnement est à l'extérieur du malade. Les bombes au cobalt, qui utilisent une source radioactive γ de cobalt 60, ont pratiquement disparu, au moins dans les pays développés, au profit des accélérateurs de particules de rayonnement X haute énergie et faisceaux d'électrons. Il existe trois techniques principales : la radiothérapie conventionnelle, la radiothérapie conformationnelle et la tomothérapie ou radiothérapie hélicoïdale, mais qui est peu répandue.
- La curiethérapie : la source radioactive est placée pendant une durée limitée (le plus souvent quelques heures) ou définitivement, à l'intérieur du malade, dans la tumeur ou dans une cavité à son contact. Trois techniques principales, elles-mêmes se subdivisent en sous-techniques suivant leur débit de dose (bas débit et haut débit) et leur type de chargement (manuel ou différé). Il s'agit de la curiethérapie interstitielle, la curiethérapie endocavitaire et la curiethérapie endoluminale.
- La radiothérapie métabolique vectorielle : la source radioactive est liquide, injectable, non scellée, et va se fixer sur les cellules cibles.
- La radiochirurgie : proche de la radiothérapie externe, son principe et ses indications sont cependant différents des autres techniques de radiothérapie en se rapprochant de ceux de la chirurgie, elle utilise un ou plusieurs faisceaux ultra-focalisés. Trois types d'appareillage sont utilisés : le Gamma-Knife, le Novalis, et l´accélérateur adapté avec micro-multilames.
Sommaire
Histoire
En médecine, la radiothérapie est utilisée comme traitement contre le cancer depuis plus de 100 ans. La radiothérapie s’est développée à partir du début du 20e siècle, surtout grâce au travail innovateur de Marie Curie (1867-1934), récipiendaire du Prix Nobel de physiologie ou médecine, qui a découvert deux éléments radioactifs, le Polonium et le Radium, en 1898. Ces découvertes marquèrent le début d’une nouvelle ère en médecine et en recherche médicale. Jusqu’au milieu des années 1900s, le Radium été utilisé sous plusieurs formes, jusqu’à ce que le Cobalt et le Césium commencèrent à être utilisés. Les accélérateurs linéaires étaient sont utilisés comme source de radiation depuis la fin des années 1940s.
Avec l’invention de la tomodensitométrie (Anglais : computed tomography ou CT-Scan) en 1971 par Godfrey Hounsfield, la planification des traitements de radiothérapie en trois-dimensions devint possible, ce qui représenta une avancée majeure par rapport aux traitements en deux dimensions. Les traitements basés sur la tomodensitométrie permet aux radio-oncologues de déterminer plus précisément la distribution de la dose de radiation en utilisant les images tomodensitométriques de l’anatomie du patient.
L’arrivée de nouvelles technologies d’imagerie, comme l’imagerie par résonance magnétique (IRM) dans les années 1970s et la tomographie par émission de positons (TEP) dans les années 1980s, a permis de passer de passer de la radiothérapie conformationnelle 3D à la radiothérapie conformationnelle avec modulation d’intensité (RCMI) et la radiothérapie guidée par l’image (IGRT) qui permet de contrôler la position exacte de la zone à traiter d’une séance à l’autre. Ces avancées scientifiques et technologiques ont permis aux radio-oncologues de visualiser et de traiter plus efficacement les tumeurs, ce qui se traduit par un meilleur pronostic des patients, une meilleure préservation des organes et moins d’effets secondaires.
Indication
En fonction du type de la tumeur, de sa localisation, de sa taille, de son extension et de son stade, de l'état général du patient et des symptômes associés, on distingue trois situations très différentes dans lesquelles on va utiliser la radiothérapie dans des buts bien précis :
Radiothérapie curative
Comme son nom l'indique, l'objectif est d'irradier toutes les cellules cancéreuses afin d'entraîner le contrôle voire la guérison du cancer. Cela implique l'absence de lésions à distance. Elle est indiquée dans environ la moitié des irradiations. Elle peut être utilisée seule ou en association avec la chirurgie ou la chimiothérapie.
La dose nécessaire dépend du type et du volume de la tumeur, certaines étant très radiosensibles alors que d'autres sont radiorésistantes. Il faut veiller à ce que la dose permettant le contrôle tumoral soit inférieure à la dose de tolérance critique des organes, ce qui implique une technique rigoureuse au risque de ne pas délivrer une dose suffisante et d'avoir une récidive locale ou au contraire de délivrer une dose excessive et d'entraîner un effet secondaire. Le protocole habituel délivre une dose de 10 Gy par semaine à raison de 5 séances de 2 Gy par jour. La dose totale varie selon les cas de 30 à 70 Gy.
Radiothérapie palliative
L'objectif n'est pas ici de guérir le cancer mais de soulager le patient par de légères doses, permettant d'atténuer la douleur résultant de cancer trop avancé pour être soigné.
Elle s'adresse aux cancers trop évolués localement ou métastatiques.
Le traitement étant palliatif, il doit être de courte durée et peu agressif, pour entraîner le moins de désagréments possible au patient. Par exemple, l'irradiation de type "split-course", permet de récupérer entre 2 séries d'irradiations.
Radiothérapie symptomatique
Son objectif est de soulager un symptôme majeur particulièrement gênant pour le malade. Son efficacité est :
- Antalgique : L'effet antalgique de l'irradiation est quasiment constant et se manifeste rapidement en quelques jours. Elle est souvent utilisée dans les douleurs des métastases osseuses. La disparition de la douleur se produit dès les premières séances, après parfois une recrudescence douloureuse due à l'inflammation radio induite.
- Hémostatique : Dans le cas des hémorragies persistantes que l'on retrouve parfois dans des cancers du rectum, de la vessie, ORL ou gynécologiques, quelques séances de radiothérapie entrainent l'assèchement et l'arrêt du saignement.
- Décompressive : Dans les cancers avec signes de compression médullaire - qui constituent une urgence, ou radiculaire, la radiothérapie peut être un traitement efficace, à condition de la commencer dès les premiers signes de compression. Elle doit être de courte durée, souvent juste quelques séances afin de limiter l'irradiation vertébrale. De plus, les œdèmes par compression veineuse ou lymphatique sont également bien améliorés par la radiothérapie.
Application
Selon la localisation et le stade des tumeurs, la radiothérapie peut être utilisée seule, mais elle est le plus souvent combinée avec un traitement chirurgical et/ou une chimiothérapie et/ou une hormonothérapie.
La plupart des cancers peuvent être traités par radiothérapie dans une certaine mesure. Ceci inclut les cancers du sein, de la prostate, du poumon, du rectum etc.
Cette thérapie est, la plupart du temps, appliquée pour traiter une région localisée autour d'une tumeur. Le champ des radiations couvre souvent aussi le réseau lymphatique drainant la tumeur.
Afin d'atteindre la zone tumorale et ses extensions éventuelles sans porter atteinte aux tissus sains environnants, on irradie la cible successivement selon différents angles, de telle sorte que les champs d'irradiation se superposent sur la région à traiter. Le maximum de radiation est alors localisé à la zone tumorale.
Avant le développement des médicaments immunosuppresseurs, cette technique était utilisée pour prévenir les réactions immunitaires indésirables lors de transplantations d'organes.
Dosage
La dose de radiations délivrée en radiothérapie se mesure en gray (Gy). Le médecin radiothérapeute prescrit une dose à délivrer dans une région donnée, en général la tumeur, ainsi que le fractionnement à utiliser c'est-à-dire la dose par séance. Il définit le cas échéant les contraintes de dose à ne pas dépasser dans les régions avoisinantes appelées organes à risques.
La dose prescrite et son fractionnement dépendent de la localisation et de la nature de la maladie. Généralement une dose de 45 à 80 Gy est délivrée à la cible par fraction de 2 Gy/jour. Le sein est par exemple traité par des doses de 45 à 50 Gy et les tumeurs pulmonaires par des doses supérieures à 65 Gy. La dose peut être délivrée par des faisceaux de photons ou d'électrons d'énergie comprise entre 1,25 MeV (bombe au cobalt) et plusieurs MeV pour les accélérateurs linéaires. Plus rarement les neutrons, les protons, les pions ou encore des photons d'énergie plus basse sont également utilisés.
Le radiophysicien propose alors une planification du traitement qui sera validée ensuite par le radiothérapeute. Il s'agit d'établir le nombre et la disposition des faisceaux qui vont permettre de délivrer la dose à la cible en limitant la dose délivrée aux tissus sains.
Voici les doses maximales admissibles de certains organes:
- Moelle épinière : 45 Gy ;
- Tronc cérébral : 54 Gy ;
- Chiasma optique : 54 Gy ;
- Nerf optique : 60 Gy ;
- Cerveau : 60 à 70 Gy ;
- Parotides : 40 à 60 Gy ;
- Larynx : 60 à 64 Gy ;
- Poumons: 20 Gy ;
- Foie : 20 Gy ;
- Os : 50 Gy ;
- Prostate : 75-80 Gy ;
- Cœur : 45-50 Gy ;
- Cristallin : 12 Gy ;
- Thyroïde : 20 Gy.
Surveillance
Comme tout traitement une surveillance s'impose. Elle doit s'assurer :
- de la bonne réalisation technique de l'irradiation,
- de la bonne tolérance du patient, jugée sur la clinique essentiellement, en surveillant l'apparition d'effets secondaires,
- de la bonne efficacité du traitement, jugée sur la clinique et les examens complémentaires.
Contrôle des conditions techniques de l'irradiation
- Le bon fonctionnement du générateur de rayonnement est contrôlé par les ingénieurs, le technicien biomédical ou le radiophysicien du service de radiothérapie ; le contrôle périodique des doses qu'il délivre est effectué par le radiophysicien. Le détail de ces contrôles obligatoires est rédigé par l'Afssaps
- Le bon positionnement du malade et du faisceau est contrôlé par le manipulateur en électroradiologie médicale et le radiothérapeute lors de la première séance de repérage.
- Les temps d'irradiation, les doses délivrées et les collimations sont programmés par le dosimétriste et le radiophysicien en coopération avec le radiothérapeute à l'aide d'outils informatiques.
- La bonne installation du malade sur la table et le suivi du traitement sont contrôlés à chaque séance par le manipulateur en électroradiologie médicale et, lors des consultations, par le radiothérapeute.
Surveillance clinique du patient
La surveillance du malade pendant toute la durée de la radiothérapie est assurée par le médecin radiothérapeute et par son médecin traitant. Elle a pour but essentiel de s'assurer de la bonne tolérance par le malade et de la bonne efficacité du traitement.
- Lors de la première consultation, particulièrement longue, le patient est informé de toutes les modalités techniques de la radiothérapie et des effets indésirables et secondaires à surveiller. Il est pesé et des conseils hygiéno-diététiques sont donnés. Une évaluation psychologique est faite et un suivi ou un traitement sont envisagés. Un traitement symptomatique est également prévu selon les cas - douleur, anxiété, troubles digestifs, amaigrissement ...
- Puis des consultations de suivi sont effectuées de façon hebdomadaire. Elles ont pour but notamment
- de soutenir le patient sur le plan psychologique de façon adaptée,
- d'apprécier la tolérance clinique, sur le plan général - poids, fatigue, état général et sur le plan locorégional - apparition de complications locales aigües,
- de suivre l'évolution de la lésion, grâce à la clinique et aux symptômes ou grâce à des examens complémentaires biologiques ou radiologiques,
- de suivre sur le plan hygiéno-diététique le patient.
- Parfois l'irradiation doit être interrompue en cas d'intolérance majeure.
- En fin de traitement, le radiothérapeute rédige un compte rendu complet précisant notamment la technique utilisée, les doses délivrées, les effets secondaires éventuellement rencontrés, la tolérance et l'efficacité. Ce compte rendu est adressé aux différents médecins responsables du patient.
Effets secondaires
Les effets secondaires peuvent être divers et variés suivant la localisation de l'irradiation. Dans tous les cas, on distingue la toxicité aiguë de la toxicité tardive.
La toxicité aiguë regroupe les conséquences qui se font ressentir dans les quelques jours après le traitement et jusqu'à 6 mois après. Elle touche surtout les tissus à renouvellement rapide comme la peau, les muqueuses, la moelle osseuse. La toxicité tardive regroupe les effets secondaires qui apparaitront entre 6 mois et 30 ans après la fin de l'irradiation. Elle est irréversible et touche essentiellement les tissus de soutien, avec développement d'une fibrose.
Ci-dessous, les effets secondaires en fonction des différents sites:
- Yeux :
- opacification du cristallin : cataracte induite à partir de 10 Gy
- la rétine est radio résistante (non sensible aux rayonnements ionisants)
- Si la dose est supérieure à 50 Gy, risque de nécrose de l'œil
- Au niveau ORL :
- toxicité aiguë : mucite[1] (irritation de la muqueuse), épithélite, agueusie
- toxicité tardive : xérostomie vers 30 à 40 Gy, nécrose osseuse, hypothyroïdie, risque dentaire
- Cheveux :
- Alopécie à 30 Gy, définitive à 40 Gy
- Œsophage :
- Œsophagite aiguë à 40 Gy, sténose tardive si plus de 60 Gy
- Poumons :
- toxicité aiguë : pneumopathie radique (toux, asthénie, dyspnée, état fébrile)
- toxicité tardive : insuffisance respiratoire, variable en fonction du volume pulmonaire irradié
- Cœur :
- toxicité aiguë : péricardite à partir de 50 Gy
- toxicité tardive : risque coronariens
- Intestin :
- toxicité aiguë : diarrhée, douleurs
- toxicité tardive : grêle radique si dose supérieure à 45 Gy
- Organes de reproduction :
- stérilité définitive ou temporaire possible en fonction de l'âge à partir de 6 à 12 Gy
- testicules:
- Oligospermie transitoire: 0.2 Gy
- Azoospermie transitoire: 2 Gy
- Azoospermie définitive: 6 Gy
- Ovaires:
- Stérilité temporaire: 3 Gy
- Stérilité définitive: 12 Gy
- Vessie :
- toxicité aiguë : pollakiurie, brulure mictionnelle
- toxicité tardive : fibrose de la vessie à partir de 60 Gy
- Reins :
- insuffisance rénale
- Moelle épinière :
- Myélite radique (exceptionnel)
- Peau :
- l'érythème apparaissant dans les deux semaines, suivi d'une desquamation sèche
- la radiodermite exsudative, formée de phlyctènes pouvant suinter
- la radionécrose aiguë, ulcération douloureuse
- toxicité tardive : l'atrophie, les troubles de la pigmentation, télangiectasies, scléroses.
En cas d'effet indésirable grave, un surdosage doit être évoqué, mais aussi une radiosensibilité individuelle augmentée (défaut de réparation de l'ADN).
Principe
Les radiations ionisantes (= transfert d'énergie dans un milieu créant des ionisations dans celui-ci), lors de la traversée de la matière vont avoir un certain nombre d'interactions avec les composants de celle-ci, noyaux et électrons. Elles vont transférer de l'énergie à ces composants et créer des ionisations dont la densité va dépendre de la nature de la particule (charge, masse au repos et énergie) et du milieu. Ceci va aboutir à des effets chimiques dans les molécules rencontrées et notamment au niveau de l'ADN, des protéines ... mais surtout au niveau des molécules d'eau aboutissant à la création de radicaux libres, espèces chimiques très réactives. La formation des radicaux libres va dépendre en partie de la concentration en oxygène du milieu. Ces radicaux libres vont interagir avec les autres molécules du milieu.
La cible finale de l'action directe des radiations ionisantes ou indirecte (par le biais des radicaux libres) expliquant leurs effets biologiques est l'ADN même si les phospholipides membranaires vont aussi participer aux lésions cellulaires. Les interactions des radicaux libres avec l'ADN vont induire des ruptures de la molécule.
Au niveau cellulaire, on pourra ainsi constater des lésions létales d'emblée ou des lésions sublétales susceptibles de provoquer la mort cellulaire en cas d'accumulation. Ces lésions consistent en des ruptures intéressant un seul brin de l'ADN (lésions sub-létales) ou les deux brins (souvent des lésions létales). Ces lésions seront ou non réparées en fonction de conditions cellulaires particulières et notamment en fonction de la position de la cellule dans son cycle multiplicatif (cycle cellulaire) et de la disponibilité d'enzymes de réparation pour le type de lésion induite, ou de son état métabolique (disponibilité en nutriments) . Il existe en effet au moins 5 systèmes de réparations des lésions simple-brin ou double-brin de l'ADN. En cas de non réparation, les cassures chromosomiques induites vont aboutir à des aberrations chromosomiques que l'on peut mettre en évidence notamment au niveau des lymphocytes par un simple caryotype (dosimétrie biologique).
Ce sont ces anomalies qui vont induire la mort cellulaire selon plusieurs modes : il existe normalement un contrôle avant la mitose (ou transition de la phase G2 à M(itose)). En cas de non conformité (aberrations chromosomiques, impossibilité d'assemblage du fuseau mitotique ...) la cellule peut connaître une apoptose ou mort cellulaire programmée. Un autre mode, le plus fréquent est induit par l'impossibilité de fixation ou de disjonction des chromosomes sur le fuseau mitotique. La cellule va alors connaître une mort mitotique. Bien entendu, les choses sont un peu plus compliquées notamment parce que les cellules vont aussi pouvoir relarguer des cytokines et qu'il peut exister une mort cellulaire de cellules voisines qui n'ont pas subi de lésions de leur ADN (effet dit bystander)probablement par activation des récepteurs de mort cellulaire (voie extrinsèque de l'apoptose).
Au niveau d'une tumeur ou des tissus sains, le point important va être la perte de capacité de division de cellules dites clonogéniques (que l'on pourrait aussi appeler cellules souches), cellules capables de générer tout un assortiment de cellules plus différenciées et/ou de se reproduire elles-mêmes. Dans certains cas, en effet, une cellule présentant des lésions de son ADN peut ne pas avoir totalement perdu sa capacité de division et elle pourra donner un clone limité de cellules qui, in fine, s'arrêteront de proliférer ou mourront de manière différée. Le résultat, en ce qui concerne la tumeur est quand même une mort cellulaire même si elle est différée. On pense ainsi qu'il faut détruire toutes ces cellules clonogéniques pour obtenir la stérilisation d'une tumeur. D'un autre côté, la cellule peut aussi ne pas avoir perdu sa capacité de multiplication et ne pas connaître de mort différée. Ceci explique la cancérogénèse induite par les radiations ionisantes.
En ce qui concerne les lésions des organes, on sépare les organes dont les cellules ont un turn over rapide (peau, muqueuse intestinale, moelle ...)dont les lésions vont être responsables des effets précoces (cytopénie, diarrhée, mucites ...) et ceux dont les cellules se multiplie peu ou pas qui seraient responsables des lésions tardives (derme, moelle épinière, système nerveux central, ...). En fait, si pour expliquer les radiolésions précoces survenant en cours de traitement il suffit de penser que les cellules en cours de prolifération sont tuées et que la cicatrisation se fait par entrée en prolifération des cellules souches, les lésions tardives sont le fait à la fois de la destruction de cellules clonogéniques à renouvellement lent mais aussi de processus de cicatrisation inappropriés notamment des lésions dites précoces, de phénomènes inflammatoires et du vieillissement physiologique des tissus. [2]
Implications
Notes et références
- En cas de radiothérapie de la tête et du cou, une mucite orale survient chez plus de 80% des patients. Elle apparait environ 1 à 2 semaines après le début du traitement et peut empêcher de boire ou de manger lorsqu'elle est sévère. Sa prévention repose sur les soins bucco-dentaires , l'hygiène bucco-dentaire et sur l'action de sucer des glaçons quelques heures en commençant quelques minutes avant le traitement (activité démontrée : Revue Prescrire, n°282, Avril 2007, mucites orales dues aux traitements anticancéreux)
- Eric J. Hall Amato J. Giaccia Radiobiology for the radiologist 6th edition Lippincott Williams & Wilkins 2006
Voir aussi
Liens internes
- Cancer
- Chimiothérapie
- Curiethérapie
- Collimateur multilames
- Hadronthérapie
- Oncologie chirurgicale
- Protonthérapie
- Radiochirurgie
- Radiomucite
- Syndrome d'irradiation aiguë
- Générateur de rayons X
- Télécobaltothérapie
Liens externes
- SFRO (Société Française de Radiothérapie Oncologique)
- SFjRO (Société Française des jeunes Radiothérapeutes Oncologues)
- PROS (Paediatric Radiation Oncology Society) : Société de Radiothérapie d'Oncologie Pédiatrique
- ASTRO (American Society for Therapeutic Radiology and Oncology): Société Américaine des Radiothérapeutes
- ESTRO (European Society for Therapeutic Radiology and Oncology): Société Européenne des Radiothérapeutes
- FNCLCC (Fédération Nationale des Centres de Lutte Contre le Cancer)
- SFPM (Société Française des Physiciens Médicaux)
- Radiation the cancer risk.
- RTOG (The Radiation Therapy Oncology Group): an organisation for radiation oncology research
- La radiothérapie des cancers, cours du Dr Bernard Gery, radiothérapeute, médecin spécialiste du Centre François Baclesse
- La radiothérapie, sur www.ligue-cancer.asso.fr
- La radiothérapie, sur infocancer.nexenservices.com
- Radiothérapie des cancers, Faculté de médecine de Strasbourg - Polycopié : Module 10 - Cancérologie clinique onco-hématologie - Année 2005-2006
- Radiothérapie Externe, sur www.radiotherapie-hegp.fr
- iLQ - Calculateur d'équivalence de dose
Littératures
Grand public
Professionnels
- Jean-Jacques Mazeron, Alain Maugis, Christian Barret et Françoise Mornex "Techniques d'irradiation des cancers La radiothérapie conformationnelle" édition Maloine ISBN 2-224-02811-3
Catégories :- Radioactivité
- Radio-Oncologie
- Spécialité médico-technique
- Physique médicale
Wikimedia Foundation. 2010.