- Hadrontherapie
-
Hadronthérapie
L'hadronthérapie est une méthode innovante radiothérapie pour le traitement du cancer . Elle est destinée à détruire les cellules cancéreuses radiorésistantes et inopérables en les irradiant avec un faisceau de particules. La radiothérapie conventionnelle utilise essentiellement des rayons X, l'hadronthérapie d'autres types de particules : des hadrons, notamment des protons (protonthérapie) et des particules de carbone.
Sommaire
Avantages
Les hadrons constituent les noyaux des atomes. Grâce à leur charge électrique ils peuvent acquérir de la vitesse grâce aux accélérateurs de particules et guidés par des faisceaux, ils se transforment en projectiles d'énergie. Cette énergie transférée à l'atome-cible provoque un dysfonctionnement qui conduit à la mort biologique des cellules touchées.
Les principaux avantages par rapport à la radiothérapie classique sont :
- une balistique plus précise. Pour irradier la zone cancéreuse, le rayonnement traverse les tissus en déposant une certaine énergie. Dans le cas des hadrons, le dépôt d'énergie en fonction de la profondeur de tissus traversé est plus "piqué" qu'avec les photons. Cette qualité balistique permet d'atteindre des cibles localisées en profondeur donc de traiter des tumeurs cancéreuses non opérables ou résistantes aux rayons X/Y, tout en épargnant mieux les tissus sains environnants. Les cellules touchées meurent 3 à 10 fois plus vite et grâce à l'imagerie en temps réel, le clinicien peut visualiser la zone traitée et utiliser le faisceau d'hadrons comme un nano-scalpel.
- un « effet biologique » supérieur à celui des photons (on parle d'effet biologique relatif). Les dégâts causés par un rayonnement hadronique sur les cellules tumorales sont supérieurs à ceux causés par photons en radiothérapie conventionnelle. Ainsi, par exemple, il devient possible de traiter une tumeur au cerveau en 90 secondes, ceci sans anesthésie et sans douleur.
Indications
On peut résumer les résultats des études cliniques par[1],[2] :
- Environ 1% des patients traités aujourd'hui avec des photons devrait certainement être traités avec des protons puisque les résultats sont meilleurs que ceux obtenus en radiothérapie conventionnelle
- Environ 12% des patients traités aujourd'hui avec des photons devrait profiter d'un traitement par proton mais d'autres études cliniques sont nécessaires pour quantifier, localisation par localisation, les avantages cliniques.
- Environ 3% des patients traités aujourd'hui avec des photons devrait profiter d'un traitement par carbone, mais de nombreuses autres essais d'escalade de dose et d'études cliniques sont nécessaires.
Comment ça marche ?
L'objectif consiste à irradier les cellules cancéreuses avec le faisceau de particules afin de les détruire, tout en épargnant au maximum les tissus sains environnants. Pour cela, il faut connaitre les interactions entre les particules et la matière. Les effets de ce rayonnement sur la matière sont mesurés par la dose (ou énergie déposée par unité de masse). Il s'agit donc de contrôler le faisceau d'irradiation de façon à ce que la dose déposée soit maximale à l'endroit de la zone tumorale et minimale ailleurs[3].
-
Les particules sont accélérées dans un cyclotron ou un synchrotron. Un synchrotron est nécessaire pour les ions de carbone. L'interaction des particules avec les tissus dépend de la vitesse de la particule : le dépôt d'énergie dans les tissus est inversement proportionnel au carré de vitesse. Dans la matière, les particules sont freinées de façon continue et d'autant plus fortement qu'elles pénètrent profondément. Tant qu'elles possèdent une vitesse élevée (énergie supérieure à 50 MeV/u), leur effet ionisant sur les tissus n'est que relativement faible. Ce n'est que vers la fin de leur parcours que la plus grande partie du dépôt d'énergie a lieu. À ce moment-là, ce dépôt augmente fortement sur une distance de quelques millimètres, pour ensuite diminuer rapidement. On appelle pic de Bragg le profil décrivant la dose déposée en fonction de la profondeur de tissu traversé. L'énergie de la particule à la sortie de l'accélérateur règle la profondeur de pénétration et la position du maximum d'effet. Ce comportement permet ainsi de déposer une dose très élevée à la tumeur tout en épargnant les tissus environnants et/ou les organes à risque. Cette propriété rend ce type de rayonnement plus précis que les photons (ou rayons X) utilisés en radiothérapie conventionnelle.
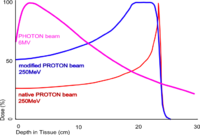 Courbe de rendement en profondeur des photons et des protons, remarquez le pic de Bragg (protons) très net : les protons déposent leurs énergies dans une petite fenêtre de profondeur.
Courbe de rendement en profondeur des photons et des protons, remarquez le pic de Bragg (protons) très net : les protons déposent leurs énergies dans une petite fenêtre de profondeur.
- Un autre avantage existe pour les ions carbone : la densité d'ionisation est élevée à la fin du parcours. Cela entraîne des dommages plus importants sur l'ADN des cellules cancéreuses, qui ont ainsi plus de mal à se réparer que les cellules saines se trouvant en amont. On considère que ce type de rayonnement est entre 1,5 et 3 fois plus efficace qu'un faisceau de photons (environ 1,1 pour les protons). On parle d'« effets biologiques relatifs ». Les rapports des dégâts entre hadron et photon sont complexes et dépendent de nombreux paramètres. La discipline étudiant ces effets est la radiobiologie.
Centres d'hadronthérapie par ions carbone dans le monde
Centres d'hadronthérapie par ion carbones dans le monde Nom Ville Pays Localisation Commentaire GSI Gesellschaft für Schwerionenforschung Darmstadt  Allemagne
AllemagneOpérationel HIT Heidelberger Ionenstrahlen-Therapie Heidelberg  Allemagne
AllemagneEn construction NIRS-HIMAC Heavy Ion Medical Accelerator in Chiba Chiba  Japon
JaponOpérationel HIBMC Hyogo Ion Beam Medical Center Hyogo  Japon
JaponOpérationel CNAO National Center of Oncological Adrotherapy Pavia  Italie
ItalieEn construction ETOILE Espace de Traitement Oncologique par Ions Légers dans le cadre Européen Lyon  France
FranceOuverture fin 2013 ARCHADE Advanced Resource Centre for HADrontherapy in Europe Caen  France
FranceOuverture d'un centre de recherche en 2011. MedAustron Austrian Ion Therapy & Cancer-Research Centre Project Wiener Neustadt  Autriche
AutricheEn projet Un nouveau centre d'hadronthérapie devrait ouvrir ses portes fin 2013 à Lyon[4].
Il a pour nom "ETOILE". Depuis l'annonce officielle du Ministre de la Santé en février 2007 le projet se concrétise. Un Groupement de Coopération Sanitaire (GCS) a été crée pour mener à bien ce projet vers la construction du " Centre Étoile" [1], qui sera ainsi le premier centre en France de traitement de cancer par hadronthérapie par ions carbone. Un centre de ressource en hadronthérapie s'ouvrira à Caen et sera dévolu à la R&D et viendra en soutien des centres accueillant des patients.
Quelques centres d'hadronthérapie par proton (protonthérapie) dans le monde
Références
- ↑ (en) R. Mayer et al., « Epidemiological aspects of hadron therapy: a prospective nationwide study of the Austrian project MedAustron and the Austrian Society of Radio-oncology », dans Radiother. Oncol., vol. 73, 2004, p. S24–8.
- ↑ (en) U. Amaldi et G. Kraft, « Radiotherapy with beams of carbon ions », dans Reports on Progress in Physics, vol. 68, 2005, p. 1861-82 [lien DOI].
- ↑ (en) O. Jäkel, « Hadron Therapy: Radiotherapy using Fast Ion Beams, in: Ion Beam Science, Part I », dans Matematisk-fysiske Meddelelser, vol. 52, no 1, 2006, p. 37-57 (ISSN 0023-3323).
- ↑ La création du centre d'hadronthérapie de Lyon confirmée, février 2007, Dépêche Le Progrès sur le site de l'Aderly. Consulté le 05/03/2007
Liens externes
- Portail de la physique
- Portail de la médecine
Catégories : Radio-Oncologie | Terme médical commençant par H
Wikimedia Foundation. 2010.
