- Dapsone
-
Dapsone 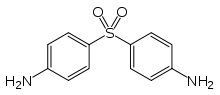
Général Nom IUPAC 4,4'-sulfonyldianiline No CAS No EINECS Code ATC J04 DrugBank PubChem SMILES InChI Apparence solide Propriétés chimiques Formule brute C12H12N2O2S [Isomères] Masse molaire[1] 248,301 ± 0,016 g·mol-1
C 58,05 %, H 4,87 %, N 11,28 %, O 12,89 %, S 12,91 %,pKa 2.41 Propriétés physiques T° fusion 175,5 °C Solubilité 380 mg·l-1 eau à 37 °C.
Sol dans acide chlorhydrique dilué, alcool, méthanol, acétone.Masse volumique 250 à 350 kg·m-3 Précautions Directive 67/548/EEC 
XnPhrases R : 22, Phrases S : (2), 22, SGH[3] 
AttentionClassification du CIRC Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[2] Écotoxicologie DL50 250 mg·kg-1 souris oral
225 mg·kg-1 souris i.v.
250 mg·kg-1 souris s.c.
313 mg·kg-1 souris i.p.Unités du SI & CNTP, sauf indication contraire. La dapsone (DDS) est un médicament antibiotique de la famille des sulfones.
Sommaire
Histoire
La dapsone, ou sulfone-mère, est synthétisée par E. Fromm et J. Witmann en 1908[4]. En 1937 Ernest Fourneau en France et G. Buttle au Royaume-Uni découvrent, indépendamment l’un de l’autre, l’action antibactérienne des sulfones[5] et deux ans plus tard, en 1939, Noël Rist démontre qu’elles sont efficaces, in vitro et in vivo, contre la tuberculose[6]. Mais les résultats sont peu satisfaisants sur l’homme. Les recherches se poursuivent donc, et c’est aux États-Unis, en 1943, que Guy Henry Faget, guidé par la parenté des bacilles de Koch et de Hansen, essaie les sulfones avec succès dans le traitement de la lèpre[7]. Une nouvelle étape est franchie en 1950, quand H. Floch et P. Destombes introduisent la dapsone à l'Institut Pasteur de Guyane[8]. Depuis lors, les sulfones sont devenus un des piliers du traitement de la lèpre[9].
Effets
La dapsone est principalement connue pour son effet antilépreux (étant associée en trithérapie à la rifampicine et à la clofazimine) ainsi que antidermatique.
Elle possède une activité bactériostatique (c'est-à-dire qu'elle empêche les bactéries de se multiplier, sans pour autant les tuer directement) contre Mycobacterium leprae (ou « bacille de Hansen ») permettant de stopper la lèpre et de limiter ses effets invalidants après 3 ans de traitement en moyenne. Elle possède aussi une action contre Toxoplasma gondii, Mycobacterium avium et Pneumocystis carinii (dans ce cas, également en prophylaxie (en tant qu'indication thérapeutique secondaire associée à la triméthoprime) pour les personnes atteintes du SIDA).
Associée à la pyrimethamine, elle est aussi employée en prophylaxie contre le paludisme dans les zones ou Plasmodium falciparum est chloroquinorésistant. La molécule de pyrimethamine est utilisée pour ses propriétés pharmacologiques primaires certaines et la dapsone pour ses propriétés secondaires certaines.
La résistance à ce médicament est très rare (1 à 2 % des souches de Mycobacterium leprae), et n'apparaît que dans des cas de traitement mal suivis, à dose trop faible, et trop longtemps. Son mécanisme d'action dans le traitement de la dermatite herpétiforme reste inconnu.
Contre-indications
- Hypersensibilité ou allergie à la famille des sulfones;
- Déficit en G6PD (Favisme);
- Drépanocytose;
- Thalassémie;
- Traitement en cours à la zidovudine.
Utilisation pratique
La dapsone se prend par voie orale, en une prise par jour. Il convient, avant de débuter le traitement, de faire un bilan biologique sanguin (la dapsone peut entraîner une anémie hémolytique, d'autant plus fréquente que la dose est élevée). Des prises de sang hebdomadaires doivent être faites, en particulier en début de traitement, pour dépister des effets secondaires et adapter la dose adéquate en conséquence.
Effets secondaires
- Anémie hémolytique;
- Ictere;
- Troubles digestifs (perte d'appétit, nausées, douleurs abdominales, vomissements, etc.);
- Picotements et sensation de froid dans les pieds et les mains;
- Fièvres passagères mais répétées;
- Vertiges;
- Très rarement
- Troubles neurologiques, allergie, anomalies de la formule sanguine;
- Pancréatite[10]
Autres informations
En Belgique, la dapsone fait partie des substances soumises à une règlementation spéciale de l'« Agence Fédérale des Médicaments et des Produits de Santé ». Aucun médicament contenant de la dapsone n'est mis sur le marché pharmaceutique; ils ne pourront être obtenus qu'en importation parallèle.
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme » sur http://monographs.iarc.fr, CIRC, 16 janvier 2009. Consulté le 22 août 2009
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- E. Fromm and J. Wittmann, Berichte Deutsch Chem. Ges., vol. 41, 1908, p. 2266.
- Ernest Fourneau, Thérèse et Jacques Tréfouël, Federico Nitti, Daniel Bovet, « Action antistreptococcique des dérivés sulfurés organiques », C. R. Acad. Sci., vol. 204, 1937, p. 1763.
G. Buttle, Y. Smith, G. Foster, « Treatment of streptococcal infections in mice with 4:4'diamino-dipheni-sulphone », Lancet, vol. 1, 1937, p. 133. - N. Rist, F. Bloch et al., « Action du p.aminophénylsulfamide et de la p.diaminodiphénylsulfone sur les cultures des bacilles tuberculeux des mammifères et des oiseaux », C. R. Soc. Biol., 1939
- G. H. Faget, R. C. Pogge, F. A. Johansen et al., « The Promin Treatment of Leprosy : A Progress Report », Pub. Health Rep., novembre 1943.
- H. Floch, P. Destombes, Bull. Soc. Pathol. Exot. Filiales, janvier 1951, vol. 44, n° 3-4, pp. 151-156.
- E. Bergogne-Bérézin, P. Dellamonica, « Histoire des antibiotiques », dans Antibiothérapie en pratique clinique, 2e éd., Masson, 1999, p. 3.
- CNRS - The Annals of pharmacotherapy ISSN 1060-0280 CODEN APHRER - 2003, vol. 37, no10, pp. 1438-1440 [3 page(s) (article)] (24 ref.)[(fr) lire en ligne]
Liens externes
Catégories :- Produit chimique nocif
- Aminobenzène
- Benzosulfone
- Antibiotique
Wikimedia Foundation. 2010.
