- Mélatonine
-
 Pour les articles homonymes, voir Melatonine.
Pour les articles homonymes, voir Melatonine.Mélatonine 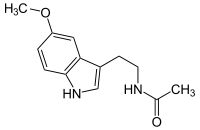
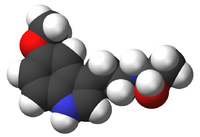
Structure de la mélatonine Général Nom IUPAC N-[2-(5-methoxy-1H-indol-3-yl)ethyl]
ethanamideSynonymes N-acetyl-5-methoxytryptamine ou Hormone du sommeil No CAS No EINECS Code ATC N05 DrugBank PubChem SMILES InChI Propriétés chimiques Formule brute C13H16N2O2 [Isomères] Masse molaire[1] 232,2783 ± 0,0125 g·mol-1
C 67,22 %, H 6,94 %, N 12,06 %, O 13,78 %,Propriétés biochimiques Codons UGG Données pharmacocinétiques Biodisponibilité 30 – 50 % Métabolisme hépatique via CYP1A2 mediated 6-hydroxylation Demi-vie d’élim. 35 à 50 minutes Excrétion Urine Unités du SI & CNTP, sauf indication contraire. La mélatonine, souvent dénommée hormone du sommeil, est surtout connue comme étant l’hormone centrale de régulation des rythmes chronobiologiques, et d’un certain point de vue, de pratiquement l’ensemble des sécrétions hormonales, chez l’humain, chez tous les mammifères et semble-t-il chez la plupart des espèces animales complexes. Cette neurohormone est synthétisée à partir d’un neurotransmetteur, la sérotonine, qui dérive elle-même du tryptophane, un acide aminé essentiel. Elle est sécrétée par la glande pinéale (dans le cerveau) en réponse à l’absence de lumière.
La mélatonine semble avoir de multiples fonctions, autres qu’hormonales chez l’humain et les mammifères, en particulier comme antioxydant. Elle semble aussi jouer un rôle dans le système immunitaire.
Diverses algues et plantes produisent aussi de la mélatonine, ou phytomélatonine[2],[3]. L’organisme peut d’ailleurs l’extraire de ces sources végétales (riz, bananes, ananas, etc.[4])[5].
Sommaire
Rôles multiples
Elle est considérée par les biochimistes et les chronobiologistes comme une hormone primordiale, car elle régule la sécrétion de la plupart des hormones humaines (paracrines et endocrines). La mélatonine agit différemment selon son origine :
- celle produite dans la glande pinéale et à partir du tractus gastro-intestinal agit comme une hormone endocrine car elle diffuse dans le sang ;
- celle produite par la rétine agit comme une hormone paracrine.
Glycémie, appétit, sommeil, etc. et mélatonine : Une étude internationale[6] a montré que la glycémie dépendait aussi de l’expression de quelques gènes dont celui codant un récepteur (MT2) de la mélatonine. Or ce récepteur MT2 est trouvé dans la rétine, dans le nerf optique, dans la région du diencéphale mais aussi dans les cellules du pancréas sécrétant l’insuline (chargée de contrôler la glycémie).
On pensait déjà que la mélatonine intervenait aussi dans l’appétit (et peut-être dans certains cas d’obésité), car injectée à des rats, elle augmente leur prise de nourriture et leur poids[7] et inversement une nourriture grasse perturbe le sommeil de souris de laboratoire via une hormone adiponectine, et une perturbation du rythme circadien les fait grossir. Par ailleurs, une mutation du gène codant pour le récepteur 2 (MT2) de la mélatonine est associée à une augmentation du risque d’obésité et au Diabète de type 2, mais aussi aux troubles du sommeil.
Horloge biologique
Julius Axelrod a, par de nombreuses expériences, découvert le rôle de la mélatonine et de la glande pinéale sur le cycle du sommeil et les autres rythmes circadiens. En temps normal, l’hormone du sommeil est sécrétée la nuit uniquement (pic de sécrétion à 5 heures du matin chez l’humain, et en moyenne, car sa production est inhibée par la lumière) et elle gère (en partie) les rythmes circadiens.
Psychisme
Dans les régions à hiver très gris comme l’Europe du Nord, c’est la baisse de luminosité hivernale (jours courts et gris) qui déclencherait une surproduction de mélatonine engendrant chez un grand nombre de personnes une asthénie, voire une dépression saisonnière, qui disparaissent au printemps.
Un nouvel antidépresseur (agomélatine[8]) cible les récepteurs à la mélatonine. Il est selon son fabricant très efficace sur les dépressions saisonnières qu’on estime induites par le manque de lumière en hiver, et ses effets métaboliques semblent positifs (au contraire de nombreux autres psychotropes connus).
Des séances de luminothérapie permettent généralement de réguler la production de mélatonine.
Antioxydant
La mélatonine est un puissant antioxydant[9],[10],
qui traverse facilement les parois cellulaires ou la barrière hémato-encéphalique. Elle détruit ou inhibe l’action de certains radicaux libres et éléments facteurs de stress oxydatif tels que le radical hydroxyle (.OH), le peroxyde d’hydrogène, le monoxyde d’azote, l’anion peroxynitrite, l’acide peroxynitreux, et de l’acide chlorhydrique. Les produits de chacune de ces réactions ont été identifiées dans les systèmes chimiques pur et dans un cas au moins in vivo. Les produits secondaires issus de l’interaction de la mélatonine avec l’ion OH (le 3-hydroxymelatonin cyclique) sont par exemple retrouvés dans l’urine des humains et des rats.[réf. nécessaire]
En outre, la mélatonine augmente l’activité de plusieurs enzymes antioxydantes, ce qui améliore sa capacité de protection des macromolécules contre le stress oxydatif. L’expérimentation animale a montré que la mélatonine acquise via des aliments végétaux comestibles élève le taux d’indole dans le sang. Le taux sanguin de mélatonine est corrélé avec l’activité antioxydante totale du sérum. Contrairement aux autres antioxydants (comme la vitamine C), la mélatonine est versatile ; c’est-à-dire qu’une fois oxydée, elle ne peut pas être directement réduite pour retrouver son état initial.[réf. nécessaire]
Une étude russe[11] indique que l’administration de mélatonine chez le rat produit un effet aussi anxiolytique qu’un médicament de référence, le diazépam (Valium), administré à la même dose (1 mg·kg-1).
Maladie d'Alzheimer
Une étude[12] publiée en 2008 montre que pour la maladie d’Alzheimer la prise de mélatonine (de même que l’exposition à la lumière naturelle), améliore les symptômes de troubles des cycles du sommeil, en agissant comme inducteur de sommeil mais aussi comme facteur d’allongement de la durée de celui-ci.
L’exposition à la lumière naturelle diminuerait aussi chez ces malades :- les symptômes de dépression (-19 %) ;
- les limitations fonctionnelles au quotidien (-53 %) ;
- la détérioration cognitive (-5 %).
La prise de mélatonine facilite l’endormissement (endormissement 8 minutes plus tôt en moyenne) et allonge le sommeil de 27 minutes en moyenne). L’association lumière + mélatonine a aussi diminué les comportements agressifs (-9 %), les phases d’agitation et de réveils nocturnes.
Le Dr Albert Lachman (spécialiste des troubles du sommeil) estime[13] qu’en améliorant le sommeil du malade on améliore aussi les fonctions cognitives et l’humeur. Il conseille « de bien éclairer les pièces en journée, de laisser les rideaux ouverts et, à l’inverse, de diminuer les sources de lumière en soirée pour que l’organisme reçoive le signal que la nuit est là ». « Malheureusement, dans certaines maisons de repos, pour des questions d’organisation, on fait plutôt l’inverse » ajoute-t-il[13].Système immunitaire
Associée au calcium, la mélatonine peut également aider à la réponse immunitaire des Lymphocytes T. Son utilisation médicale pour augmenter la réponse est cependant soumise à controverse puisqu’elle favoriserait également les maladies auto-immunes.
Libido ?
La mélatonine augmenterait la libido (chez les rats de sexe masculin) par un antagonisme des récepteurs de la sérotonine de type 5-HT(2A)[14].
Autres
La mélatonine joue un rôle dans la régulation du rythme éveil/sommeil, du rythme circadien, mais aussi dans la régulation de la pression artérielle, la protection des os.
Selon une étude italienne[15], le vin comporterait une quantité importante de mélatonine, ce qui expliquerait, peut-être et en partie, pourquoi certaines personnes auraient sommeil après l’absorption d’une quantité plus ou moins importante de vin.
Aliments riches en mélatonine
Selon une étude[16] des chercheurs du Health Science Center de l’Université du Texas, les noix et les noisettes sont une source importante de mélatonine facilement absorbée par l’organisme. Après avoir comparé le taux sanguin de rats nourris de noix à celui de rats nourris normalement, les chercheurs ont noté que la consommation de noix entraînait une multiplication par trois des taux sanguins de mélatonine. Ils pensent que les bienfaits des noix découlent de la synergie entre la mélatonine et les nutriments qu’elles contiennent.
La mélatonine se retrouve également dans le maïs, les tomates et les pommes de terre, mais en quantités nettement inférieures. La teneur en mélatonine de plusieurs aliments serait encore très mal connue, selon les auteurs de l’étude.
Les chercheurs sont incapables de dire quelle quantité de noix devrait être consommée quotidiennement afin de profiter de ses effets protecteurs. Mais ils affirment qu’en raison de la multitude de composés bénéfiques qu’elles contiennent, leur consommation est nettement préférable à la prise de suppléments de mélatonine. Selon ces chercheurs, il est donc préférable de prendre des noix, dont la capacité à normaliser les taux de mélatonine demeure inconnue, à des suppléments de mélatonine, dont les indications et les effets thérapeutiques sont connus. Il est important de préciser ici que ces chercheurs ont été payés par la Commission californienne des noix (California Walnut Commission).
Biosynthèse
La biosynthèse de mélatonine se décompose en deux temps, en effet, la mélatonine provient de la transformation du tryptophane, puis de la modification nocturne de sérotonine.
Synthèse diurne constitutive
La sérotonine est synthétisée de façon constitutive le jour et même la nuit pour certains individus. Elle provient de la transformation du tryptophane faisant intervenir deux enzymes. Tout d’abord, le tryptophane est transformé en 5-hydroxytryptophane par l’enzyme tryptophane hydroxylase (TH). Le 5-hydroxytryptophane subit ensuite une autre modification par l’enzyme aminoacide aromatique décarboxylase (AA-DC) pour donner la sérotonine. La sérotonine est stockée dans la glande pinéale (ou épiphyse) au fur et à mesure de sa synthèse. La TH est une enzyme mitochondriale. C’est l’enzyme limitante de la production de sérotonine.
Synthèse nocturne régulée
La nuit, la sérotonine est sécrétée et l’enzyme arylalkylamine-N-acétyltransférase (AA-NAT) catalyse sa dégradation en N-acétylsérotonine (ou N-acétyl-5 hydroxytryptamine). Ce composé est ensuite transformé en mélatonine (ou N-acétyl-5 méthoxytryptamine) grâce à l’enzyme hydroxyindole-O-méthyltransférase (HIOMT). L’AA-NAT est une enzyme photosensible et son activité est dépendante de la quantité de sérotonine. Elle est l’enzyme limitante de la production de mélatonine.
Régulation par l'AA-NAT
Chez les rongeurs, l’adrénaline nocturne, par augmentation d’AMPc, active la transcription de l’AA-NAT puis l’inhibe par accumulation graduelle d’ICER (Induced cAMP Element Response), maximum en fin de nuit.
Chez les ongulés et les primates, l’adrénaline nocturne, par augmentation d’AMPc, inhibe la protéolyse de l’AA-NAT synthétisée de façon constitutive.
Usage médical
Dosage et posologie
La sécrétion nocturne de mélatonine est impliquée dans le déclenchement du sommeil. Elle est donc utilisée depuis quelques années, dans certains pays, pour soigner les troubles du sommeil (insomnies des personnes âgées, ou le décalage horaire).
Aux États-Unis, au Canada et au Mexique, par exemple, la mélatonine est en vente libre. En France, sa vente est toujours régulée : cette molécule est inscrite sur la liste I des substances vénéneuses depuis le 7 avril 2009[17].
En Europe, la mélatonine a obtenue une AMM via la procédure centralisée pour la spécialité CIRCARDIN[18] dosé à 2 mg. En France, cette spécialité ne dispose que d’une ATU depuis 2005[19],[20].
Les doses suggérées sont cependant très élevées. Victor Herbert, M.D., J.D., de la Mt. Sinai School of Medicine, passe en revue plusieurs études du Massachusetts Institute of Technology qui montrent que les suppléments de mélatonine en vente libre contiennent de 3 à 10 fois plus de cette hormone qu’il n’est nécessaire pour augmenter la qualité du sommeil[21]. Ces hautes doses peuvent même être contre-productives : Lewy et collègues apportent un soutien expérimental à l’idée, déjà répandue, que des doses élevées de mélatonine peuvent exercer une action qui se propage à des phases qui ne sont pas des phases de réponse à la mélatonine (« too much melatonin may spill over onto the wrong zone of the melatonin phase-response curve »)[22]. Dans cette étude, 0,5 mg de mélatonine a été efficace, mais pas 20 mg (40 fois plus).
Sur un plan pratique, 0,3 mg (=300 µg c’est-à-dire microgrammes) représente une dose quotidienne suffisante pour recaler un rythme circadien déphasé ; cela implique que la mélatonine, pour ceux qui peuvent se la procurer, est beaucoup plus abordable qu’on aurait pu le penser. Contrairement à un médicament de type somnifère, la mélatonine ne provoque pas d’effets secondaires comme l’accoutumance.[réf. nécessaire]
Analogues pharmaceutiques de la mélatonine
Alors que la mélatonine n’est pas largement recommandée par les autorités médicales[23], Ramelteon ((S)-N-(2-(1,6,7,8-tetrahydro-2H-indeno-(5,4)furan-8-yl)ethyl)propionamide), vendue sous le nom de Rozerem (propriété de Takeda Pharmaceuticals), qui est conçue pour activer les récepteurs de la mélatonine MT1 et MT2, a été approuvée pour le traitement de l’insomnie aux États-Unis[24].
Usages en médecine vétérinaire
La plupart des animaux semblent produire de la mélatonine et/ou y être sensibles. La mélatonine est aussi un produit vétérinaire qui permet des gestations à toute période de l’année chez des mammifères d’élevage (chèvre…). Les poules exposées à la lumière pondent toute l’année, phénomène induit par l’éclairage forcé.
Rôles de la lumière et de l'obscurité
L’impact de l’éclairage artificiel sur l’humain est encore mal mesuré, mais les aveugles souffrent souvent de troubles du sommeil. La prise quotidienne de mélatonine une heure avant le coucher recalerait leur rythme circadien sur le cycle de vingt-quatre heures et donc améliorerait, voire préviendrait, les troubles du sommeil.
Sécurité
La mélatonine est a priori non toxique et les effets secondaires rapportés sont peu fréquents, excepté la somnolence, si prise à haute dose. La mélatonine exogène n’affecte normalement pas sa sécrétion endogène, à court ou moyen terme. Toutefois, la prise de mélatonine associée à un inhibiteur des monoamine oxydases (IMAO) peut provoquer un surdosage car les IMAO inhibent la métabolisation de la mélatonine par l’organisme.
Une étude du département de nutrition de l’université Andrews indique que certains comprimés de mélatonine contiendraient jusqu’à 10 fois la dose nécessaire pour provoquer l’effet physiologique sur le niveau de mélatonine dans le sang pour améliorer le repos nocturne. Selon cette étude, à ces fortes doses, la mélatonine pourrait provoquer des migraines et des sautes d’humeur et déstabiliser l’équilibre hormonal de l’organisme (voir Usage médical, supra).[réf. souhaitée]
Voir aussi
Articles connexes
Liens externes
Bibliographie
- (en) Brzezinski A. Melatonin in humans. The New England journal of medicine. 1997 Jan 16;336(3):186-95. http://www.ncbi.nlm.nih.gov/pubmed/8988899
- (en) Reiter RJ, Korkmaz A. Clinical aspects of melatonin. Saudi Med J. 2008 Nov;29(11):1537-47. http://www.ncbi.nlm.nih.gov/pubmed/18997997
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) REITER Russel J. ; DUN XIAN TAN ; BURKHARDT Susanne ; MANCHESTER Lucien C. ; Melatonin in plants, in Nutrition reviews ; 2001, Ed : International Life Sciences Institute ; vol. 59, no 9, p. 286-290 (47 ref.) ; ISSN:0029-6643 Fiche INIST CNRS.
- (en) Caniato R, Filippini R, Piovan A, Puricelli L, Borsarini A, Cappelletti E ; « Melatonin in plants ». (2003) ; Adv Exp Med Biol 527: 593–7. PMID 15206778.
- Tableau.
- (en) Paredes SD, Korkmaz A, Manchester LC, Tan DX, Reiter RJ, « Phytomelatonin : a review », dans J. Exp. Bot., vol. 60, no 1, 2009, p. 57–69 [texte intégral, lien PMID, lien DOI].
- Étude conduite par Philippe Froguel (laboratoire Génomique et physiologie moléculaire des maladies métaboliques ; CNRS/ Université Lille 2 Droit et Santé/ Institut Pasteur de Lille) et l’Imperial College London, en collaboration avec des équipes françaises, finlandaises et danoises, sur la base de l’analyse du génome de 23 000 personnes, publiée dans Nature Genetics en décembre 2008 (A variant near MTNR1B is associated with increased fasting plasma glucose levels and type 2 diabetes risks. N. Bouatia-Naji et al. ; Nature Genetics, XXX 2008). Les résultats de cette étude ont été confirmés par deux autres études internationales publiées au même moment (CNRS).
- Article « Les clés du sommeil », Pour la Science, Janvier 2004.
- Médicament développé par les laboratoires Servier et Novartis qui sera probablement vendu sous le nom de Valdoxan/Thymanax.
- (en)Korkmaz A, Reiter RJ, Topal T, Manchester LC, Oter S, Tan DX, « Melatonin : an established antioxidant worthy of use in clinical trials », dans Mol. Med., vol. 15, no 1-2, 2009, p. 43–50 [texte intégral, lien PMID, lien DOI]
- (en)Akcay YD, Yalcin A, Sozmen EY, « The effect of melatonin on lipid peroxidation and nitrite/nitrate levels, and on superoxide dismutase and catalase activities in kainic acid-induced injury », dans Cell. Mol. Biol. Lett., vol. 10, no 2, 2005, p. 321–9 [texte intégral, lien PMID].
- (en)Pineal melatonin exhibits more pronounced antistressor properties than anxiolytic diazepam. Eksp Klin Farmakol. 2007 Nov-Dec;70(6):9-12.
- (en) Riemersma-van der Lek et coll. ; Effect of bright light and melatonin on cognitive and non cognitive function of elderly residents of group care facilities. A randomized controlled trial. Revue JAMA 2008 ; 299 : 2642-2655.
- Cité dans un Article de Julie Luong intitulé Lumière et mélatonine contre la maladie d’Alzheimer (15 octobre 2008).
- (en) Brotto LA, Gorzalka BB. (2000) Melatonin enhances sexual behavior in the male rat. Physiol Behav. 2000 Feb;68(4):483-6. PMID: 10713287.
- Étude sur la mélatonine dans le vin.
- (en)Reiter RJ, Manchester LC, Tan DX. Melatonin in walnuts : Influence on levels of melatonin and total antioxidant capacity of blood. Nutrition. 2005 Sep;21(9):920-4.
- Journal officiel de la République française no 0082 du 7 avril 2009 page 6068, Arrêté du 26 mars 2009 portant classement sur les listes des substances vénéneuses, NOR:SASP0907274A.
- [1], Agence européenne des médicaments.
- [2], Agence française de sécurité sanitaire des produits de santé.
- [3], Agence française de sécurité sanitaire des produits de santé.
- (en) Zhdanova I, Wurtman R, Regan M, Taylor J, Shi J, Leclair O. (2001) Melatonin treatment for age-related insomnia. J Clin Endocrinol Metab 86, 10, p. 4727-30 PMID 11600532.
- (en) Lewy AJ, Emens JS, Sack RL, Hasler BP, Bernert RA. (2002) « Low, but not high, doses of melatonin entrained a free-running blind person with a long circadian period ». Chronobiol Int. 19, 3, p. 649-58, PMID 12069043.
- (en) Wolkove N, Elkholy O, Baltzan M, Palayew M, Sleep and aging : 2. Management of sleep disorders in older people CMAJ : Canadian Medical Association journal - Journal de l’Association médicale canadienne, volume 176, no 10, p. 1449-54 PMID 17485699.
- (en) McGechan A, Wellington K. Ramelteon. « Ramelteon » CNS Drugs 2005;19:1057-65.
Catégories :- Hormone épiphysaire
- Tryptamine
- Méthoxybenzène
- Amide
- Antioxydant
- Sommeil
- Rythme circadien
- Monoamine
Wikimedia Foundation. 2010.
