- Inox
-
Acier inoxydable

Cet article est lié aux
composés du fer et du carbonePhases - Austénite
- Bainite
- Carbure de fer
- Cémentite
- Ferrite
- Graphite
- Lédéburite
- Martensite
- Perlite
Acier - Acier Corten
- Acier duplex
- Acier électrique
- Acier inoxydable
- Acier maraging
- Acier rapide
- Désignation normalisée
Autre produits ferreux Les aciers inoxydables jouent un grand rôle dans d'innombrables domaines : vie quotidienne, industrie mécanique, agroalimentaire, chimie, transports, médecine, chirurgie, etc. Ce sont des aciers, alliages de fer et de carbone, auquel on ajoute essentiellement le chrome qui, au delà de 12 à 13 %, produit la résistance souhaitée à l'oxydation.
D'autres éléments peuvent être ajoutés, notamment le nickel qui améliore les propriétés mécaniques en général et la ductilité en particulier, et d'autres éléments comme le molybdène ou le titane qui améliore la stabilité de l'alliage pour des températures autres que l'ambiante ainsi que des éléments à hauts points de fusion comme le vanadium et le tungstène accompagné en général d'une augmentation de la teneur en chrome, pour obtenir la résistance aux hautes températures au contact d'une flamme (aciers réfractaires).
Rappels sur la corrosion
Les phénomènes de corrosion des métaux sont surtout de nature électrochimique. En présence d'une solution de type électrolyte, le potentiel métal-solution varie selon les points de la surface et de ce fait, des courants électriques apparaissent et provoquent l'endommagement du métal.
La résistance à la corrosion dépend de la valeur de ces potentiels et surtout de leur répartition sur les surfaces. Toutes les hétérogénéités donnent naissance à des couples électriques, à commencer par celles qui résultent des différences de structure et de composition des microcristaux qui constituent le matériau lui-même. D'autres hétérogénéités sont dues à la présence de soudures, de rivets, de façonnages locaux entraînant un écrouissage (dans les tôles pliées par exemple), mais aussi au frottement contre des pièces antagonistes ou même à de simples rayures.
À chaud, la diffusion des agents corrosifs dans l'épaisseur du métal peut compliquer encore le problème.
La lutte contre la corrosion est une préoccupation constante dans beaucoup de domaines industriels. Une solution relativement simple consiste à recouvrir la surface à protéger par un matériau insensible au milieu agressif, matériau qui peut être métallique ou non. Les peintures, les vernis, certains traitements de surface, les revêtements métalliques de plomb, de zinc, de nickel, de chrome, etc. peuvent être souvent utilisés avec succès. Il est possible également de remplacer les métaux par d'autres matériaux de plus grande inertie chimique comme le graphite, la céramique, le verre, les matières plastiques, etc.
Généralités sur les aciers inoxydables
Composition des aciers inoxydables
Pour être classé dans la catégorie inoxydable, un acier doit contenir au moins 11 % de chrome.
Les plus courants :
- X2CrNi18-10 (304L) : C : 0,02 %, Cr : 17 à 19 %, Ni : 9 à 11 %, utilisés pour la réalisation d'ouvrages toutes qualités ;
- X2CrNiMo17-12 (316L) : C : 0,02 %, Cr : 16-18 %, Ni : 11-13 %, Mo (molybdène) : 2 %, utilisés dans les industries chimiques, pharmaceutique, pétrolières, agro-alimentaires et aussi intensément en milieu nautique ;
- X8Cr17 (430) : C : 0,08 %, Cr : 16-18 %, utilisés pour les articles de ménage, l'électroménager, les éviers ;
- X6CrTi12 (409) : C : 0,06 %, Cr : 11-13 %, Ti (titane), utilisé dans les échappements automobiles, fourneaux etc.
(analyse chimique en % pondéral) La plupart des aciers inoxydables utilisés sont conformes à des normes :
- européennes (norme EN 10088 en particulier) ;
- américaines (normes de l'AISI) ; L signifie low carbon (bas carbone), H signifie High carbon (haut carbone).
Les normes d'autres pays existent également mais sont peu connues internationalement.
- Concernant le tableau d'équivalence ci dessous il faut remarquer que la nuance américaine de type 316 autorise une teneur en molybdène de 3% maximum ce qui peut poser un problème de conformité lorsque la spécification préconise une norme européenne qui limite la teneur en molybdène à 2,5 %.
Équivalences des désignations Afnor
NF A 35573 (France)EN 10027
(européenne)AISI (États-Unis) Composition % C % Mn % P % S % Si % Ni % Cr % Mo Autres Z10CN18-09 X12CrNi18-09 302 0,12 2 0,04 0,03 1 6 à 8 16 à 18 — — Z10CNF18-09 X12CrNi18-08 303 ≤ 0,12 2 0,06 ≥ 0,15 1 8 à 10 17 à 19 0,6 — Z6CN18-09 X5CrNi18-09
1.4301304 0,07 2 0,04 0,03 1 8 à 10 17 à 19 — — Z2CN18-10 X2CrNi18-09
1.4307304 L 0,03 2 0,04 0,03 1 9 à 11 17 à 19 — — Z8CN18-12 X5CrNi19-11
1.4303305 0,1 2 0,04 0,03 1 11 à 13 17 à 19 — — Z12CNS25-13 X7CrNi23-14 309 0,2 2 0,04 0,03 1 11 à 14 22 à 25 — — Z12CNS25-20 X12CrNiSi25-20 310 0,15 2 0,04 0,03 1 18 à 21 23 à 26 — — Z6CND17-11 X5CrNiMo18-10
1.4401316 0,07 2 0,04 0,03 1 10 à 12,5 16 à 18 2 à 2,5 — Z2CND17-12 X2CrNiMo18-10
1.4404316 L 0,03 2 0,04 0,03 1 10,5 à 13 16 à 18 2 à 2,5 — Z6CNDT17-12 X10CrNiMoTi18-10
1.4571316 Ti 0,1 2 0,04 0,03 1 10,5 à 13 16 à 18 2 à 2,5 Ti . 5 C ; Ti . 0,6 Z6CNT18-10 X10CrNiTi18-09
1.4541321 0,12 2 0,04 0,03 1 10 à 12 17 à 19 — Ti . 5 C ; Ti . 0,6 Z6C13 X7Cr13
1.4003403 0,08 1 0,04 0,03 1 — 11,5/13,5 — — Z12C13 X10Cr13
1.4006410 0,08/0,15 1 0,04 0,03 1 — 11,5/13,5 — — Z12CF13 X12CrS13 416 0,08/0,15 1,5 0,06 ≥ 0,15 1 0,5 12 à 14 0,15/0,6 — Z20C13 X20Cr13
1.4021420 0,16-0,25 ≤ 1,5 ≤ 0,04 ≤ 0,015 ≤ 1 — 12 — — Z30C13 X30Cr13 420 B 0,3 1 0,04 0,03 1 — 12 à 14 — — Z15CN16-02 X22CrNi17
1.4057431 0,1/0,2 1 0,04 0,03 1 1,5/3 15/17 — — Z100CD17 X105CrMo17 440 C 1 1 — — — — 17 — — Z8C17 X6Cr17
1.4016430 0,08 1 0,04 0,03 1 0,5 16/18 — — Z10CF17 X12CrMoS17 430 F 0,12 1,5 0,06 ≥ 0,15 1 0,5 16/18 0,2/0,6 — Produits en aciers inoxydables
Les principales formes de produits sont :
- les tôles à chaud et à froid ;
- les tubes ronds, carrés (deco), rectangulaires (deco) ;
- les fils ;
- les demi-produits destinés soit à être forgés, soit relaminés ;
- les fibres ;
- accessoires, robinetterie, raccords.
Généralités
En plus de la résistance à la corrosion qui caractérise les matériaux énumérés plus haut, les aciers inoxydables possèdent une qualité déterminante qui est la résistance mécanique.
L'élément d'alliage auquel les aciers inoxydables doivent leur principale caractéristique est le chrome. Contrairement à ce que l'on croit généralement, ce métal est très réactif du point de vue chimique et il est en particulier très oxydable, mais son oxyde forme une véritable peau à la fois transparente et protectrice. Allié au fer et au nickel, il provoque la formation d'un composé de surface oxydé capable de ralentir ou même d'arrêter totalement la corrosion.
Le chrome et le nickel s'oxydent ainsi :
- 4 Cr + 3 O2 → 2 Cr2O3
- 2 Ni + O2 → 2 NiO
Ainsi, le fer ne réagit pas avec le dioxygène, c'est donc le fer qui est rendu inoxydable et non l'acier véritablement.
Il existe de très nombreuses nuances d'aciers inoxydables et le choix est parfois difficile, car ils n'ont pas tous le même comportement dans un milieu donné. On les désigne souvent par les pourcentages massiques en nickel et en chrome. Ainsi, un inox 18/10, tel que ceux utilisés en coutellerie, pour les couverts et pour la cuisine en général, contient 18 % en masse de chrome et 10 % en masse de nickel. Cette désignation est en fait très insuffisante car elle ne préjuge en rien de la structure métallurgique.
La teneur en chrome est dans tous les cas d'au moins 12 %. D'autres éléments d'alliage, pour l'essentiel des métaux relativement « nobles » comme le nickel, le molybdène, le cuivre, améliorent encore la résistance chimique, en particulier dans les milieux non oxydants.
Les propriétés de résistance de ces alliages ont été découvertes en 1913 lorsque l'on s'aperçut que des échantillons polis en vue d'examens de laboratoire ne subissaient pas d'oxydation. On peut dire que :
- les aciers inoxydables ne peuvent être corrodés à froid qu'en présence d'humidité. C'est ainsi qu'ils résistent au chlore, gaz pourtant très corrosif, pourvu que ce dernier soit parfaitement sec ;
- l'action des solutions aqueuses est telle que la corrosion électrochimique prend le pas sur la corrosion chimique directe ; la bonne tenue du matériau dépend, comme cela a été écrit plus haut, des potentiels électrochimiques en surface et de leur répartition ;
- comme l'aluminium, métal extrêmement oxydable qui se recouvre d'un oxyde protecteur, les aciers inoxydables se comportent de manière active lorsqu'ils viennent d'être usinés, décapés ou polis et de manière passive lorsque les attaques extérieures ont permis de former la « peau » qui les protège ;
- une bonne utilisation des aciers inoxydables nécessite donc un métal d'une très grande homogénéité pour éviter des corrosions locales et un passage de l'état actif à l'état passif en tous les points de la surface exposée.
Par rapport à une électrode à hydrogène de référence, le potentiel des aciers inoxydables se situe entre le molybdène et le mercure, non loin de l'argent et du platine.
Le dépôt de particules ferreuses sur les surfaces d'acier inoxydable est très dangereux en milieu humide, car la rouille sert de catalyseur et la surface finit par se « piquer ».
Histoire - Découverte
Les premiers alliages de fer résistant à la corrosion furent coulés dès l'antiquité : le pilier de fer de Delhi, érigé sous ordre de Kumarâgupta Ier au Ve siècle subsiste encore de nos jours en parfait état. Cependant une distinction doit être faite dans le vocabulaire : ces alliages devaient leur résistance à leur haute teneur en phosphore, et non en chrome. Il ne s'agissait donc pas d'aciers inoxydables dans le sens que l'on donne actuellement au terme. Dans ces alliages et sous des conditions climatiques favorables, il se forme en surface une couche de passivation d'oxyde de fer et de phosphates qui protège le reste du métal bien mieux qu'une couche de rouille.
Les premiers aciers résistants à base de chrome furent développés par le métallurgiste français Pierre Berthier, qui remarqua leur résistance à certains acides et imagina leur application en coutellerie. Cependant, à l'époque, on n'utilisait pas les bas taux en carbone et haut taux en chrome couramment utilisés dans les aciers inoxydables modernes, et les alliages obtenus alors, trop riches en carbone, étaient trop fragiles pour avoir un véritable intérêt.
En 1878, les établissements Jacob Holtzer[1] situés à Unieux (Loire) commencent la production industrielle d'aciers chromés.
Dans les années 1890, l'Allemand Hans Goldschmidt développa et breveta un procédé appelé la thermite qui permettait d'obtenir du fer sans carbone. Entre 1904 et 1911, divers chercheurs, notamment le Français Léon Guillet, mirent au point différents alliages que l'on pourrait aujourd'hui considérer comme inoxydables. En 1911, l'Allemand Philip Monnartz mettait en évidence l'influence du taux en chrome des alliages et leur résistance à la corrosion.
Enfin, en 1913, l'Anglais Harry Brearley des laboratoires Brown-Firth, en travaillant sur l'érosion dans les canons d'armes à feu, développa, dans la ville de Sheffield en Angleterre, un acier qu'il baptisa rustless (« sans-rouille ») et qui sera ensuite rebaptisé stainless (« sans-tâche », ou « pur ») qui sera officiellement le premier acier à porter le nom d'« inoxydable » ; Brearley entra dans l'histoire comme leur inventeur. Il s'agissait alors d'un acier inoxydable martensitique (0,24 % en carbone et 12,8 % en chrome). Cependant d'autres aciers comparables avaient été développés en Allemagne par Eduard Maurer et Benno Strauss qui élaboraient un acier inoxydable austénitique (21 % de chrome et 7 % de nickel) pour Krupp Ag. Aux États-Unis, Christian Dantsizen et Frederick Becket lancèrent déjà la fabrication industrielle d'acier inoxydable ferritique. En 1908, Krupp avait déjà construit des navires à coque en acier inoxydable chrome-nickel.
En 1924, W. H. Hatfield, qui succéda à Harry Brearley à la tête des laboratoires Brown-Firth, élabora l'acier « 18/8 » (18 % en masse de chrome et 8 % en nickel) qui est probablement le représentant le plus utilisé des aciers inoxydables fer-chrome.
Types de corrosion des aciers inoxydables
Comme tous les métaux, ces aciers peuvent subir une corrosion chimique uniforme qui attaque les surfaces de manière régulière ; on peut alors mesurer la masse perdue par unité de surface et par unité de temps.
D'autres formes de corrosion caractérisent les aciers inoxydables austénitiques et peuvent se révéler très gênantes à l'usage :
- la corrosion intergranulaire, en cheminant entre les microcristaux du métal, finit par désagréger le métal. Elle est liée à la précipitation de carbure de chrome le long des joints. Pour qu'elle se produise, trois conditions doivent être remplies : au moins 0,035 % de carbone, une sensibilisation par un maintien à une température de 400 à 800 °C, un milieu extérieur acide avec un pouvoir oxydant compris entre deux limites bien définies ;
- la corrosion par piqûres n'est généralement pas due à une hétérogénéité du matériau mais à la présence accidentelle d'une poussière métallique qui, en milieu humide, forme une pile électrique. La surface de l'acier constitue alors la cathode et se corrode. On peut ainsi voir des tôles de 2 mm d'épaisseur se percer en quelques heures. Un milieu à la fois très acide et très oxydant peut produire des effets similaires ;
- la corrosion sous contrainte provoque la mise hors service très rapide des objets qu'elle attaque. Elle est heureusement très rare. Pour qu'elle se produise, il faut que les pièces comportent des parties mises en tension, même faiblement, sous l'effet des contraintes de service ou des effets secondaires des soudures, de l'emboutissage... et qu'elles soient en outre exposées à un milieu corrosif de type eau impure, solutions de chlorures même très diluées, soude caustique chaude.
Structure métallurgique et rôle des éléments d'addition
Les éléments d’addition
Le chrome
Les aciers inoxydables sont des alliages fer-chrome ou plus exactement acier-chrome c'est-à-dire fer-carbone-chrome. Conformément à la norme européenne EN 10088-1[2], un acier est classé acier inoxydable s’il contient au minimum 12 % en masse de chrome et moins de 2 % de carbone.
C’est le chrome qui donne aux aciers inoxydables leur résistance à la corrosion.
Le carbone
La teneur en carbone est limitée à un maximum de 1,2 % en masse afin d’éviter la formation de carbures[3] (notamment de carbures de chrome, qui est un composé très stable mais qui n'empêche pas l'oxydation du fer) qui sont préjudiciables au matériau. Par exemple, le carbure M23C6 qui peut apparaître dans l'austénite 18-9 a un effet négatif vis-à-vis de la corrosion intergranulaire[4].
Autres éléments
Le nickel favorise la formation de structures homogènes de type austénitique, intéressantes pour éviter la corrosion mais à éviter soigneusement dans le domaine du frottement.
Le manganèse est un substitut du nickel. Certaines séries d’alliages austénitique ont été développées permettant de faire face aux incertitudes d’approvisionnement du nickel[5].
Le molybdène et le cuivre améliorent la tenue dans la plupart des milieux corrosifs, en particulier ceux qui sont acides, mais aussi dans les solutions phosphoriques, soufrées, etc. Le molybdène accroît la stabilité des films de passivation.
Le tungstène améliore la tenue aux températures élevées des aciers inoxydables austénitiques.
Le titane doit être utilisé à une teneur qui dépasse le quadruple de la teneur en carbone. Il évite l'altération des structures métallurgiques lors du travail à chaud, en particulier lors des travaux de soudure où il prend la place du chrome pour former un carbure de titane (TiC) évitant de ce fait la perte du caractère d'inoxydabilité dans les zones affectées par la chaleur (ZAC) du fait de la captation du chrome, conséquence directe de la formation de carbure de chrome Cr23C6.
Le niobium a un point de fusion beaucoup plus élevé que le titane et présente des propriétés semblables. Il est utilisé dans les métaux d'apport pour soudage à l'arc électrique en lieu et place du titane qui serait volatilisé pendant le transfert dans l'arc électrique.
Le silicium joue également un rôle dans la résistance à l’oxydation, notamment vis-à-vis des acides fortement oxydants (acide nitrique concentré ou acide sulfurique concentré chaud[6].Système fer-chrome
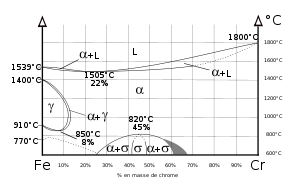
Le fer pur possède trois formes allotropiques en fonction de la température :
- jusqu’à 910 °C (point A3) : forme alpha (α), ferrite (cubique centré) ;
- de 910 à 1 400 °C (point A4) : forme gamma (γ), austénite (cubique à faces centrées) ;
- de 1 400 à 1 538 °C (température de fusion) : forme delta (δ), ferrite (cubique centré).
Le chrome est un élément dit alphagène. Il favorise fortement la forme ferritique. Sur le diagramme de phase Fe-Cr, le domaine austénitique est assez réduit et est représenté par un domaine limité appelé boucle gamma.
Pour des teneurs supérieures à 11,5 % de chrome, l’alliage reste ferritique dans toute la plage de température. Il y a disparition de la transformation allotropique α-γ. Entre 10,5 et 11,5 % de chrome, l’alliage est biphasé ferrite + austénite dans certaines plages de température. Il subit une transformation ferrite/austénite pour des teneurs inférieures à 10,5 %.
On notera que le chrome jusqu’à 8 % abaisse la température A3 et se comporte comme un élément gammagène. Ce comportement s’inverse pour des teneurs supérieures à 8 %, point à partir duquel cette température augmente[7].
Pour certaines teneurs de chrome, dans le cadre d’un refroidissement lent, il peut y avoir formation de phase intermétallique sigma (σ) à des températures inférieures à 820 °C. Elle précipite au joint de grain ou dans la matrice ferritique entraînant une fragilité[8].
Système fer-chrome-nickel
Le nickel est à l’opposé du chrome un élément dit gammagène. Il ouvre le domaine austénitique.
Concrètement, l’addition de nickel augmente la taille de la boucle gamma.
Éléments α-gènes γ-gènes
D’autres éléments ont un rôle alphagène ou gammagène. Un rôle particulier est tenu par le carbone et l’azote.
Le carbone à un rôle gammagène et rentre donc en « compétition » avec le chrome[4]. En fait plus que le carbone seul, c’est le couple carbone-azote dont il faut tenir compte. Ces deux éléments étant des éléments d’alliage d'insertion contrairement aux autres éléments qui sont des éléments de substitution[9].
Les éléments alphagènes sont le chrome, le molybdène, le silicium, le titane, le niobium, le vanadium, le tungstène, l'aluminium et le tantale[10].
Les éléments gammagènes sont le nickel, le carbone, l'azote, le cobalt et le manganèse. Le manganèse peut avoir un rôle plus complexe[10].
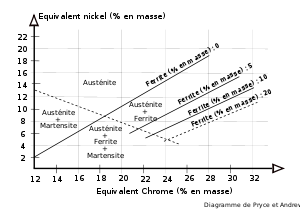
Plusieurs modèles approximatifs ont été mis au point pour prévoir le comportement de l’alliage en fonction de la composition globale de l’alliage. Les teneurs sont affectées de coefficients établis par expérience afin de tenir compte du poids de chacun des éléments.
Pour les produits laminés, il existe le modèle de Pryce et Andrew donnant les équations suivantes :
On remarquera le poids important du carbone et de l’azote.
Il existe également le modèle de Schaeffler et le modèle de Delong pour les aciers inoxydables à l’état brut de soudage[11].
- Modèle de Schaeffler :
- Modèle de Delong :
Contrairement au modèle de Schaeffler, le modèle de Delong prend en compte l’azote.
Types d'aciers inoxydables
Les aciers au chrome sont ferritiques et magnétiques à l'état adouci. Certains se comportent comme des aciers spéciaux auto-trempants, d'autres ne se trempent que partiellement ou pas du tout. Les aciers au nickel-chrome sont en général austénitiques et le traitement d'hypertrempe, loin de les durcir, a au contraire la propriété de les adoucir. Il existe d'innombrables nuances appropriées aux usages les plus divers.
On distingue les quatre familles d'aciers inoxydables suivantes :
- Les aciers martensitiques
Ils sont utilisés lorsque les caractéristiques de résistance mécanique sont importantes. Les plus courants titrent 13 % de chrome avec au moins 0,08 % de carbone. D'autres nuances sont plus chargées en additions, avec éventuellement un faible pourcentage de nickel.
Exemples : X20Cr13, X46Cr13, X29CrS13.
- Les aciers ferritiques
Ils ne prennent pas la trempe. On trouve dans cette catégorie des aciers réfractaires à haute teneur en chrome (jusqu'à 27 %), particulièrement intéressants en présence de soufre. Les aciers ferritiques sont parfois utilisés comme barrière de résistance à la corrosion (tôles plaquées, tôle claddées) des parois d'équipements sous pression en acier utilisés par dans les industries pétrochimique et chimique. Ces aciers sont souvent utilisés en lieu et place des aciers austéniques pour la réalisation d'ustensiles de cuisine bon marché et de qualité médiocre (plats et couteaux par exemple).
Exemples : X6Cr17, X6CrMo17-1, X3CrTi17.
- Les aciers austénitiques
Ce sont de loin les plus nombreux, en raison de leur résistance chimique très élevée, de leur ductilité comparable à celle du cuivre ou du laiton, et aussi de leurs bonnes caractéristiques mécaniques élevées. Les teneurs en éléments d'addition tournent autour de 18 % de chrome et 10 % de nickel. La teneur en carbone est très basse et la stabilité améliorée par des éléments tels que le titane ou le niobium. Ces aciers sont aussi utilisés en compétition avec les alliages légers et l'acier à 9 % de nickel pour la réalisation d'équipements destinés à la cryogénie.
Exemples : X2CrNi18-9, X2CrNiMo17-12-2.
- Les aciers improprement dénommés « austéno-ferritiques »
Ils ont des propriétés de résistance à la corrosion intergranulaire ainsi qu'en eau de mer remarquables et présentent, pendant l'essai de traction, un palier élasto-plastique. Ils ont un comportement mécanique semblable aux aciers de construction. La transformation liquide / solide se traduit par une solidification en phase ferritique (ferrite delta) puis d'une seconde transformation, à l'état solide, en austénite. Ils devraient donc, en conséquence, être dénommés aciers ferrito-austénitiques. Le simple fait de désigner correctement ces aciers permet de tout de suite comprendre qu'un refroidissement lent, pendant le soudage, permettra à un maximum de phase ferritique de se transformer en phase austénique et réciproquement, un refroidissement rapide aboutira à un gel de la ferrite laissant peu de possibilités à la transformation austénitique.
Exemple : X2CrNiN23-4.
La connaissance des types d'acier est essentielle pour les systèmes constitués d'éléments assemblés mécaniquement ou par soudage, la mise en présence de deux aciers inoxydables trop différents dans un électrolyte peut en effet provoquer des phénomènes de corrosion électrochimique très destructeurs.
- Caractéristiques mécaniques
- Voir : b:Matériaux/Caractéristiques mécaniques des aciers#Aciers inoxydables
Conditions à réunir pour favoriser la résistance à la corrosion
Les facteurs favorables à la lutte contre la corrosion sont également applicables aux aciers inoxydables :
- les surfaces doivent être décapées pour éliminer tous les oxydes résultant du travail à chaud : laminage, forgeage, traitements thermiques, assemblages par soudure, etc. ;
- ne traiter thermiquement que des pièces propres et sèches, sans traces de graisses, de résidus de produits dégraissants, et surtout sans particules ferreuses. Le nettoyage à l'acide nitrique avant traitement est généralement une excellente solution, ;
- supprimer les tensions résiduelles résultant d'un écrouissage à froid, en particulier celles qui résultent de l'emboutissage ;
- éviter, lors de la conception des pièces, de créer des zones difficiles à nettoyer ;
- éviter tous les contacts non indispensables entre les pièces d'acier inoxydables et les autres matériaux, métalliques ou non ;
- utiliser des outils (brosse, piquettes, marteaux, disques de meule, etc.) n'ayant servi que sur ce type d'acier ;
- protéger des projections et des poussières métalliques provenant de la mise en œuvre, à proximité, d'aciers non inoxydables. Favoriser le travail en atelier blanc ;
- Plus encore pour les aciers inoxydables que pour les autres métaux, l'état de surface doit être particulièrement soigné car il conditionne l'établissement d'un film passivant.
Influence de divers milieux
- Eaux industrielles : l'eau pure est sans effet mais les chlorures (et dans une moindre mesure beaucoup d'autres sels), même à l'état de traces, sont particulièrement néfastes pour les aciers inoxydables ; les nuances contenant du molybdène sont alors les plus indiquées.
- Vapeur d'eau : normalement sans effet, elle peut toutefois poser des problèmes si elle contient certaines impuretés.
- Atmosphères naturelles, à l'exception des atmosphères marines : elles posent d'autant moins de problèmes que l'acier contient davantage d'éléments nobles et que la surface est mieux polie.
- Atmosphères marines et industrielles : les aciers au chrome s'altèrent très lentement mais on préfère en général utiliser des aciers au molybdène.
- Acide nitrique : il attaque la plupart des métaux industriels mais l'acier inoxydable en général lui résiste particulièrement bien, par suite de la passivation de sa surface : le molybdène n'est intéressant que si l'acide contient des impuretés.
- Acide sulfurique : la résistance dépend beaucoup de la concentration et la présence d'impuretés oxydantes améliore la passivation. D'une manière générale les nuances austénitiques contenant du molybdène sont les meilleures.
- Acide phosphorique : la résistance est généralement bonne mais il faut surveiller les impuretés, en particulier l'acide fluorhydrique.
- Sulfites acides : la corrosion peut être catastrophique car ces solutions, que l'on rencontre souvent dans les papeteries, comportent beaucoup d'impuretés ; là encore les alliages au molybdène sont préférables.
- Acide chlorhydrique : la corrosion augmente régulièrement au fur et à mesure que la concentration augmente, l'association est donc à éviter.
- Acides organiques : ils ne sont généralement pas aussi corrosifs que les acides minéraux et ceux que l'on rencontre dans l'industrie alimentaire (acides acétique, oxalique, citrique, etc.) sont pratiquement sans effet.
- Solutions alcalines : les solutions froides n'ont pratiquement pas d'action mais il n'en est pas de même pour les solutions concentrées et chaudes.
- Solutions salines : le comportement est généralement assez bon, sauf en présence de certains sels comme les chlorures ; les nitrates au contraire favorisent la passivation et améliorent la tenue. l'acide nitrique en mélange avec des saumures saturées peut provoquer des destructions de l'acier inox (même des nuances en 316L).
- Produits alimentaires : il n'y a généralement aucun problème de corrosion sauf avec certains produits qui contient des composants sulfureux naturels ou ajoutés, comme la moutarde et les vins blancs.
- Produits organiques : ils sont généralement sans action sur les aciers inoxydables, saufs s'ils sont chlorés et à chaud (la javel à plus de 60 °C et à des concentrations élevées peut détruire (piqures noires) l'acier inox. Les colles, savons, goudrons, produits pétroliers, etc. ne posent aucun problème.
- Sels et autres produits minéraux fondus : les produits alcalins corrodent tous les aciers inoxydables mais les nitrates, cyanures, acétates, etc. n'attaquent pas les aciers inoxydables. La plupart des autres sels et des métaux fondus produisent des dégâts rapides.
Mise en œuvre des aciers inoxydables
Problèmes particuliers du travail à chaud
Par rapport à d'autres matériaux métalliques, les aciers inoxydables possèdent certaines propriétés particulières dont il faut tenir compte lors de la mise en forme :
- ils réagissent énormément aux températures assez hautes ;
- ils sont très mauvais conducteurs de la chaleur ;
- leur résistance mécanique est élevée, surtout dans le cas des austénitiques (à froid ce sont au contraire les martensitiques les plus résistants) ;
- le grain tend à grossir à chaud et ne peut être régénéré que par corroyage ;
- le travail doit être suivi d'un recuit et d'un décapage permettant de profiter de la résistance à la corrosion.
Les pièces massives doivent donc être chauffées lentement jusqu'à environ 800 °C avant d'être portées plus rapidement à la température de travail, qui se situe aux alentours de 1 000 °C. Il faut éviter avant tout la décarburation des aciers martensitiques, le maintien prolongé à haute température des aciers ferritiques et des aciers austénitiques, dont le grain grossit facilement et se révèle difficile ou parfois même impossible à régénérer. Le refroidissement rapide à l'eau, après travail, est souvent préconisé.
Traitements thermiques
C'est le plus souvent sous forme de tôles ou de tubes que l'on utilise les aciers inoxydables, et dans ce cas on est souvent obligé de pratiquer un recuit d'adoucissement après des opérations telles que l'emboutissage, pour éviter le maintien de contraintes résiduelles trop élevées.
Le dégraissage avant traitement doit être particulièrement soigné, les atmosphères oxydantes sont les plus indiquées et les atmosphères carburantes doivent être proscrites.
Les aciers martensitiques trouvent leur principale utilisation en construction mécanique, sous forme de pièces massives. Pour obtenir la résistance voulue, ils sont généralement trempés puis revenus. L'adoucissement s'impose généralement après l'écrouissage résultant du travail à froid. Le revenu abaissant la résistance à la corrosion, il vaut mieux utiliser une nuance moins riche en carbone qui diminue l'intensité de la trempe et permet d'éviter un revenu à trop haute température.
Les aciers ferritiques ne prennent pas la trempe mais il faut souvent les recuire, par exemple entre deux passes d'emboutissage et, dans des cas bien particuliers et après avis du producteur de l'acier, après soudure. Un trop long maintien à température élevée engendre une certaine fragilité par suite du grossissement du grain.
Les aciers austénitiques et austéno-ferritiques sont adoucis par un traitement à haute température, de 900 °C jusqu'à 1 150 °C, suivi d'un refroidissement aussi rapide que possible. La résistance à la corrosion, particulièrement à sa forme intergranulaire, nécessite de pratiquer autant que possible un traitement d'hypertrempe.
La détente des tensions internes peut se faire à température relativement basse, environ 400 °C ou 450 °C.
Les aciers inoxydables à durcissement structural nécessitent des traitements particuliers selon les nuances.
Formage à froid
Toutes les techniques habituelles du travail à froid sont applicables aux aciers inoxydables et donc aux pièces obtenues à partir de tôles ou de fils que l'on peut trouver dans d'innombrables objets d'usage courant.
Les aciers inoxydables sont relativement durs et cette dureté s'élève par écrouissage, au fur et à mesure qu'on les déforme. Ce phénomène est particulièrement marqué pour les aciers austénitiques. Les aciers ferritiques s'écrouissent moins mais l'allongement qu'on peut leur imposer est plus faible.
Le « retour élastique » après formage est beaucoup plus grand que pour les aciers doux « ordinaires ».
La lubrification entre les pièces en cours de formage et les outils est essentielle mais ne pose pas de problèmes particuliers pour la plupart des opérations. Toutefois, pour les pièces à caractère décoratif il faut faire attention à la formation de défauts superficiels par suite d'un grippage intempestif. L'emploi d'outils en acier trempé, en fonte méhanite ou encore en cupro-aluminium, ainsi que les protections par des vernis pelables ou des feuilles plastiques constituent souvent une bonne solution.
L'écrouissage diminue la résistance à la corrosion et crée parfois un magnétisme résiduel. Un recuit permet de restaurer les structures.
Le pliage à la presse ou à la molette ne présente pas de difficulté particulière.
L'emboutissage nécessite des machines deux fois plus puissantes que celles qui servent pour l'acier doux. La pression exercée par les serre-flans doit être suffisante pour éviter les plissements mais pas trop pour éviter les déchirures. Les fontes alliées au nickel-chrome donnent les meilleurs outillages, les feuilles minces peuvent être conformées dans des matrices en alliage cuivre-zinc. Les congés doivent avoir un rayon ni trop petit, ni trop grand, pour éviter à la fois un écrouissage excessif et les plissements, on prend en général entre 5 et 10 fois l'épaisseur des flans. La lubrification s'effectue avec tous les lubrifiants classiques, solutions savonneuses, huiles solubles ou non, avec dans les cas difficiles des ajouts de lubrifiants solides ou de matières chimiquement actives : plomb, talc, graphite, bisulfure de molybdène, huiles sulfurées ou sulfochlorées, additifs phosphorés, etc. Les recuits se font de préférence en atmosphère oxydante et autant que possible aussitôt après l'emboutissage.
Le repoussage ne pose pas de problème particulier, les précautions à prendre sont les mêmes que pour l'emboutissage, les meilleurs outils sont en acier cémenté.
Assemblage des aciers inoxydables
Soudage et brasage
Les procédés de soudage existants restent valables dans l'ensemble ; on recherche naturellement des soudures saines, sans porosités, dotées d'une bonne résistance mécanique, mais ici il faut en outre qu'elles conservent les qualités de résistance à la corrosion qui sont celles des matériaux de base.
Il faut avant tout limiter dans toute la mesure du possible l'appauvrissement en chrome (par exemple par formation de carbures du genre Cr23C6 aux dépens de la matrice environnante qui perd 95 % de sa teneur en Cr), en raison du rôle essentiel de cet élément qui se manifeste de par la très grande résistance à la corrosion de sa couche d'oxyde. Il est opportun de nettoyer convenablement les abords des soudures y compris les bords à souder afin d'éviter la formation de ces carbures : enlever toutes traces de graisse, de dépôts de carbone (traçage au crayon mine), proscrire les flammes et atmosphères carburantes y compris avant les traitements thermiques. La propriété de la couche d'oxyde ne doit pas faire oublier que le chrome est oxydable et donc de la nécessité de protéger le bain de fusion de l'action de l'oxygène par une atmosphère inerte qui peut être selon le cas, de l'argon ou de l'hélium ou de l'azote voire le vide, dans des procédés de soudage sans laitier comme le TIG, le MIG, le A-TIG, le plasma, le laser, le faisceau d'électron...
- Les aciers martensitiques, en raison de leur haute teneur en carbone, se prêtent mal au soudage homogène (problème de rupture fragile en 1ère passe)et de fissuration à froid par conjugaison des trois facteurs : présence de structures fragiles, effet de l'hydrogène et apparition de contraintes), à chaque fois que possible préconiser le soudage hétérogène avec produit d'apport austénitique.
- Les aciers ferritiques tendent à devenir fragiles lorsqu'ils sont soudés en homogène et devraient être immédiatement suivi d'un traitement d'hyper-trempe (remise en solution des carbures et des composés intermétalliques), ce qui n'est pas toujours réalisable. Lorsque rien ne s'y oppose (problème de corrosion galvanique par exemple) ou qu'il n'y a pas de contre-indication avec la destinée de l'équipement fabriqué, il est préconisé de souder en hétérogène avec un produit d'apport austénitique en utilisant de faibles énergies de soudage pour éviter la formation de zones à gros grains fragiles à basse température.
- Les aciers austénitiques sont les plus aptes au soudage. Le métal d'apport et les paramètres de soudage doivent être choisis avec soin afin que le joint soudé conserve les propriétés chimiques et mécaniques de l'acier de base.
- Les aciers austéno-ferritiques :
Article détaillé : Les aciers duplex.
On a toujours intérêt à privilégier les méthodes qui limitent dans le temps et en volume la fusion du métal : le soudage par résistance (par points, à la molette, par étincelage) donne d'excellents résultats et il ne faut pas oublier le brasage, qui ne provoque aucune fusion du métal de base. Le brasage diffusion sous vide donne d'excellents résultats pour l'assemblage de pièces usinées relativement petites et aux profils complexes (pièces d'horlogerie, micro-moteurs, prothèses, instrumentation...). Les brasures à l'argent donnent des joints très résistants mais le brasage au cuivre, à l'étain et, par voie de conséquence le soudo-brasage au laiton sont formellement proscrits car ils provoquent une décohésion granulaire et la ruine de l'assemblage.
Le meilleur moyen pour souder les aciers inoxydables, lorsque c'est possible, est le soudage avec métal d'apport austénitique. tous les procédés traditionnels sont utilisables, soudage à l'arc à l'électrode enrobée, le soudage à l'arc submergé, les procédés sous atmosphère inerte comme le TIG et le MIG, le soudage plasma. Le flux d´argon ou d'hélium autour de l'arc électrique empêche l'oxydation du bain de fusion ainsi que pendant le transfert du métal d'apport.
Rivetage et boulonnage
Les rivets donnent des joints bien serrés en raison de leur coefficient de dilatation élevé. Au-dessous de 5 mm on peut riveter à froid. L'étanchéité est généralement moins bonne que pour les aciers ordinaires, en raison de l'absence de rouille.
Il est bien entendu conseillé de ne pas « marier » les métaux de façon disparate, afin d'éviter la corrosion électrochimique que cela ne manquerait pas de provoquer. La visserie et la boulonnerie en acier inoxydable s'imposent donc tout naturellement.
Usinage
Du point de vue de l'usinage les aciers inoxydables peuvent être classés en deux catégories :
- Les aciers ferritiques et surtout martensitiques s'usinent pratiquement de la même manière que les aciers de construction classiques de même dureté, il est cependant conseillé de réduire légèrement les vitesses de coupe.
- Les aciers austénitiques se distinguent des aciers de construction ordinaires par leur faible limite d'élasticité, leur allongement important avant rupture et leur forte aptitude à l'écrouissage, ce qui oblige à modifier les conditions d'usinage dans des proportions parfois très importantes. D'une manière générale il faut utiliser des machines plus puissantes, très rigides, ne vibrant pas, et fixer très énergiquement les pièces que l'on veut travailler. On privilégiera les fortes profondeurs de passe à des vitesses relativement faibles.
Les angles de coupe doivent être les plus grands possibles pour accentuer la solidité des arêtes et faciliter l'évacuation de la chaleur.
Les liquides de coupe jouent un rôle particulièrement important dans le cas des aciers austénitiques. Une très forte onctuosité (capacité d'un lubrifiant à se fixer solidement aux parois par suite de divers phénomènes d'adsorption) est nécessaire : on utilisera donc des huiles minérales soufrées ou sulfochlorées additionnées éventuellement de corps gras comme l'huile de ricin ou de colza.
Découpage
Les aciers ferritiques et martensitiques se travaillent comme les aciers courants, mais pas les austénitiques. Ceux-ci ont une forte propension au grippage et il faut veiller à la bonne dépouille latérale des scies et des poinçons ; la puissance des machines doit être nettement plus élevée. Dans tous les cas on veillera à bien éliminer les parties endommagées, particulièrement dans le cas de découpage au chalumeau.
Traitements de surface
Le traitement de surface sert à améliorer l'état de surface d'un matériau donné.
La shoopisation est un traitement de surface parfois spécifié pour les pièces en acier doux destinées à être utilisés en extérieur (exposition aux intempéries).
Décapage et passivation
Il faut avant tout éliminer toute la calamine, les particules ferreuses plus ou moins adhérentes à la suite du passage dans les outillages de fabrication ou du brossage à la brosse métallique, les résidus d'outillages abrasifs (surtout s'ils ont auparavant servi à travailler des aciers ordinaires). Le décapage chimique et le sablage sont vivement conseillés.
Il faut toujours veiller à ce que les pièces que l'on met en service soient convenablement passivées, ce qui peut se faire si on les abandonne suffisamment longtemps à l'air ou si on les oxyde chimiquement pour gagner du temps.
Meulage et polissage
Pour éviter la contamination des surfaces, les outils de meulage et de polissage doivent autant que possible être réservés au travail des aciers inoxydables. Les pellicules graisseuses qui se forment souvent au cours de ces opérations doivent être soigneusement éliminées car elles isolent le métal et empêchent sa passivation.
Le polissage est indiqué seulement dans les cas où il peut réellement améliorer l'état de surface, on peut souvent s'en passer pour les tôles laminées à froid.
Autant que possible on soignera la qualité des soudures pour que l'on n'ait pas besoin de les parachever par meulage, car cette opération diminue leur résistance.
Le polissage électrolytique provoque généralement moins de pertes de matière que le polissage mécanique. Cependant il doit être conduit selon des prescriptions très strictes pour donner de bons résultats.
Entretien
Dans beaucoup de cas un nettoyage au savon suffit. Il existe des détersifs appropriés mais rien ne vaut en fin de compte l'acide nitrique qui élimine les dépôts et laisse une surface très bien passivée.
Références
- ↑ « Unieux (42) – Établissements Jacob Holtzer », sur le site jetons-monnaie.net.
- ↑ EN 10088-1 : Aciers inoxydables. - Partie 1 : liste des aciers inoxydables
- ↑ Michel Dupeux, Aide mémoire sciences des matériaux, éditions Dunod, Paris, 2004 (ISBN 2-10-005458-9), p. 212.
- ↑ a , b et c J. Barralis, G.Maeder, Métallurgie, élaboration, structures-propriétés, normalisation, collection « Les précis AFNOR/Nathan » , 2005 (ISBN 2-09-179582-8), p. 103.
- ↑ Pierre-Jean Cunat, « Aciers inoxydables, critères de choix et structures », traité « Matériaux métalliques », Techniques de l’ingénieur, mars 2000, p. M4540-3.
- ↑ Pierre-Jean Cunat, « Aciers inoxydables, critères de choix et structures », traité « Matériaux métalliques », Techniques de l’ingénieur, juin 2000, p. M4541-6.
- ↑ J. Philibert et al. Métallurgie, du minerai au matériau, Éditions Dunod, 2e édition, 2002, (ISBN 2-10-006313-8), p. 621.
- ↑ J. Barralis, G.Maeder, Métallurgie, élaboration, structures-propriétés, normalisation, collection « Les précis AFNOR/Nathan », 2005 (ISBN 2-09-179582-8), p. 102.
- ↑ J. Philibert et al, op. cit., p. 617.
- ↑ a et b Pierre-Jean Cunat, « Aciers inoxydables, critères de choix et structures », traité « Matériaux métalliques », Techniques de l’ingénieur, mars 2000, p. M4540-7.
- ↑ Pierre-Jean Cunat, « Aciers inoxydables, critères de choix et structures », traité « Matériaux métalliques », Techniques de l’ingénieur, mars 2000, p. M4540-8.
Voir aussi
- Philolaos est un sculpteur qui a réalisé dans le jardin des Gogottes de Guyancourt des sculptures en béton lavé et en acier inoxydable.
Liens
Articles sur l'inox LA SOLUTION FERRITIQUE Professionel de l'inox
- Portail de la chimie
- Portail de l’industrie
Catégories : Alliage | Acier | Couverture (construction)
Wikimedia Foundation. 2010.