- 5-fluoro-uracile
-
Fluorouracil
Fluorouracil 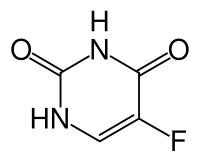
Structure chimique du fluorouracil Général Nom IUPAC 5-fluoro-2,4(1H,3H)-pyrimidinedione No CAS No EINECS Code ATC Apparence cristaux blancs presqu'inodores Propriétés chimiques Formule brute C4H3FN2O2 [Isomères] Masse molaire 130,0772 g∙mol-1
C 36,93 %, H 2,32 %, F 14,61 %, N 21,54 %, O 24,6 %,pKa 8,02 Propriétés physiques T° fusion 283 °C décomposition T° ébullition 190 à 200 °C (0,1 mmHg) Solubilité 11,1 g/L dans l'eau à 22 °C.
12,2 g/L dans l'eau à 20 °C.
2,9 g/L éthanol à 20 °C.
Soluble dans DMSO.
Facilement soluble dans des solutions aqueuses alcalinesPrécautions Directive 67/548/EEC 
XnPhrases R : 20/21/22, 36/37/38, 63, 68, Phrases S : 26, 36/37/39, Classification du CIRC Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[1] Écotoxicologie DL50 115 mg/kg souris oral
81 mg/kg souris i.v.
169 mg/kg souris s.c.
100 mg/kg souris i.p.Données pharmacocinétiques Métabolisme Intracellulaire et hépatique Demi-vie d’élim. 5-20 min. Excrétion Rénale et par les poumons Considérations thérapeutiques Voie d’administration parentérale ou topique Grossesse chimiothérapie :
Médicament dangereux pour l'embryon et le fœtus
Une contraception doit être envisagée chez les femmes en âge de procréer.Précautions Statut légal en Belgique : sous ordonnance,
y compris les formes topiquesUnités du SI & CNTP, sauf indication contraire. Le fluorouracile (5-FU) ou 5-fluorouracile est un médicament utilisé dans le traitement du cancer. Il appartient à la classe des médicaments antimétabolites, sous-classe des analogues de la pyrimidine.
Sommaire
Mécanisme d'action
L'uracile intervient dans la biosynthèse des acides nucléiques à deux niveaux :
- Il est incorporé dans l'ARN sous forme d'UTP (uridine triphosphate)
- Il constitue la source principale de dTTP (désoxythymidine triphosphate) qui sera incorporé dans l'ADN. La thymidylate synthétase est la seule enzyme qui permet la synthèse de ce nucléotide.
Le 5-FU doit être métabolisé dans la cellule pour être actif en subissant les mêmes réactions enzymatiques que les nucléotides normaux. Il agit principalement sur la synthèse d'ADN sous forme de 5-FdUMP (5 fluorodésoxy-uracile monophosphate) en bloquant l'activité de la thimidylate synthétase. De plus, un autre de ses métabolites (le 5-FUTP) a la capacité de s'incorporer dans les divers types d'ARN. La transcription se fera de manière erronée.
Formes parentérales
Son indication principale est en cas de cancer du côlon ou de l'anus, dans lequel il a été pendant des décennies le traitement chimiothérapeutique de premier choix. Depuis peu, les médicaments à base de platine sont venus s'y ajouter.
En tant qu'analogue de la pyrimidine, le fluorouracil est transformé au sein de la cellule en différents métabolites cytotoxiques qui seront incorporés dans l'ADN et l'ARN, induisant au bout du compte l'arrêt du cycle cellulaire et l'apoptose.
Formes topiques
Traitement local dans certaines kératoses et tumeurs cutanées
 Fluorouracil (topique)
Fluorouracil (topique)
Noms commerciaux :
- Efudix® crème (Belgique, France, Suisse)
En Suisse, il existe également le Verrumal®, une solution consistant en une association de médicaments à base de fluorouracil et d'acide salicylique (Traitement des verrues)
Autres informations :
Sous classe :
NB : capécitabine
La capécitabine est une prodrogue qui est convertie en 5-FU dans les tissus. Elle peut être administrée par voie orale.
Notes et références
- ↑ IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme » sur http://monographs.iarc.fr, 16 janvier 2009, CIRC. Consulté le 22 août 2009
- Portail de la médecine
- Portail de la pharmacie
- Portail de la chimie
Catégories : Composé du fluor | Produit chimique nocif | Antimétabolite | Pyrimidinedione | Composé organo-fluoré
Wikimedia Foundation. 2010.
