- Raltégravir
-
raltégravir 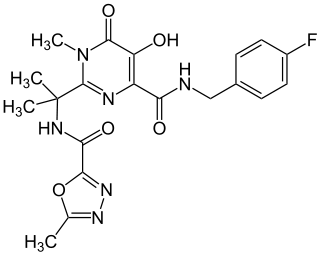
Général Nom IUPAC N-(2-(4-(4-fluorobenzylcarbamoyl) -5-hydroxy-1-methyl-6-oxo-1,6-dihydropyrimidin -2-yl)propan-2-yl)-5-methyl -1,3,4-oxadiazole-2-carboxamide No CAS SMILES InChI Propriétés chimiques Formule brute C20H21FN6O5 [Isomères] Masse molaire[1] 444,4163 ± 0,0202 g·mol-1
C 54,05 %, H 4,76 %, F 4,27 %, N 18,91 %, O 18 %,Classe thérapeutique Antirétroviral : Inhibiteur d'intégrase Données pharmacocinétiques Biodisponibilité "bonne" Considérations thérapeutiques Voie d’administration Orale Grossesse Contre-indiquée
(catégorie C)Précautions surveiller la créatine kinase Unités du SI & CNTP, sauf indication contraire. Le raltégravir est la dénomination commune internationale de l'Isentress, un inhibiteur de l'intégrase du VIH qui a obtenu son AMM européenne le 20 décembre 2007[2]. Cette molécule, brevetée par les laboratoires Merck & Co., est également connue sous son ancien nom de code, MK-0518[3]. Plus précisément, il s'agit d'un inhibiteur de transfert de brins (INtegrase Strand Transfer Inhibitor, INSTI).
Sommaire
Posologie et effets secondaires
La posologie habituelle est de 400 mg, deux fois par jour (un essai conduit par Merck a évalué l'efficacité d'une monoprise quotidienne de 800 mg mais a conclu que cette posologie était moins efficace[4],[5],[6]). Les comprimés ne doivent pas nécessairement être ingérés avec des aliments, contrairement à d'autres antirétroviraux.
Les effets secondaires semblent inexistants, ou du moins comparables à ceux rencontrés lors de l'administration d'un placebo : nausées, vertiges, diarrhées. Chez certains patients, on a toutefois pu observer une augmentation du taux de créatine kinase, sans pouvoir établir que ce problème était dû au médicament[7]. Chez d'autres, très peu nombreux, une dépression préexistante a empiré temporairement à l'instauration du traitement sous Isentress, nécessitant même une hospitalisation dans un cas[8]. À noter également : plus de quatre ans après l'approbation du médicament par la FDA, celle-ci a fait rajouter début novembre 2011 un avertissement dans la notice des boîtes d'Isentress, afin de prévenir de la survenue, dans quelques cas très rares, du syndrome de Stevens-Johnson chez certains patients[9].
Toujours sur le point des effets secondaires, il convient toutefois d'appliquer le principe de précaution, le raltégravir étant une des seules molécules agissant sur l'intégrase du virus disponibles à l'heure actuelle; on ne connaît pas de possibles effets secondaires à long terme (éventuel risque de cancer[10]). De plus, il faut souligner qu'on ne sait pas ce qu'il advient de l'ADN proviral, qui n'est plus intégré au génome de la cellule. Il faut également remarquer que les essais sur les animaux ont montré une activité délétère sur le fœtus[11].
Efficacité et accessibilité
La molécule semble très puissante, malgré le peu de recul qu'on a sur son utilisation. Elle permet notamment d'atteindre une charge virale indétectable plus rapidement qu'avec une trithérapie comprenant de l'éfavirenz[12].
Certaines souches de virus sont cependant résistantes à ce médicament, du fait d'une mutation sur le gène de l'intégrase[13].
Le médicament a obtenu l'accord de la FDA pour une mise sur le marché aux États-Unis en octobre 2007. Le prix d'une boîte de 60 comprimés (30 jours de traitement) était de 902,31€[14] en France lors de la mise sur le marché, mais Merck a revu le prix à la baisse : le prix pour un mois de traitement est en 2011 de 772,43€[15].
À noter également : le raltégravir se diffuse bien dans le système nerveux central[16] et le tractus génital[17], ce qui permet de diminuer respectivement le vieillissement du cerveau et la possibilité de contamination en cas de rapport sexuel non protégé. Le raltégravir est efficace contre le VIH-2[18], contrairement aux INNTI.
Le raltégravir a également fait ses preuves en tant que remplaçant de l'enfurvitide[19]; l'Isentress remplaçant les injections bi-quotidiennes de Fuzeon, jugées difficiles à vivre par les patients. L'essai Trio (ANRS 139) a montré que dans le cadre d'une multithérapie, l'Isentress permettait d'obtenir, en association avec d'autres molécules récentes, un résultat «spectaculaire» sur des patients en échec thérapeutique[20].
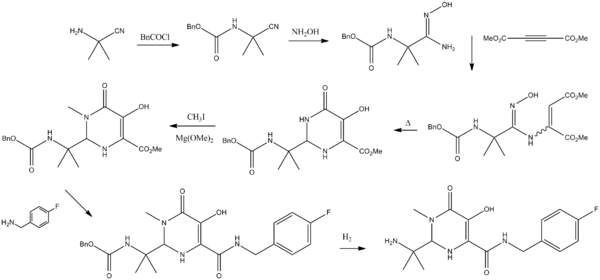
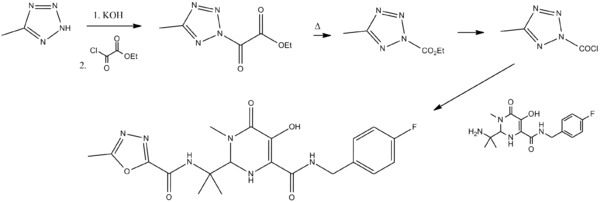
Synthèse de la molécule
K. M. Belyk, H. G. Morrison, P. Jones et V. Summa, 2007. Brevet WO 2006060730.
Perspectives
Deux essais visant à dispenser un traitement sans analogues nucléosidiques ou nucléotidiques ont été conduits : l'essai Spartan (raltégravir associé à de l'atazanavir non boosté), dont les résultats sont mitigés, et l'essai Progress (raltégravir associé au Kaletra), plus concluant[21].
La molécule, associée au maraviroc, permettrait de diminuer l'inflammation du système nerveux central causée par le VIH[22].
Des essais sont conduits afin de déterminer si l'Isentress, en association avec d'autres molécules, antirétrovirales ou non, permettrait de diminuer voire de supprimer les réservoirs viraux.
De récentes recherches ont également démontré que le raltégravir était actif sur certaines souches du HSV; des études pourraient mener à la création d'un médicament efficace contre tous les virus de la famille de l'herpès[23].
Liens externes
- Une fiche à propos du raltégravir sur HIV Medication Guide (en français)
- Notice de l'Isentress sur le site de l'AFSSAPS
- (en) Un memento complet sur aidsmeds.com
- (en) Le site officiel, www.isentress.com
- Du nouveau sur les inhibiteurs d’intégrase, sur le site actions-traitements.org
- Plan de gestion de risque sur le site de l'AFSSAPS
Autres inhibiteurs d'intégrase en développement
Deux autres molécules de la classe des anti-intégrase : l'elvitégravir de Gilead Sciences/Japan Tobacco, le MK-2048, elle aussi développée par Merck & Co. et le dolutégravir de ViiV Healthcare.
Références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) EPARs for authorised medicinal products for human use : Isentress
- Nouvelles molécules en développement : Mythiques anti-intégrases
- (en) Merck Testing Once-Daily Isentress sur aidsmeds.com
- Raltégravir en une prise par jour sur actions-traitements.org
- Isentress Once-Daily Is Less Effective Than Twice-Daily sur aidsmeds.com
- Résumé des caractéristiques du produit, page 8
- (en) Worsening Depression in Four Patients on Isentress sur aidsmeds.com
- (en) FDA Warns of Serious Skin Reactions Among Isentress Users sur aidsmeds.com
- Préoccupations concernant le risque de cancer associé au raltégravir (CATIE TraitementSida 173, Juin 09) sur actions-traitements.org
- Résumé des caractéristiques du produit, page 7
- http://www.medscape.com/viewarticle/707219 (en) Compared with patients receiving efavirenz, those receiving raltegravir had a shorter time to achieve viral suppression sur medscape.com
- Malet I, Delelis O, Valantin MA, et als. (en) Mutations associated with failure of raltegravir treatment affect integrase sensitivity to the inhibitor in vitro, Antimicrob Agents Chemother, 2008;52:1351-1358
- Isentress en pharmacies de ville sur seronet.info
- Fiche de l'Isentress sur doctissimo.fr
- http://www.groupesida.ch/filrouge/assets/pdf/remaides-73-suisse.pdf Remaides n°73, page 9
- http://www.edimark.fr/ejournaux/croi2010/19fev/breves.php?PHPSESSID=1gcrpsd52f8ml8kmd16ltn6217#1433 "Raltégravir dans le tractus génital : ça passe !" sur edimark.fr
- Feuillet d'information : Raltégravir (Isentress) sur catie.ca
- Essai EASIER (ANRS 138) sur actupparis.org
- Essai ANRS 139 Trio : des résultats spectaculaires sur vih.org
- http://www.vih.org/20100716/vienne-2010-j-2-il-parait-que-15993 Vienne 2010, J-2 : Il paraît que…], article de Gilles Pialoux sur vih.org
- (en) ART Intensification with Maraviroc (Selzentry) or Raltegravir (Isentress) May Improve Immune Activation and Inflammation sur hivandhepatitis.com
- (en) HIV Drug Isentress Could Fight All Herpes Viruses sur aidsmeds.com
Catégories :- Antirétroviral
- Pyrimidone
- Amide
- Lactame
- Alcool (chimie)
- Oxadiazole
- Fluorobenzène
- Énol
- Inhibiteur d'intégrase
Wikimedia Foundation. 2010.