- 56-41-7
-
Alanine

Cet article possède un paronyme, voir : Aniline. Alanine 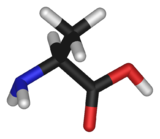
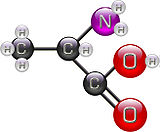
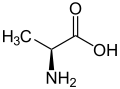
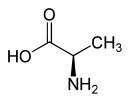
L ou S(+)-alanine et D ou R(-)-alanine Général Nom IUPAC acide (S)-2-aminopropanoïque Synonymes A, Ala No CAS (racémique)
L ou S(+)
D ou R(-)No EINECS (racémique)
D
LNo E E639 (DL) FEMA Propriétés chimiques Formule brute C3H7NO2 [Isomères] Masse molaire 89,0932 g∙mol-1
C 40,44 %, H 7,92 %, N 15,72 %, O 35,92 %,pKa 2,35
9,69Propriétés physiques T° fusion 295 °C à 297 °C Solubilité 166,5 g/L dans l'eau à 25 °C;
difficilement soluble dans l'alcoolMasse volumique 1,4 g/cm³ Propriétés biochimiques Codons GCU, GCC, GCA, GCG pH isoélectrique 6,11 Acide aminé essentiel Non Propriétés optiques Pouvoir rotatoire [α]D -14,1° (0,9 g/100ml dans HCl 1N, D ou R)[1]
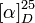 +2,42° (10g/100ml dans H2O, L ou S)[1]
+2,42° (10g/100ml dans H2O, L ou S)[1]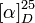 +13,7° (2,06 g/100ml dans HCl 6N, L ou S)[1]
+13,7° (2,06 g/100ml dans HCl 6N, L ou S)[1]Précautions SIMDUT[2] Produit non contrôlé Unités du SI & CNTP, sauf indication contraire. La L-alanine est un des 20 acides aminés les plus courants. Elle est hydrophobe, possède un groupement méthyle latéral, et est le deuxième plus petit acide aminé parmi les 20 derrière la glycine. L’alanine est un acide aminé non essentiel et a été isolée dès 1879. La dénomination IUPAC est acide amino-2 propionique ou acide α-aminopropionique.
On trouve également dans la nature l'énantiomère D-alanine, qui participe en particulier à la construction du peptidoglycane, le constituant principal de la paroi des bactéries. La D-alanine est formée à partir de L-alanine par l'action d'une isomérase, l'alanine racémase.
La L-alanine est créée dans les cellules musculaires au départ du glutamate dans un processus appelé transamination. Dans le foie, l’alanine se transforme en pyruvate. De plus, l’alanine amino transférase (ALAT) catalyse la réaction dans laquelle le groupement aminé de l’alanine est transféré au α-cétoglutarate. C'est un acide aminé aliphatique.
Sommaire
Synthèse
L'alanine est un des 21 acides aminés que l'on trouve dans les chaînes peptidiques des protéines. On fait agir le malonate d'éthyle sur l'éthanoate de sodium.L'anion obtenu réagit sur le bromoéthane en milieu basique puis une saponification suivie d'un passage en milieu acide.Puis on fait réagir le dibrome en présence de phosphore. Enfin l'action de l'ammoniac en excès suivie d'une hydrolyse acide permet d'obtenir l'alanine
Bêta-alanine
La bêta-alanine est l'acide 3-aminopropionique ou acide β-aminopropanoïque. En France, elle est présente dans la spécialité pharmaceutique ABUFENE® qui est censée agir sur la vasodilatation lors de bouffées de chaleur[réf. nécessaire].
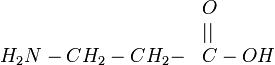
Structure chimique de la bêta-alanine
Des dérivés de la β-alanine découvert en 1948 ont une saveur sucrée plus intense que le saccharose, par exemple le suosan qui a un pouvoir sucrant de 350[3].
Notes et références
- ↑ a , b et c (en) Maryadele J. O'Neil, Ann Smith, Patricia E. Heckelman, Susan Budavari, The Merck Index: An Encyclopedia of Chemicals, Drugs and Biologicals, 13th edition, MERCK & CO INC, 2001, 2564 p. (ISBN 0911910131)
- ↑ « Alanine (l-) » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ (en) (en) AD Kinghorn & CM Compadre, Alernative Sweeteners: Third Edition, Revised and Expanded, Marcel Dekker, New York, 2001 (ISBN 0-8247-0437-1), « Less common high-potency sweeteners », p. 208-234
Voir aussi
Articles connexes
Liens externes
Ala | Arg | Asn | Asp | Cys | Glu | Gln | Gly | His | Ile | Leu | Lys | Met | Phe | Pro | Ser | Thr | Trp | Tyr | Val Acide aminé essentiel | Protéine | Peptide | Code génétique - Portail de la biochimie
- Portail de la chimie
Catégorie : Acide aminé
Wikimedia Foundation. 2010.
