- Acide déshydroascorbique
-
Acide déshydroascorbique 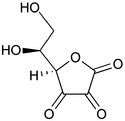
Structure de l'acide L-déshydroascorbiqueGénéral No CAS No EINECS PubChem ChEBI SMILES InChI Propriétés chimiques Formule brute C6H6O6 [Isomères] Masse molaire[1] 174,1082 ± 0,007 g·mol-1
C 41,39 %, H 3,47 %, O 55,14 %,Unités du SI & CNTP, sauf indication contraire. L’acide déshydroascorbique est une forme oxydée de l'acide ascorbique, dont l'énantiomère L est la vitamine C. L'acide ascorbique (L ou D) est en effet un composé réducteur jouant le rôle d'antioxydant dans les cellules vivantes, où il est oxydé en acide déshydroascorbique, lequel peut à son tour être réduit à nouveau en acide ascorbique par des enzymes ou par le glutathion[2]. Le glutathion est déterminant pour accroître les propriétés antioxydantes du sang[3], car en son absence des quantités bien plus importantes d'acide ascorbique seraient nécessaires.
Bien que l'acide ascorbique soit absorbé plus efficacement par l'organisme sous forme d'acide déshydroascorbique, la concentration de ce dernier dans le plasma sanguin et dans les tissus demeure normalement faible, car les cellules le réduisent rapidement en acide ascorbique[4],[5]. C'est la raison pour laquelle l'acide L-déshydroascorbique est doté d'activité vitaminique C au même titre que l'acide L-ascorbique.
La structure réelle de la molécule en solution est plus complexe que celle traditionnellement indiquée dans les manuels, car la configuration 1,2,3-tricarbonyle est trop électrophile pour subsister plus de quelques millisecondes en solution aqueuse. Les analyses réalisées par spectroscopie ont révélé la formation rapide d'un hémiacétal entre l'hydroxyle –OH en position 6 et le carbonyle C=O en position 3 :
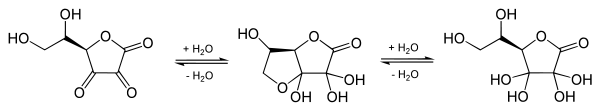 Équilibre entre les formes anhydre et hydratées de l'acide déshydroascorbique. L'hémiacétal central est la forme prédominante.
Équilibre entre les formes anhydre et hydratées de l'acide déshydroascorbique. L'hémiacétal central est la forme prédominante.
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) Alton Meister, « Glutathione-ascorbic acid antioxidant system in animals. », dans The Journal of biological chemistry, vol. 269, no 13, 1994, p. 9397-9400 [texte intégral, lien PMID]
- (en) S. S. Gropper, J. L. Smith, J. L. Grodd, Advanced Nutrition and Human Metabolism, Belmont, CA. USA, Thomson Wadsworth, 2004, 4the éd., p. 260-275.
- (en) J May, « Recycling of vitamin C from its oxidized forms by human endothelial cells », dans Biochimica et Biophysica Acta (BBA) - Molecular Cell Research, vol. 1640, 2003, p. 153–61 [lien DOI]
- (en) L. Packer, « Vitamin C and redox cycling antioxidants » dans Vitamin C in health and disease, Marcel Dekker Inc, New York, 1997.
Wikimedia Foundation. 2010.
