- Glutamate monosodique
-
Glutamate monosodique 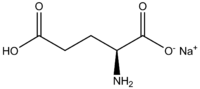
Général Nom IUPAC (2S)-2-amino-5-hydroxy-5-oxo
-pentanoate de sodiumSynonymes Sel sodique de l'acide glutamique
Sel de glutamateNo CAS (L(+) anhydre)
(L(+) monohydrate)No EINECS PubChem No E E621 FEMA Apparence Poudre blanche cristalline Propriétés chimiques Formule brute C5H8NNaO4 [Isomères] Masse molaire[1] 169,1111 ± 0,006 g·mol-1
C 35,51 %, H 4,77 %, N 8,28 %, Na 13,59 %, O 37,84 %,
187,13 g/mol (monohydrate)Propriétés physiques T° fusion 225 °C (décomposition)[2] Solubilité 739 g·l-1 (eau, 25 °C),
pratiquement insol. dans l'huile ou les solvants organiques[2]Unités du SI & CNTP, sauf indication contraire. Le glutamate monosodique (E621), communément nommé glutamate ou encore GMS (MSG en anglais), est utilisé principalement comme exhausteur de goût dans l'alimentation.
Sommaire
Histoire
Il a été découvert, dans une algue kombu en 1908 par le professeur japonais Kikunae Ikeda qui breveta son invention avec l'aide de Saburosuke Suzuki II de la compagnie Suzuki Seiyakusho Co. qui allait devenir Ajinomoto. [réf. nécessaire]
Son procédé de fabrication a été breveté la même année. La production en 2003 est de plus de 1,5 million de tonnes dont 80 % seraient consommés en Asie. On évalue à 95 000 tonnes la consommation en Europe.[réf. nécessaire]
Son code dans le système harmonisé de l'organisation mondiale des douanes est le 29224220.
Structure et propriétés
La dénomination du glutamate monosodique dans la nomenclature de l'Union internationale de chimie pure et appliquée (IUPAC) est le (S)-2-amino-5-hydroxy-5-oxo-pentanoate de sodium .
Sa formule chimique est C5H8NNaO4 et sa masse molaire est de 169,13 g/mol.
Dans sa forme pure, le glutamate monosodique a l'apparence d'une poudre blanche et cristalline.
Le glutamate monosodique est l'un des sel de l'acide glutamique, un acide aminé naturel. Quand il est dissous dans l'eau, ou la salive, il se décompose rapidement en ions sodium et ion glutamate (le glutamate est la forme anionique de l'acide glutamique).
L'acide glutamique
Dans la culture alimentaire japonaise, l'acide glutamique est responsable de l'un des cinq goûts, l'umami. En tant que condiment et exhausteur de goût, il est fréquemment utilisé dans les cuisines asiatiques.
Utilisation
Le glutamate monosodique est un additif alimentaire autorisé par l'union européenne (E621[3]). Il est principalement utilisé sous sa forme mono hydraté[4]. Cependant d'autres sels de l'acide glutamique sont aussi utilisés[3] :
- Glutamate monopotassique (E622)
- Diglutamate de calcium (E623)
- Glutamate d’ammonium (E624)
- Diglutamate de magnésium (E625)
Les sels de l'acide glutamique sont autorisés dans les denrées alimentaires en général (à l’exception de celles mentionnées à l’article 2 paragraphe 3 de la directive 95/2/CE) jusqu'à un maximum de 10 g·kg-1 seul ou en mélange. Il n'y a pas de limitation d'usage dans les condiments et assaisonnements (quantum satis (la))[3]. Ils appartiennent à la catégorie des exhausteurs de goût[5].
Controverse
Chez certaines personnes, le glutamate monosodique peut provoquer des réactions de type allergique ou une réaction d'hypersensibilité comme une sensation de brûlure, de pression faciale, des maux de tête, des nausées ou encore des douleurs thoraciques se manifestant une vingtaine de minutes après l'ingestion pour une durée d'environ deux heures. Généralement, ces réactions sont temporaires et ne présentent pas d'effets néfastes pour la santé sur le long terme[6].
Le premier symptôme serait un "flush" (coloration rouge intense et passagère du visage, du cou et du torse). Pourrait apparaitre aussi : yeux injectés de sang, céphalées, sensation de brûlures survenant au niveau du tronc et irradiant vers la périphérie, impression d'oppression thoracique, brûlures de la tête, bouffées de chaleur, nausées et vomissements, sensation d'étouffement, difficultés à respirer, tendance à faire des malaises...Cette affection surviendrait un quart d'heure à une demi-heure après ingestion et pourrait durer jusqu'à deux heures. La puissance de cette réaction ne serait pas proportionnelle à la dose ingérée, quelques milligrammes suffiraient. Son lien avec l'ingestion de glutamate n'est pas scientifiquement prouvé.[réf. nécessaire] À peu près une personne sur 5 000 serait sensible à son ingestion, mais curieusement une sur 50 000 dans les pays asiatiques.
Usage
Selon Santé Canada, de nombreux aliments "peuvent contenir des concentrations élevées de glutamate libre d'origine naturelle : les tomates et le jus de tomate, les raisins et le jus de raisin, d'autres jus de fruits, les champignons et des fromages tels que le parmesan ou le Roquefort. Le glutamate libre est aussi présent dans des ingrédients tels que les légumes et les protéines végétales hydrolysés, de même que dans les extraits de levure autolysée. Dans son rapport sur les réactions indésirables au glutamate monosodique, la Federation of American Societies for Experimental Biology (FASEB)1 conclut qu'il n'existe aucune différence entre les réactions physiologiques aux glutamates artificiels et celles provoquées par les glutamates naturels."[7]
De nombreux aliments utilisés dans la cuisine occidentale sont naturellement riches en glutamate monosodique comme l'asperge verte (106mg/100g), la coquille saint jacques (140mg/100g) et la tomate (246 mg/100g) et, malgré leur fort taux en glutamate, ils ne sont pas connus pour être des déclencheurs de migraines, mais des intolérances ou allergies à ces produits sont régulièrement rapportées.
Il est actuellement utilisé couramment en combinaison avec des arômes dans les apéritifs (goût bacon, goût fromage, ...).Il est un composant important des auxiliaires de cuisine ("bouillons cubes", fonds de sauces, sauces, etc). Il est à noter que les produits portant la mention "Bio" comportent rarement du glutamate monosodique.
Recherches sur l'obésité
Le glutamate monosodique, administré à des rats à leur naissance, les rend systématiquement obèses. Ce traitement est donc couramment employé dans les recherches sur l'obésité[8],[9] ; des recherches sur l'homme commencent à présenter des résultats similaires[10].
Toxicité chez l'homme
Le conseil européen de l'information sur l'alimentation (EUFIC), organisme financé par l'industrie agroalimentaire, considère que « le glutamate monosodique est un ingrédient alimentaire qui souffre souvent d’une mauvaise réputation, pourtant infondée ». En se basant sur des études scientifiques publiées entre 1988 et 2000, l'organisme public affirme que « le glutamate monosodique peut être utilisé en toute sécurité pour ajouter du goût ou pour réduire les taux du sodium présent dans les aliments »[11].
Les avis de l'EUFIC, de la JECFA (FAO/OMS) et de la FASEB (Federation of American Societies for Experimental Biology) contredisent toutes les études menées il y a plus de cinquante ans par D. R. Lucas et J. P. Newhouse. Ceux-ci affirmaient, en 1957, avoir observé la toxicité du glutamate quand, après avoir nourri des souris nouveau-nées avec du glutamate monosodique, ils ont constaté la destruction de neurones dans la couche interne de leur rétine[12]. Vers 1969, J. Olney affirma avoir découvert que ce phénomène n'était pas limité à la rétine, mais concernait tout le cerveau, et il le nomma alors excitotoxicité. Olney affirma également que cette mort cellulaire ne concernait que les neurones post-synaptiques, que la neurotoxicité des agonistes du glutamate était proportionnelle à leur efficacité à activer les récepteurs aux glutamates, et que les antagonistes des glutamates pouvaient inhiber cette neurotoxicité[13]. Le mécanisme de l'excitotoxicité serait désormais mieux connu. L'acide glutamique et ses analogues pourraient être responsables de l'hyperexcitation des récepteurs excitateurs neuronaux comme les récepteurs NMDA et AMPA. Ce mécanisme physiopathologique est incriminé dans un certain nombre de maladies neurologiques.
En 1986, l'administration américaine des denrées alimentaires et des médicaments (FDA) a déterminé que le glutamate monosodique (GMS) était GRAS (Generally Recognized As Safe, c'est-à-dire généralement reconnu comme sûr), mais que des réactions brèves peuvent apparaître chez certains individus. En 1995 un rapport de la Federation of American Societies for Experimental Biology (FASEB) a réaffirmé le caractère GRAS du GMS et n'a trouvé aucun lien entre le GMS et une toxicité à long terme (telle que les maladies d'Alzheimer et de Huntington) ou de toxicité chronique. Aucune évidence de causes de lésions cérébrales ou dommages nerveux n'a été décelée. Cependant le rapport a identifié des réactions complexes aux GMS dans deux groupes type d'individus. Le premier groupe concerne les personnes qui consomment une grande quantité de GMS (plus de 3 g par repas), en particulier à jeun. Une quantité typique de consommation est d'environ 0,5 gramme. Le second groupe inclut les personnes avec une forme sévère d'asthme[14].
Le glutamate monosodique peut causer chez certaines personnes des réactions de type allergique ou d'hypersensibilité. En règle générale ces sensations apparaissent vingt minutes après la consommation et disparaissent environ deux heures plus tard. On ne considère pas que ces réactions ont un effet sur la santé à long terme, mais il est recommandé aux personnes qui y sont sujettes d'éviter la consommation de MSG[15].
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- MONOSODIUM GLUTAMATE sur Hazardous Substances Data Bank. Consulté le 3 février 2010
- Parlement européen et Conseil de l'europe, « La Directive 95/2/CE concernant les additifs alimentaires autres que les colorants et les édulcorants », dans Journal officiel de l'Union européenne, no L 61, 20/02/1995, p. 1-56 [texte intégral (page consultée le 19/05/2008)].[PDF]
- Commission européenne, « DIRECTIVE 2001/30/CE modifiant la directive 96/77/CE établissant des critères de pureté spécifiques pour les additifs alimentaires autres que les colorants et les édulcorants », dans Journal officiel de l'Union européenne, no L 146, 2001 [texte intégral (page consultée le 11/07/2008)].
- (en) JECFA, « MONOSODIUM L-GLUTAMATE », Jecfa Monograpf sur www.fao.org, FAO, 2006. Consulté le 11 juillet 2008.
- Foire aux questions sur le glutamate monosodique (MSG) sur le site gouvernemental de santé canada
- Foire aux questions sur le glutamate monosodique, sur le site de Santé Canada, consulté le 16 janvier 2011
- A.E. Hirata, I.S. Andrade, P. Vaskevicius and M.S. Dolnikoff, « Monosodium glutamate (MSG)-obese rats develop glucose intolerance and insulin resistance to peripheral glucose uptake », 20. Consulté le 16 février 2010
- Gobatto, C. A., Mello, M. A. R., Souza, C. T., Ribeiro, I. A., « The monosodium glutamate (MSG) obese rat as a model for the study of exercise in obesity. ». Consulté le 16 février 2010
- Jeremiah Stamler et al, « Association of Monosodium Glutamate Intake With Overweight in Chinese Adults: The INTERMAP Study », 22. Consulté le 16 février 2010
- Le glutamate monosodique, FOOD TODAY sur www.eufic.org, Novembre 2002. Consulté le 11 juillet 2008.
- (en) Lucas DR, Newhouse JP. The toxic effect of sodium L-glutamate on the inner layers of the retina. AMA Arch Ophthalmol. 1957 Aug;58(2):193-201. PMID 13443577
- (en) Olney JW. Brain lesions, obesity, and other disturbances in mice treated with monosodium glutamate. Science 1969 May 9;164(880):719-21. PMID 5778021
- (en) Michelle Meadows, « MSG: A Common Flavor Enhancer » sur www.fda.gov, FDA/Office of Public Affairs, 2003. Mis en ligne le 06/01/2003., consulté le 11 juillet 2008.
- Foire aux questions sur le glutamate monosodique, sur le site de Santé Canada, consulté le 13 septembre 2010
Voir aussi
Articles connexes
- Excitotoxicité
- Neurotoxicité
- Récepteur du glutamate
- Aspartame
- Portail de la chimie
- Portail de l’agriculture et l’agronomie
Catégories :- Composé du sodium
- Sel d'acide carboxylique
- Exhausteur de goût
- Goût umami
- Hydrate
Wikimedia Foundation. 2010.

