- Acide fluorosulfurique
-
Acide fluorosulfurique 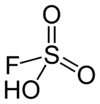

Structure de l'acide fluorosulfurique.Général Nom IUPAC acide fluorosulfurique Synonymes acide fluorosulfonique No CAS No EINECS No RTECS PubChem SMILES InChI Apparence liquide incolore Propriétés chimiques Formule brute HFSO3 Masse molaire[1] 100,07 ± 0,006 g·mol-1
H 1,01 %, F 18,99 %, O 47,96 %, S 32,04 %,pKa -10 Propriétés physiques T° fusion -87,3 °C T° ébullition 165,5 °C Solubilité Soluble dans l'eau Masse volumique 1,84 (liquide) Précautions Directive 67/548/EEC 
CPhrases R : 20, 35, Phrases S : (1/2), 26, 45, SIMDUT[2] 

SGH[3] 
DangerUnités du SI & CNTP, sauf indication contraire. L'acide fluorosulfurique, également appelé acide fluorosulfonique, est un composé chimique de formule HFSO3. C'est un liquide peu visqueux, soluble dans les solvants polaires tels que le nitrobenzène, l'acide acétique et l'acétate d'éthyle, mais peu soluble dans les solvants apolaires tels que les alcanes. Il s'agit d'un superacide de pKa égal à -10 dont le mélange équimolaire avec le pentafluorure d'antimoine SbF5 donne l'acide magique HFSO3·SbF5, un acide parmi les plus forts connus. Cette acidité lui permet de dissoudre pratiquement n'importe quelle substance organique, même les composés faiblement accepteurs de protons.
HFSO3 s'hydrolyse lentement en acide fluorhydrique et acide sulfurique ; l'acide triflique HSO3CF3, qui lui est structurellement apparenté, est plus stable dans l'eau.
Sommaire
Propriétés
L'acide fluorosulfurique peut être vu comme une molécule d'acide sulfurique où un groupe -OH aurait été remplacé par un atome de fluor. L'électronégativité du fluor, supérieure à celle de l'oxygène, entraîne une augmentation de l'acidité du produit obtenu.
Préparation
On prépare l'acide fluorosulfurique en faisant réagir du fluorure d'hydrogène HF sur du trioxyde de soufre SO3 :
Une autre façon procéder consiste à attaquer du bifluorure de potassium KHF2 ou du fluorure de calcium CaF2 par de l'oléum H2S2O7 à 250 °C puis à distiller HFSO3 après en avoir éliminé le fluorure d'hydrogène par circulation d'un gaz rare.
Utilisation
L'acide fluorosulfurique est utilisé pour produire des mélanges de HF et H2SO4 pour graver le cristal. Il favorise l'isomérisation les alcanes et l'alkylation des hydrocarbures avec des alcènes, bien qu'on ne sache pas encore si cette réaction peut avoir un intérêt industriel. Il peut également être utilisé en laboratoire comme agent de fluoration.
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- « Acide fluorosulfonique » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
Catégories :- Produit chimique corrosif
- Oxoacide de soufre
- Composé du fluor
- Superacide
Wikimedia Foundation. 2010.
