- Zeolite
-
Zéolithe
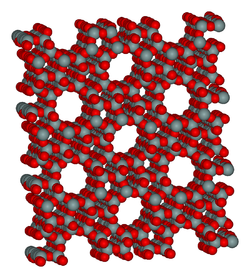
 Natrolite ; zéolithe de formule Na2[Si3AlO10] (Val de Fassa à Monzoni (Italie). Le caractère fibreux de certaines zéolithes les rend susceptible de produire des mésothéliomes (comme l'amiante) si elles sont inhalées en fines particules
Natrolite ; zéolithe de formule Na2[Si3AlO10] (Val de Fassa à Monzoni (Italie). Le caractère fibreux de certaines zéolithes les rend susceptible de produire des mésothéliomes (comme l'amiante) si elles sont inhalées en fines particules
Une zéolithe, ou zéolite (du latin zeolithus, du grec zeô ou zein : « bouillir » et lithos : « la pierre ») est un minéral appartenant à la famille des aluminosilicates hydratés de métaux des groupes IA et IIA du tableau périodique des éléments, tels le calcium, le magnésium et le potassium).
Sommaire
Composition chimique
La composition des différentes zéolithes est proche de celle des argiles. Leur formule chimique, très variable, respecte le squelette suivant : Nax1Cax2Mgx3Bax4Kx5Alx6[Six7Ox8], x9 H2O, où x1 à x9 sont des entiers positifs ou nuls.
Par exemple, la natrolite a pour formule Na2[Si3Al2O10], 2 H2O et l'heulandite (Ca, Na2)2[Si7Al2O18], 6 H2O.
Structure
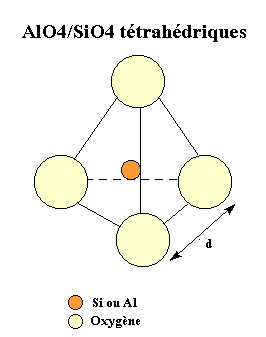 AlO4 ou SiO4 tétraédriques
AlO4 ou SiO4 tétraédriques
Les zéolithes sont des polymères inorganiques cristallins structurellement complexes, basés sur une suite indéfinie tridimensionnelle de structures quadri-connectées de AlO4 et de SiO4 tétraédriques, liées entre elles par un échange d'ions oxygène (oxyde). Chaque AlO4 tétraédrique présent dans la structure apporte une forte charge négative qui est contre-balancée par un ou plusieurs cations, tels Ca2+, Mg2+ ou K+.
Origine
Les zéolithes peuvent être naturelles ou synthétiques. Plus de 150 types de zéolithes ont été synthétisées et 48 zéolithes naturelles sont connues.
Les zéolithes naturelles se forment sur des terrains où les roches et les cendres volcaniques ont réagi avec les eaux souterraines alcalines et aussi dans les couches de dépôts organiques des bassins superficiels. Cette formation dure plusieurs centaines ou milliers d'années. Les zéolithes naturelles sont très rarement pures car elles sont généralement contaminées à divers degrés par d'autres minéraux métalliques, du quartz ou d'autres zéolithes. Pour cette raison, les zéolithes naturelles sont exclues de beaucoup d'applications industrielles où l'uniformité et la pureté sont essentielles. Des zéolithes ont même été trouvées sur Mars [1].
Les zéolithes synthétiques présentent l'avantage d'être très pures et de structure uniforme. Ces paramètres sont extrêmement importants pour certaines applications telle que les utilisations catalytiques en lit fluidisé (pour l’industrie pétrolière en particulier). Il est également possible de fabriquer des structures zéolitiques naturellement inconnues et qui permettent de maximiser l’efficacité de l’opération pour laquelle elle est destinée. L'activité de recherche sur la synthèse des zéolithes est importante et encouragée par la croissance du marché. Puisque les principales matières premières employées pour fabriquer les zéolithes sont la silice et l’alumine, qui sont parmi les composants minéraux les plus abondants sur terre, le potentiel de production des zéolithes synthétiques est pratiquement illimité.
Historique
La découverte des zéolithes
En 1756, le minéralogiste suédois Axel Frederik Cronstedt découvre la première zéolithe minérale, baptisée stilbite. Il reconnaît les zéolithes comme une nouvelle classe de minerais constitué d'alumino-silicates hydratés et de terres alcalines. Du fait de son caractère intumescent quand ce minéral est chauffé par une flamme de chalumeau, Cronstedt appelle ce minéral « zéolithe ». En 1840, Alexis Damour observe que les cristaux de zéolithes peuvent être déshydratés de façon réversible sans aucune modification apparente sur leur morphologie et leur transparence.
En 1845, Schafhautle rapporte la synthèse hydrothermale du quartz par chauffage d'un gel de silice avec de l'eau dans un autoclave. En 1850, Way et Thompson clarifient la nature de l'échange d'ions dans les terres. En 1858, Eichhorn démontre la réversibilité de l'échange d'ions dans les zéolithes. En 1862, S. C. Deville rapporte la première synthèse hydrothermale d'une zéolithe, la levynite.
En 1896, après avoir observé que des liquides variés tels que l'alcool, le benzène et le chloroforme ont été occlus dans les zéolithes, Friedel développe l'idée que la structure des zéolithes déshydratées est constituée d'une matrice spongieuse ouverte.
En 1909, Grandjean observe que la chabazite déshydratée adsorbe l'ammoniaque, l'air, l'hydrogène et d'autres molécules. En 1925, Weigel et Steinhoff rapportent le premier effet de « tamis moléculaire » et notent que les cristaux de chabazite déshydratées adsorbent rapidement l'eau, l'alcool méthylique, l'alcool éthylique et l'acide formique mais ni l'acétone, ni l'éther ni le benzène.
En 1927, Leonard décrit le premier usage des rayons X pour l'identification dans la synthèse minérale. Les premières structures des zéolithes sont déterminées en 1930 par Taylor et Pauling.
En 1932, McBain établit pour la première fois le terme « tamis moléculaire » pour définir les matières solides poreuses qui agissent comme des tamis à l'échelle moléculaire. Au milieu des années 1930, la littérature décrit les échanges d'ions, l'adsorption, les tamis moléculaires, les propriétés structurelles et minérales de zéolithes et relate la synthèse de nombreuses zéolithes. Barrer commence son travail de pionnier dans l'adsorption des zéolithes et leur synthèse. Il propose la première classification, basée sur des considérations de tailles moléculaires. En 1948, il rapporte la première synthèse complète d'une zéolithe analogue à la zéolithe naturelle mordenite.
Le développement industriel
Les zéolithes naturelles
Deux cents ans après leur découverte par Cronstedt en 1756, les zéolithes minérales (ou naturelles) sont considérées comme des constituants mineurs des roches basaltique et volcanique sans réelle application. À la fin des années 1950, les découvertes géologiques majeures révèlent l'ampleur des gisements de zéolithes naturelles dans les dépôts sédimentaires aux États-Unis d'Amérique. Ainsi, quelques zéolithes présentes en quantités importantes et très proches de dépôts minéraux d'importance commerciale, commencent à être commercialisées comme adsorbants. On exploite donc la chabazite, l'erionite, la mordenite et la clinoptilolite en quantité industrielle.
Le Japon devient le plus gros utilisateur des zéolithes naturelles. La mordenite et la clinoptilolite sont utilisées comme adsorbants dans les opérations de séparation, de déshydratation et de purification de l'air. Les zéolithes naturelles trouvent aussi des applications dans l'industrie papetière, dans les ciments et les bétons, dans les engrais et comme compléments alimentaire pour le bétail. Cette dernière application représente le plus gros débouché en volume pour les zéolithes naturelles.
Les zéolithes synthétiques
Les travaux de Barrer, dans le milieu des années 1940, poussent R.M. Milton à s'intéresser à l'étude de la synthèse de zéolithe et à la recherche de nouvelles techniques de séparation et de purification de l'air. Entre 1949 et 1954, R.M. Milton et D.W. Breck découvrent un nombre significatif de zéolithes commercialement intéressantes, les zéolithes A, X et Y. Ainsi, en 1954, Union Carbide commercialise pour la première fois des zéolithes synthétiques comme une nouvelle classe de matériel industriel servant à la séparation et à la purification. Les premières applications concernent donc la déshydratation des gaz réfrigérants et du gaz naturel.
En 1959, Union Carbide commercialise un procédé pour la séparation des isoparaffines basé sur l'utilisation de zéolithes : cela représente la première utilisation industrielle utilisant les caractéristiques de « tamis moléculaire » des zéolithes. La même année, Union Carbide commercialise une zéolithe de type Y comme catalyseur pour les réactions d'isomérisation, ce qui constitue la première utilisation industrielle utilisant les caractéristiques catalytiques des zéolithes.
En 1962, Mobil Oil introduit l'usage des zéolithes synthétiques de type X comme catalyseur dans les réactions de craquage de molécules (en particulier, valorisation des coupes lourdes des pétroles). Entre 1967 et 1969, Mobil Oil réalise la synthèse de zéolithes à haute teneur en silice et des zéolithes de type ZSM-5. En 1974, Henkel introduit les zéolithes A dans la fabrication des détergents comme remplaçants des phosphates qui sont soupçonnés d'être mauvais pour l'environnement. En 1977, l'industrie utilise largement les zéolithes : 22 000 tonnes de zéolithe Y sont usitées pour le craquage catalytique.
Utilisation
Usages industriels
Chimie
Les zéolithes sont employées comme :
- échangeur d'ions ;
- piège moléculaire : les molécules piégées peuvent ainsi être analysées séparément ;
- tamis moléculaire : seules les molécules de certaines tailles et formes peuvent passer à travers la structure zéolitique. On peut ainsi :
- assécher les solvants organiques ;
- assécher les gaz vecteurs des chromatographes ;
- protéger les appareils sensibles à l'humidité.
- catalyseurs.
- séparateur des gaz : par exemple, élimination de H2O, CO2 et SO2 des gisements de gaz naturel de basse qualité, mais aussi pour d'autres séparations comme celles des gaz nobles, de l’azote, du fréon et des formaldéhydes.
Récemment, une technique de déshydratation à basse ou moyenne température — entre -20 °C et 60 °C — nommée zéodratation a vu le jour : bien que peu consommateur d'énergie et écologique, ce procédé, qui s'apparente à la lyophilisation, est encore très peu répandu.
Construction
La zéolithe synthétique est employée comme additif dans le procédé de fabrication du mélange béton-asphalte. Le développement de cette application commencée en Europe (Allemagne) dans les années 1990 a connu un grand intérêt dans le monde entier. En effet, il permet de diminuer le niveau de température pendant la fabrication et la pose du béton-asphalte, ayant pour résultat une consommation inférieure de combustible fossile, et de ce fait libère moins de dioxyde de carbone, d'aérosols et de vapeurs nocives.
Thermorégulation
Les zéolithes peuvent être employés en tant que collecteurs thermiques solaires. Dans ces applications, leur grande chaleur d’adsorption, leur facilité d'hydratation et de déshydratation, et leur stabilité structurale sont exploitées. Cette propriété de forte hygroscopie est en effet couplée à une réaction exothermique inhérente au passage entre la forme déshydratée et la forme hydratée (chaleur d’adsorption), ce qui fait des zéolithes des collecteurs efficaces pour le stockage de l'énergie solaire par exemple.
Usage médical
Les systèmes de génération d'oxygène basés sur l’utilisation de zéolithe sont largement répandus pour produire de l'oxygène de qualité médicale. La zéolithe est utilisée comme tamis moléculaire qui extrait l'oxygène à partir de l'air, dans un processus qui absorbe l'azote atmosphérique.
Leur utilisation également est possible aussi pour l’amélioration de la coagulation des saignements graves. On retrouve des produits utilisant cette technologie sous le nom de QuikClot ou Hemosorb. Le fabricant affirme que le matériel granulé biologiquement inerte peut être versé directement sur la blessure pour arrêter le saignement intense presque instantanément[2].
Usages domestiques
Les zéolithes sont utilisées en tant qu'échangeur d'ions dans des applications domestiques telles que la purification ou l’adoucissement de l’eau.
La majeure partie des zéolithes synthétiques (zéolithe A) est réservée au marché des lessives. En 1992, ce marché s’élevait à 1,44 million de tonnes par an, soit environ un tiers du marché mondial.
Usages agricoles
Dans l'agriculture, la clinoptilolite (zéolithe naturelle) est employée pour la fertilisation des sols, car elle fournit une source du potassium (engrais) lentement libéré. Si elle est préalablement dopée avec de l'ammonium, la zéolithe permet aussi une libération contrôlée d'azote. Les récentes études Cubaines dans le domaine suggèrent que certaines cultures peuvent être cultivées sur des sols composés de zéolithe (ou d’un mélange zéolithe-terre) dans lesquels la zéolithe a été préalablement dopée ou enduite d'engrais et de micro-nutriments.
Substrat pour bonsaï
La zéolithe est également employée par les amateurs et professionnels du bonsaï (notamment la variété chabazite, également dénommée chabasai du fait d'une consonance plus "nipponne"). Son taux de rétention en eau (de l'ordre de 48%), associé à un drainage efficace et une bonne capacité d'échange cationique (capacité à fixer et redistribuer les éléments nutritifs) en font un substrat aux vertus nombreuses. De plus, la zéolithe reste stable dans le temps et ne se délite pas à l'image de l'akadama. La zéolithe pourrait bien à terme remplacer d'autres substrats importés du Japon et donc plus onéreux. Cependant, la zéolithe demeure difficile d'accès pour le simple particulier.
Quelques données économiques
Actuellement, la production annuelle mondiale de zéolithe naturelle est d’environ 4 millions de tonnes. La majorité de celle-ci, c'est-à-dire 2,6 millions de tonnes, est destinée au marché Chinois qui est employée principalement dans l'industrie des ciments. L'Europe de l'Est, l'Europe de l'Ouest, l'Australie, et l'Asie sont les principaux producteurs et fournissent la majeure partie des zéolithes naturelles du marché. Par comparaison, en 2004, l’Amérique du Nord produisait seulement 57 400 tonnes de zéolithe naturelle (source : U.S. Geological Survey, 2004) soit seulement environ 1,5% de la production mondiale.
Les différentes zéolithes naturelles
La famille des zéolithes naturelles inclut :
1) Famille des Analcimes :
- Analcime (Si-Al-Na hydraté)
- Pollucite (Si-Al-Cs-Na hydraté)
- Wairakite (Si-Al-Ca-Na hydraté)
- Bellbergite (Si-Al-K-Ba-Sr-Na hydraté)
- Bikitaite (Si-Al-Li hydraté)
- Boggsite (Si-Al-Ca-Na hydraté)
- Brewsterite (Si-Al-Sr-Ba-Na-Ca hydraté)
2) Famille des Chabazites :
- Chabazite (Si-Al-Ca hydraté)
- Willhendersonite (Si-Al-K-Ca hydraté)
- Cowlesite (Si-Al-Ca hydraté)
- Dachiardite (Si-Al-Ca-Na-K hydraté)
- Edingtonite (Si-Al-Ba-Ca hydraté)
- Epistilbite (Si-Al-Ca hydraté)
- Erionite (Si-Al-Na-K-Ca hydraté)
- Faujasite (Si-Al-Na-Ca-Mg hydraté)
- Ferrierite (Si-Al-Na-K-Mg-Ca hydraté)
- Herschelite (Si-Al-Na-K-Ca hydraté)
3) Famille des Gismondines :
- Amicite (Si-Al-K-Na hydraté)
- Garronite (Si-Al-Ca hydraté)
- Gismondine (Si-Al-Ba-Ca hydraté)
- Gobbinsite (Si-Al-Na-K-Ca hydraté)
- Gmelinite (Si-Al-Na-Ca hydraté)
- Gonnardite (Si-Al-Na-Ca hydraté)
- Goosecreekite (Si-Al-Ca hydraté)
4) Famille des Harmotomes :
5) Famille des Heulandites :
- Clinoptilolite (Si-Al-Na-K-Ca hydraté)
- Heulandite (Si-Al-Na-Ca hydraté)
- Laumontite (Si-Al-Ca hydraté)
- Levyne (Si-Al-Ca-Na-K hydraté)
- Mazzite (Si-Al-K-Na-Mg-Ca hydraté)
- Merlinoite (Si-Al-K-Na-Ca-Ba hydraté)
- Montesommaite (Si-Al-K-Na hydraté)
- Mordenite (Si-Al-Na-K-Ca hydraté)
- Maricopaite (Si-Al-plomb-Ca hydraté)
6) Famille des Natrolites :- Mesolite (Si-Al-Na-Ca hydraté)
- Natrolite (Si-Al-Na hydraté)
- Scolecite (Si-Al-Ca hydraté)
- Offretite (Si-Al-Ca-K-Mg hydraté)
- Paranatrolite (Si-Al-Na hydraté)
- Paulingite (Si-Al-K-Ca-Na-Ba hydraté)
- Perlialite (Si-Al-K-Na-Ca-Sr hydraté)
7) Famille des Stilbites :
- Barrerite (Si-Al-Na-K-Ca hydraté)
- Stilbite (Si-Al-Na-Ca hydraté)
- Stellerite (Si-Al-Ca hydraté)
- Thomsonite (Si-Al-Na-Ca hydraté)
- Tschernichite (Si-Al-Ca hydraté)
- Yugawaralite (Si-Al-Ca hydraté)
8) Non déterminé :
- Dachiardite de sodium
- Tétranatrolite
Voir aussi
Articles connexes
- Silice, silicates
- Cancer, cancérologie, mésothéliome
- Toxicologie, écotoxicologie
- Géologie, silicates
Liens externes
Bibliographie
Notes et références
- ↑ Claire I., Fialips et al., Icarus, volume 178, 1st nov. 2005, pages 74-83
- ↑ Saved by 'sand' poured into the wounds - health - 16 March 2006 - New Scientist
Voir aussi
- Portail de la chimie
- Portail des minéraux et roches
Catégories : Silicate (minéral) | Tectosilicate
Wikimedia Foundation. 2010.