- Méthionine
-
Méthionine 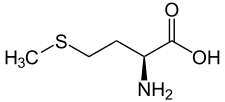
L ou S-méthionine
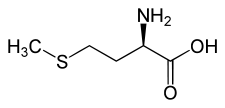
D ou R-méthionineGénéral Nom IUPAC acide 2-amino-4-(méthylsulfanyl)butanoïque Synonymes M, Met, acide 2-amino-3-mercapto-propionique No CAS (L) ou S
(D) ou R
(racémique)No EINECS (L)
(D)
(DL)Code ATC AB26 SMILES InChI Propriétés chimiques Formule brute C5H11NO2S [Isomères] Masse molaire[1] 149,211 ± 0,011 g·mol-1
C 40,25 %, H 7,43 %, N 9,39 %, O 21,45 %, S 21,49 %,pKa 2,28
9,21Propriétés biochimiques Codons AUG pH isoélectrique 5,74 Acide aminé essentiel Oui Occurrence dans les protéines humaines 2,3 % Unités du SI & CNTP, sauf indication contraire. La méthionine est un acide-α-aminé soufré non polaire, son atome de soufre participant à une fonction thioéther (-S-CH3). C'est l'un des huit acides aminés essentiels. Dans le code génétique, la méthionine est spécifiée par le codon ATG sur l'ADN et par le codon AUG sur l'ARN. Elle joue un rôle critique dans la reproduction, la survie cellulaire, la méthylation des protéines et de l'ADN.
Sommaire
Rôles biologiques
La méthionine joue un rôle particulier dans la biosynthèse des protéines, puisque toutes les chaînes protéiques démarrent par l'incorporation d'une méthionine en position N-terminale. D'autres résidus méthionine peuvent ensuite être incorporés de manière interne à la chaîne polypetidique. La première méthionine des protéines n'est pas toujours retrouvée dans les protéines terminées. Elle est en effet fréquemment clivée par une enzyme spécifique appelée méthionine aminopeptidase.
La méthionine est aussi une transméthylase, elle a la capacité de transférer le groupement méthyle lié au soufre. Par ailleurs la rupture de cette liaison dégage une grande quantité d'énergie.
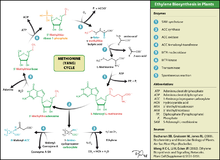
Cet acide aminé est aussi utilisé par les plantes pour synthétiser l'éthylène. Ce processus est connu sous le nom de Cycle de Yang ou cycle de la méthionine.
Egalement, elle est utilisée comme antidote au paracétamol : 100 mg de méthionine pour 500 mg de paracétamol
Dérivés de la méthionine
La méthionine est le précurseur de la S-adénosylméthionine ou SAM, un métabolite essentiel des réactions de transfert de méthyle dans la cellule. La SAM est une forme activée de la méthionine où le méthyle du thioéther devient un groupement partant utilisé pour méthyler l'ADN, l'ARN ou les protéines.
Le soufre de la méthionine est sensible à l'oxydation qui donne lieu à deux dérivés: la méthionine sulfone et la méthionine sulfoxyde
Formation et rôle de la vitamine B12
La vitamine B12 agit en tant que co-enzyme dans la synthèse de méthionine. En effet, c'est sous la forme de l'enzyme méthyl B12 qu'un groupement méthyl est ajouté à l'homocystéine pour former la méthionine. Le donneur de méthyl se trouve à être le méthyl tétrahydrofolate (méthyl THF).
On remarque donc l'importance de la vitamine B12 à la formation de l'ADN. Voilà pourquoi une déficience en vitamine B12 peut entraîner des désordres importants, comme l'anémie de type mégaloblastique[2].
Sources alimentaires
Légumineuses, œufs, poissons, ail, lentilles, viandes, oignons, soja, yogourt, parmesan et gruyère. la méthionine est très utilisée dans l'alimentation animale, et la recherche en biotechnologiess tente de trouver des moyens de la produire autrement qu'avec du pétrole[3], avec un soutien financier et stratégique de l'Europe[4] et non sans susciter des craintes en matière d'éthique environnementale[5], en raison des risques[6] lié aux biotechnologies et d'une demande sociale inexistante, voire opposée à l'artificialisation de la production de nourriture[7],[8].
Producteurs
L'un des premiers producteurs (forme liquide ; Methionine Hydroxy Analog qui peut agir sur la lactation, et forme poudre) est Adisseo, dont l'histoire commence à Commentry (en France) en 1939 avec une société « Alimentation Equilibrée », productrice d’additifs pour l'alimentation du bétail, créée par un polytechnicien (Marcel Lingot), dont méthionine et vitamine A. L'entreprise a été rachetée en 1971 par Rhône-Poulenc (devenant la « Division Animale » du groupe, qui ajoute à ses 3 usines européennes, dans les années 1980, une usine aux États-Unis. Adisseo devient autonome en 2002, avec un pôle recherche à Commentry (Centre d’Expertise et de Recherche en Nutrition).
En 2006, le groupe chinois BlueStar (Chimie) achète Adisseo et crée CINAbio (centre de R&D en biotechnologies) à Toulouse. Une nouvelle usine est prévue en Chine. En 2011 Adisseo/BlueStar dispose d'environ 1200 employés dans le monde[9].
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Essential Haematology, A.V. Hoffbrand, P.A.H. Moss and J.E. Pettit, 5th edition, Blackwell publishing
- Gouvernement français, 2011 Investissements d'avenir - Biotechnologies et bioressources - PROJET SYNTHACS Ce projet propose une alternative à l’utilisation de la pétrochimie pour produire, à partir de biomasse renouvelable, la méthionine, l’un des composants essentiels de l’alimentation animale.
- EUROPE - DG RECHERCHE - Biotechnologies, Agriculture and Food -2009< 19th Meeting of the EC-US Task Force on Biotechnology ResearchAu sommaire : The importance of Synthetic Biology activities in a EuropeanBiotechnology Programme
- CONFEDERATION SUISSE Biologie synthétique - Biologie synthétique : réflexions éthiques, Rapport de la CENH Mai 2010
- EUROPE - DG ENVIRONNEMENT >- Synthetic biology ethics: managing risks without limiting benefits, Mars 2011]
- BBSRC New report reveals public’s views on synthetic biology, 14/06/2010
- VIVAGOVEILLE Au sommaire : Ne pas ouvrir la boîte de Pandore de la biologie synthétique, Juin 2010
- Source : Page sur l'histoire du groupe Adisseo, par lui-même, consultée 2011-07-12
Lien externe
Wikimedia Foundation. 2010.