- Acide carboxylique
-
Le terme acide carboxylique désigne une molécule comprenant un groupement carboxyle (–C(O)OH) . Ce sont des acides et leurs bases conjuguées sont appelées carboxylates.
En chimie organique, un groupe carboxyle est un groupe fonctionnel composé d'un atome de carbone, lié par une double liaison à un atome d'oxygène et lié par une liaison simple à un groupe hydroxyle.
Sommaire
Généralités
En chimie, les acides carboxyliques R-COOH constituent avec les acides sulfoniques R-SO3H les deux types d'acides de la chimie organique. On les trouve de manière abondante dans la nature, sous la forme d'acide gras (lipide) et ils sont très importants en chimie industrielle. Par exemple, l'acide acétique est non seulement une brique importante pour les molécules complexes que l'on trouve en biologie, mais est aussi une molécule produite industriellement et qu'on retrouve dans le vinaigre. Un des plus connus est l'acide acétylsalicylique ou aspirine. La brique de base des protéines, les acides aminés sont des acides carboxyliques.
Le groupe fonctionnel caractéristique est le groupe carboxyle, où R est un hydrogène ou un groupe organique :
Les acides carboxyliques ont pour formule brute CnH2nO2 lorsque le R est un groupe alkyle. Le calcul du nombre d'insaturation donne :
 . Cette insaturation traduit la liaison double carbone-oxygène.
. Cette insaturation traduit la liaison double carbone-oxygène.On écrit souvent les groupements carboxyles sous la forme réduite : -COOH (forme non ionisée du groupement). La forme ionisée du groupement est : -COO-.
Celui-ci est toujours situé en fin de chaîne carbonée. L'ajout d'un groupement carboxyle à un composé organique est une carboxylation, l'élimination de ce même groupement est une décarboxylation.
Ions carboxylates
Ce sont les bases conjuguées des acides carboxyliques. Ces bases sont en général plutôt faibles. La charge négative sur la molécule est délocalisée sur les deux atomes d'oxygène du groupe carboxyle par mésomérie, ce qui explique la stabilité relative de ce type de molécules.
Nomenclature
- Systématique : si l'atome de carbone du groupe carboxyle COOH est inclus dans la chaîne principale de l'hydrocarbure correspondant (ayant le même nombre d'atomes de carbone, avec CH3 à la place de COOH) on fait suivre le nom de cet hydrocarbure du suffixe « -oïque » (dioïque pour un diacide), et en le faisant précéder du mot « acide ». Dans le cas contraire (en série cyclique par exemple), on fait suivre le mot « acide » du nom de l'hydrocarbure auquel on ajoute le suffixe « -carboxylique ».
-
Classe Formule*
du groupe caractéristiqueSuffixe Acides carboxyliques -(C)OOH
-COOHacide …-oïque
acide …-carboxylique
- (*) L'atome de carbone indiqué entre parenthèses est inclus dans le nom de la structure fondamentale et non dans le suffixe[1].
- Exemples :
- L'acide heptanoïque CH3(CH2)5-COOH peut alternativement être nommé acide hexane-1-carboxylique si l'atome de carbone du -COOH n'est pas inclus dans la numérotation de la chaîne[2].
- Acide cyclopentanecarboxylique :
 -COOH
-COOH
- Usuelle : comme de nombreux composés organiques, les acides carboxyliques ont des noms usuels fréquemment utilisés dans la littérature et rappelant la source depuis laquelle ils furent d'abord isolés. Toutefois une liste définie par l'IUPAC règle l'usage des noms triviaux acceptés aux côtés des noms systématiques[3].
Nom et source de quelques acides carboxyliques Type Structure Nom IUPAC nom commun Source Monoacides aliphatiques H-COOH acide méthanoïque acide formique sécrété par certaines fourmis (latin : formica, fourmis) CH3-COOH acide éthanoïque acide acétique latin : acetum, vinaigre CH3CH2-COOH acide propanoïque acide propionique grec : pion, gras CH3(CH2)2-COOH acide butanoïque acide butyrique grec : bouturos, beurre CH3(CH2)3-COOH acide pentanoïque acide valérique valériane CH3(CH2)4-COOH acide hexanoïque acide caproïque CH3(CH2)5-COOH acide heptanoïque acide énanthique CH3(CH2)6-COOH acide octanoïque acide caprylique noix de coco, lait maternel CH3(CH2)7-COOH acide nonanoïque acide pélargonique CH3(CH2)8-COOH acide décanoïque acide caprique CH3(CH2)9-COOH acide undécanoïque acide undécylique CH3(CH2)10-COOH acide dodécanoïque acide laurique huile de noix de coco CH3(CH2)11-COOH acide tridécanoïque acide tridécylique CH3(CH2)12-COOH acide tétradécanoïque acide myristique CH3(CH2)13-COOH acide pentadécanoïque acide pentadécylique CH3(CH2)14-COOH acide hexadécanoïque acide palmitique huile de palme CH3(CH2)15-COOH acide heptadécanoïque acide margarique CH3(CH2)16-COOH acide octodécanoïque acide stéarique graisses animales CH3(CH2)17-COOH acide nonadécanoïque acide nonadécylique CH3(CH2)18-COOH acide éicosanoïque acide arachidique huile d'arachide, les huiles de poisson et les huiles végétales CH3(CH2)20-COOH acide docosanoïque acide béhénique Monoacides aromatiques C6H5-COOH acide benzoïque benzène HO-C6H4-COOH acide 2-hydroxybenzoïque acide salicylique fruits (sous forme de salicylate de méthyle) Diacides aliphatiques HOOC-COOH acide éthanedioïque acide oxalique présent dans beaucoup d'aliments comme l'oseille (latin : oxalis) ou les épinards HOOC-CH2-COOH acide 1,3-propanedioïque acide malonique HOOC-CH2-CH2-COOH acide 1,4-butanedioïque acide succinique HOOC-CH2-CH2-CH2-COOH acide 1,5-pentanedioïque acide glutarique HOOC-(CH2)4-COOH acide 1,6-hexanedioïque acide adipique monomère du nylon HOOC-(CH2)5-COOH acide 1,7-heptanedioïque acide pimélique HOOC-(CH2)6-COOH acide 1,8-octanedioïque acide subérique HOOC-(CH2)7-COOH acide 1,9-nonanedioïque acide azélaïque HOOC-(CH2)8-COOH acide 1,10-décanedioïque acide sébacique HOOC-(CH2)9-COOH acide 1,11-undecanedioïque HOOC-(CH2)10-COOH acide 1,12-dodécanedioïque Diacides aromatiques C6H4(COOH)2 acide phtalique C6H4(COOH)2 benzène-1,3-dicarboxylique acide isophtalique C6H4(COOH)2 acide benzène-1,4-dicarboxylique ou acide paraphtalique acide téréphtalique Acides alpha hydroxylés CH2(OH)-COOH acide hydroxyacétique acide glycolique canne à sucre, betteraves, raisin CH3CH(OH)-COOH acide 2-hydroxypropanoïque acide lactique latin : lac, lactis, lait HOOC-CH2-CH(OH)-COOH acide 2-hydroxy-1,4-butanedioïque acide malique pomme (latin : malus) HOOC-CH(OH)-CH(OH)-COOH acide 2,3-dihydroxybutanedioïque acide tartrique vin HOOC-CH2-(COOH)C(OH)-CH2-COOH acide 2-hydroxypropane-1,2,3-tricarboxylique acide citrique citron Acides thiols CH3CH(SH)-COOH acide 2-mercaptopropanoïque acide thiolactique NB : un moyen mnémotechnique pour se souvenir des noms des diacides linéaires, dans l'ordre croissant du nombre de carbones, est la phrase suivante : « On Mange Saucisse Grillée A Point » (Oxalique, Malonique, Succinique, Glutarique, Adipique, Pimélique). Les diacides sont utilisés pour la synthèse de polyamides et de polyesters.
D'autres types d'acides carboxyliques peuvent être cités : les cétoacides, les acides aminés et les acides gras.
Propriétés physiques et structurelles
État
Les acides carboxyliques sont liquides dans les conditions normales tant que leur chaine carbonée présente moins de 8 atomes de carbone. Ils sont solides au-delà.
Les acides de faible masse molaire possèdent une forte odeur ; par exemple l'acide butanoïque est responsable de l'odeur du beurre rance.
Polarité, solubilité
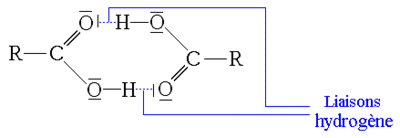
La fonction acide carboxylique est fortement polaire et est à la fois donneur et accepteur de liaisons hydrogène. Ceci permet la création de liaisons hydrogène par exemple avec un solvant polaire comme l'eau, l'alcool, et d'autres acides carboxyliques.
De par cette propriété les acides carboxyliques de petite taille (jusqu'à l'acide butanoïque) sont complètement solubles dans l'eau. Les molécules d'acides sont aussi capables de former des dimères stables par pont hydrogène, ce qui permet d'expliquer pourquoi leur température d'ébullition est plus élevée que celle des alcools correspondants.
Acidité
En solution dans l'eau, l'acide se dissocie partiellement en ion carboxylate, selon l'équation-bilan :
.
Ce sont des acides faibles dans l'eau (pKA entre 4 et 5).
Comme les alcools, les acides carboxyliques montrent un caractère acide et basique : la déprotonation en ions carboxylates est facile, mais la protonation est plus difficile. Ils possèdent donc un pKA plus faible que celui des alcools. En fait l'acidité des acides carboxyliques s'explique par l'effet inductif dans le groupement carboxyle : la liaison C=O est très polarisée (électronégativité de l'oxygène supérieure à celle du carbone) ce qui fait que le carbone est électrophile, et il attire donc les électrons de l'autre oxygène. Or cet autre oxygène est lui-même lié à un hydrogène, et cette liaison est aussi polarisée, donc l'électron de l'hydrogène qui s'est rapproché de l'oxygène est attiré à son tour par le carbone électrophile. Cet hydrogène devient donc très facilement mobile, d'où l'acidité du groupement carboxyle.
La solubilité de l'acide carboxylique croit avec le pH.
Spectroscopie
En infrarouge (IR), l'acide carboxylique présente 2 bandes de valence :
Vibration C=0 O-H Nombre d'onde (cm-1) 1 680-1 710 2 500-3 200 Intensité (forte) large, moyenne à forte Structure

D'après la théorie VSEPR :
- la géométrie autour de l'atome de carbone (liaisons) est de type trigonale ;
- la géométrie autour de l'atome d'oxygène de la fonction carbonyle (liaison double + doublets libres) est aussi de type trigonale ;
- la géométrie autour de l'atome d'oxygène de la fonction hydroxyle (liaisons + doublets libres) est de type tétraédrique (AX2E2).
L'acide carboxylique possède plusieurs formes mésomères.
Réactivité
Comme le montre, entre autres, les différentes formules mésomères de l'acide carboxylique :
- les atomes d'oxygène sont des sites nucléophiles ainsi que des bases de Lewis ;
- le carbone central est électrophile ;
- l'atome d'hydrogène électrophile est acide.
Dérivés
Les acides carboxyliques comptent de nombreux dérivés :
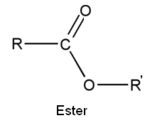
- les esters
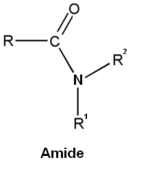
- les amides
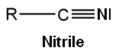
- les nitriles
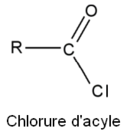
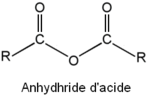
En termes de groupe partant (nucléofuge), l'ordre de facilité est :
Cl- (chlorure d'acyle), RCOO- (anhydride), RO- (ester), -NH2 et -NR1R2 (amides).
Réduction
Oxydation
- Dioxyde de carbone (CO2)
Synthèse
Synthèse par oxydation
- Des alcools ou des aldéhydes
Les acides carboxyliques peuvent être obtenus par oxydation des aldéhydes, donc en fait d'une double oxydation des alcools primaires.


- Des alcènes

exemple : synthèse de l'acide acétique par oxydation du propène

Synthèse à partir d'un dérivé d'acide
Il s'agit simplement des hydrolyses des différents dérivés d'acides.
- ester
- - hydrolyse en milieu acide : rétroestérification.
- - hydrolyse en milieu basique : saponification de l'ester.
 puis
puis 
- nitrile
Synthèse par réaction d'un organomagnésien sur le dioxyde de carbone
Articles connexes : organomagnésien et dioxyde de carbone.Réaction
Conditions
La synthèse a lieu à basse température (-40 °C). Le dioxyde de carbone est alors sous forme solide, dite carboglace. Il est mis en excès. Après réaction, on effectue une hydrolyse en milieu acide pour obtenir l'acide carboxylique.
Mécanisme
- Première étape : addition de l'organomagnésien sur CO2
- Deuxième étape : hydrolyse en milieu acide
Synthèse malonique
Article détaillé : Synthèse malonique.La synthèse malonique est un ensemble de réactions permettant de synthétiser de nombreux acides carboxyliques primaires ou secondaires à partir du malonate de diéthyle.
Elle est composée :
- d'une réaction acide-base entre le malonate de diéthyle et de l'éthanoate (de sodium, de potassium, ...) ;
- d'une substitution nucléophile, où l'on insère le groupe (primaire ou secondaire) voulu pour l'acide carboxylique final ;
- d'une double saponification des deux fonctions ester du malonate de diéthyle subsititué, suivie d'une acidification du milieu ;
- d'une décarboxylation (dégagement de dioxyde de carbone par chauffage) ;
- d'un réarrangement du produit final en acide carboxylique par tautomérie.
Cette synthèse est d'autant plus intéressante qu'a priori, elle permet de synthétiser n'importe quel acide carboxylique, puisque, à part un groupe tertiaire, il semble qu'on puisse mettre ce qu'on veut à la place de R.
Notes et références
- R. Panico, J.-C. Richer - Nomenclature UICPA des composés organiques - Masson 1994, pp. 70, 118 et suivantes (ISBN 978-2-225-84479-9). Un tableau des suffixes (et préfixes) utilisés pour désigner quelques groupes caractéristiques importants en nomenclature substitutive est consultable dans une référence IUPAC en ligne (en anglais) : Suffixes and prefixes for some important characteristic groups in substitutive nomenclature.
- Robert Panico,Jean-Claude Richer, Jean Rigaudy - Nomenclature et terminologie en chimie organique - Classes fonctionnelles. Stéréochimie - Techniques de l'Ingénieur 1996, p. 20 (ISBN 2 85 059-001-0)
- http://www.acdlabs.com/iupac/nomenclature/93/r93_705.htm
Voir aussi
Liens externes
Wikimedia Foundation. 2010.