- Aspartam
-
Aspartame
Aspartame 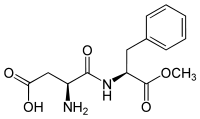
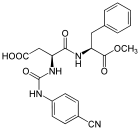
Ester méthylique de l'aspartyl-phénylalanine Général Nom IUPAC (3S)-3-amino-4-[[(1S)-1-benzyl-2-(méthoxy-2-oxoéthyl]amino]-4-oxobutanoïque Synonymes - Ester N-méthylique de N-L-α-aspartyl-L-phénylalanine
- Ester N-méthylique de l'acide 3-amino-N-(α-carbométhoxy-éthoxyphényl) succinamique
- Aspartylphénylalanate de méthyle
- Ester méthylique d'aspartyl-phénylalanine
No CAS No EINECS DrugBank PubChem No E E951 SMILES InChI Apparence Poudre cristalline blanche, légèrement hygroscopique[1] Propriétés chimiques Formule brute C14H18N2O5 [Isomères] Masse molaire 294,3031 g∙mol-1
C 57,14 %, H 6,16 %, N 9,52 %, O 27,18 %,pKa 3,1 & 7,9 (25 °C)[2] Propriétés physiques T° fusion Décomposition avant fusion. Le produit de la décomposition fond à 246 °C[2] T° ébullition >300 °C à 1 013,25 hPa[2] Solubilité Peu soluble dans l'eau (10 g/l à 20 °C[2]) et l'éthanol[3]. Masse volumique 150–600 kg⋅m-3, solide[2] Précautions Directive 67/548/EEC Phrases S : 22, 24/25, NFPA 704 Écotoxicologie DL50 >4 g⋅kg-1 (Rats, oral)[4]
>10 g⋅kg-1 (Souris, oral)[4]Composés apparentés Isomère(s) Musc cétone Autres composés Alitame, Néotame, Suosan Unités du SI & CNTP, sauf indication contraire. L'aspartame est un édulcorant artificiel découvert en 1965. C'est un dipeptide composé de deux acides aminés naturels, l'acide L-aspartique et la L-phénylalanine, le dernier étant estérifiée par un alcool, le méthanol.
L'aspartame a un pouvoir sucrant environ 200 fois supérieur à celui du saccharose et est utilisé pour édulcorer les boissons et aliments à faible calorie ainsi que les médicaments. Cet additif alimentaire est utilisé dans un grand nombre de produits et autorisé dans de nombreux pays, il est référencé dans l'Union européenne par le code E951.
Depuis sa première autorisation de mise sur le marché aux États-Unis, par la Food and Drug Administration (FDA) en 1974, l'aspartame a fait l'objet de polémiques sur ses possibles effets nocifs sur la santé. Les organismes de santé publique (FDA, EFSA...) confirment son innocuité dans les doses d'utilisation autorisées chez l'Homme.
Sommaire
Historique
La première apparition de l'aspartame date de la publication de sa synthèse en 1966[5]. Mais il aurait été découvert en 1965 par J. Schlatter, chimiste de la société G. D. Searle & Company, lors de la synthèse d'un tétrapeptide devant être testé comme médicament anti-ulcères[6],[7],[8]. L'aspartame était alors un intermédiaire de synthèse et Schlatter aurait goûté le produit tombé sur son doigt. Le goût sucré fut une découverte inattendue, l'acide aspartique et la phénylalanine n'étant pas sucrés. Le dipeptide non méthylé se révéla avoir une saveur amère. Schlatter synthétisa des composés de structure voisine, mais le produit original fut conservé et commercialisé sous le nom d'aspartame.
Une première autorisation de mise sur le marché fut accordée à l'aspartame par la FDA (États-Unis) en juillet 1974[9]. Cette autorisation fut l'objet d'une polémique, car Donald Rumsfeld, qui était alors secrétaire général de la Maison Blanche, devint ensuite directeur général de G. D. Searle & Company, qui fabrique et vend l'aspartame sous le nom de NutraSweet.
Suite à de possibles effets toxiques et cancérogènes sur le cerveau par l'aspartame ou ses métabolites, l'autorisation fut suspendue quelques mois plus tard par la FDA en décembre 1974[9]. Son usage fut rétabli en 1981 aux États-Unis[10] dans les aliments solides, puis dans les liquides en 1983. En 1981, l'aspartame est autorisé par un comité commun d'experts de l'OMS et de l'Organisation pour l'agriculture et la nourriture[11]. La même année, le comité scientifique pour les aliments humains (CSAH / SCF en anglais) de la commission européenne approuve l'aspartame.
En 1985, Monsanto fit l'acquisition de GD Searle et sépara Searle Pharmaceuticals et The NutraSweet Company en filiales distinctes[9].
L'aspartame est autorisé en France en 1988 et est codé E951 dans la classification européenne des additifs alimentaires[12].
Le brevet de l'aspartame tomba dans le domaine public en 1992.
En 1994, son emploi en tant qu'édulcorant est harmonisé par l'Union européenne (directive 94/35/CE[13]). L'aspartame est alors approuvé dans plus de 90 pays.
En 1995, l'Union européenne établit les critères de pureté pour l'aspartame (directive 95/31/CE[14]).
En 2002, le comité scientifique de la Commission européenne confirme son avis sur l'innocuité de l'aspartame. La même année, l'Agence française de sécurité sanitaire (AFSSA) conclut dans un rapport : « La consommation d'aspartame chez l'homme, même dans des populations particulièrement exposées comme les enfants diabétiques, ne dépasse pas la dose journalière acceptable (DJA), notamment en France ».
En 2003, la directive 2003/115/CE autorise un nouvel édulcorant intense dérivé de l'aspartame : le sel d'aspartame-acésulfame dont l'innocuité a été établie par le comité scientifique de l'alimentation humaine dès mars 2000[15] et les critères de puretés définie en 2001.
Structure et propriétés
Structure
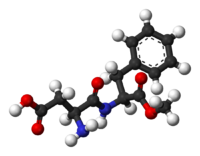
L'aspartame est un dipeptide, formé par deux acides aminés, l'acide L-aspartique et un méthyle ester de L-phénylalanine. Son nom chimique est donc L-Aspartyl-L-phenylalanine méthylester.
Propriétés chimiques
L'aspartame possède une base aminée et un groupement acide lui confèrant deux constantes d'équilibres, 3,1 & 7,9 (25 °C)[2].
Hydrolyse
Comme la plupart des peptides, l'aspartame s'hydrolyse en acides aminés à chaud et en milieu acide (pH faible). L'aspartame est plus instable en milieu neutre qu'en milieu acide (à faible pH). À température ambiante il est le plus stable à pH 4,3, avec une demi-vie de 300 jours. Cependant, à pH 7, sa demi-vie n'est que de quelques jours. L'aspartame est instable à haute température : en phase solide, la recombinaison en dicétopipérazine peut avoir lieu à partir de 105 °C. C'est la raison pour laquelle il est déconseillé de « cuisiner » l'aspartame.
L'hydrolyse du groupement estérifé de l'aspartame produit du méthanol (10 % en masse) et de l'aspartyl-phénylalanine. Ce dernier peut se recombiner en dicétopipérazine (acide 2-(5-benzyl-3,6-dioxopipérazin-2-yl)acétique) (à partir de 30 °C[1]) ou bien s'hydrolyser en ces deux acides aminés de base l'acide aspartique (40 % en masse) et la phénylalanine (50 % en masse).
Réaction de Maillard
La fonction amine de l'aspartame peut participer aux réactions de Maillard avec les groupes aldéhydes.
Propriétés physiques
L'aspartame est un solide cristallin blanc, inodore et légèrement hygroscopique. Il est faiblement soluble dans l'eau (10 g/l eau à 20 °C[2]) et l'éthanol[3]. Il se solubilise plus vite dans les solutions acides.
Biochimie
L'aspartame, contrairement au sucre, ne peut servir à la formation de graisses dans les tissus adipeux ni aux autres rôles métabolique utile de celui-ci[16].
Propriétés sucrantes
L'aspartame a un pouvoir sucrant environ 200 fois supérieur à celui du saccharose (à poids égal)[3].
À la différence de la saccharine et de l'acésulfame-K, l'aspartame n'a pas de composante ou d'arrière-goût amer. Dans les études en aveugle toutefois, les boissons sucrées au saccharose ressortent comme « plus agréables »[réf. nécessaire].
L'aspartame est souvent utilisé en mélange avec d'autre édulcorant intense (acésulfame-K) pour pallier la diminution de la saveur sucrée. La diminution est due à sa décomposition en milieu aqueux ou à sa disparition lors des réactions de Maillard entre celui-ci et les arômes possédant une fonction aldéhyde.
Un dérivé de l'aspartame, le superaspartame a un pouvoir sucrant de 8 000 à 140 000 fois supérieur à celui du saccharose.
Utilisation
L’aspartame avec l'acésulfame K est un des édulcorants intenses le plus fréquemment employés, il est utilisé dans près de 5 000 produits à travers le monde (les gommes sans sucre, les boissons allégées et autres gâteaux du même type) et de plus de 600 spécialités pharmaceutiques, dont plus de 2 000 vendues en Europe. Sa consommation est surtout motivée par le fait qu'il n'apporte que très peu de calories car il suffit de 200 fois moins que le sucre pour obtenir la même sensation sucrée. L'aspartame a aussi les avantages de ne pas favoriser les caries et d'être un édulcorant pas cher.
L’aspartame est utilisé sous forme de sucrettes ou de poudre blanche (en sachet ou boîte) pouvant se substituer au sucre, dans le café ou le thé, pâtisseries ou autres. Ces produits contiennent, en moyenne 3 % d’aspartame, les autres ingrédients étant de la maltodextrine et de l’acésulfame K.
Réglementation
Le codex alimentarius reconnaît l'utilisation de l'aspartame comme édulcorant et exhausteur de goût dans une large gamme de produits alimentaires, à des concentrations maximales variant de 0,6 g à 3 g suivant l'application[17].
En Europe, l'aspartame est autorisé dans[13] :
- les boissons non alcoolisées (0,6 g⋅l-1)
- les desserts et produits similaires (0,6-1 g⋅kg-1)
- les confiseries (0,5-1 g⋅kg-1)
- les boissons alcoolisées (bières) (0,6 g⋅l-1)
- les compléments alimentaires et autres
Santé
L'aspartame fait partie des additifs alimentaires les plus étudiés[18],[19], il est reconnu sûr pour la consommation humaine dans plus de 90 pays[20], notamment par les agences de sécurité sanitaire comme l'Autorité européenne de sécurité des aliments[21], le JECFA de l'OMS/FAO et la Food and Drug Administration.
Diabète
On a formulé l'hypothèse que la saveur sucrée puisse provoquer une sécrétion d'insuline commandée par le cerveau (cephalic-phase insulin release, ou CPIR). Selon cette hypothèse, cette sécrétion d'insuline sans apport de glucose pourrait provoquer une chute de la glycémie ce qui provoquerait une sensation de faim. Les édulcorants utilisés par les personnes obèses pour perdre du poids auraient eu un effet inverse à celui recherché[réf. nécessaire]. Néanmoins, aucune étude n'a mis en évidence ce phénomène. Cette hypothèse est donc à rejeter. [22],[23].
En 2000, une étude de la modification éventuelle de la thermogenèse apportée par une alimentation édulcorée à l'aspartame en comparaison avec une alimentation sucrée au saccharose n'a mis en évidence aucune différence significative[24].
Selon le ministère de la santé du Canada, l'utilisation de l'aspartame est sans danger pour les diabétiques[20].
Métabolisme
Lors de la digestion, l'aspartame perd son groupement hydroxyméthyl (méthanol), puis se décompose en ses deux acides aminés de base, l'acide aspartique et la phénylalanine. Sous l'effet de la chaleur, il peut aussi se recombiner pour former de la dicétopipérazine. En comparaison avec les aliments courants, l'aspartame est une source mineure de phénylalanine, d'acide aspartique et de méthanol.
Phénylalanine
La phénylalanine est un des huit acide aminé essentiel, elle est notamment naturellement présente dans le lait des mammifères. Seuls les personnes soufrant de phénylcétonurie (PKU), une maladie génétique rare (1/16 000 naissances) doivent contrôler de façon très stricte l'apport en phénylalanine, c'est pourquoi les produits contenant de l'aspartame doivent renseigner qu’ils contiennent une source de phénylalanine[25].
Méthanol
Le méthanol est un alcool présent dans les aliments fermentés (vin, bière ...), fruits mûrs et jus de fruits. Le méthanol est dangereux pour l'homme à trop forte concentration mais dès sa formation, il est immédiatement rejeté par l'organisme par la respiration, et par exemple, un jus de tomate apporte six fois plus de méthanol qu'un soda contenant de l'aspartame (Cependant, dans les produits naturels, la présence simultanée d'éthanol et de pectine empêche cette dégradation toxique du méthanol[26])
Acide aspartique
L'acide aspartique est un acide aminé, non toxique pour l'organisme qui ne pose pas de problème lors de la métabolisation de l’aspartame. C'est un constituant courant des protéines de l’organisme.
Dicétopipérazine
La dicétopipérazine n’est pas considérée comme génotoxique (provoquant l'apparition de lésions dans l'ADN, qui peuvent éventuellement conduire à des mutations) ni cancérogène chez le rat et la souris. La dose journalière acceptable de la dicétopipérazine pour l'homme a été fixée à 7,5 mg/kg/jour.
Polémiques
Depuis sa mise sur le marché, il y a eu des polémiques sur l'innocuité de l'aspartame, alimentées par des accusations de conflits d'intérêts, certaines publications scientifiques, des théories du complot et des canular informatiques.
En juillet 2005, des chercheurs de la Fondation Européenne Ramazzini, à Bologne (Italie), ont présenté à la presse une étude menée sur des rats montrant un effet cancérogène au niveau du cerveau[27]. Cette étude a été critiquée par des agences de sécurité sanitaire, notamment pour sa méthodologie qui ne supporterait pas ses conclusions. L'Autorité européenne de sécurité des aliments (EFSA) après une analyse détaillée des conditions opératoires de cette étude a conclu qu'il n'y a aucune raison de changer les conditions d'utilisation de l'aspartame en Europe[28]. La France a aussi émis des réserves sur la méthode d'étude et des doutes quant à la validité des résultats[29] et s'en tient à une « veille toxicologique » sur l'aspartame.
Notes et références
- ↑ a et b Aspartam, 01/2005:0973, Pharmacopée européenne 5.5, EDQM, 16 décembre 2005, https://www.edqm.eu
- ↑ a , b , c , d , e , f et g (en) European chemical Substances Information System, « IUCLID Chemical Data Sheet » sur http://ecb.jrc.ec.europa.eu, Fiche signalétique, Commission européenne. Consulté le 12/12/2008. [pdf]
- ↑ a , b et c Parlement européen et Conseil de l'Europe, « Directive 2008/60/CE établissant des critères de pureté spécifiques pour les édulcorants pouvant être utilisés dans les denrées alimentaires. », dans Journal officiel de l’Union européenne, no L 158, 18/06/2008, p. 17-40 [résumé, texte intégral (pages consultées le 17/10/2008)]
- ↑ a et b (en) ChemIDplus, « Aspartame - RN: 3734-33-6 » sur chem.sis.nlm.nih.gov, U.S. National Library of Medicine. Consulté le 23/07/2008.
- ↑ (en) JM Davey, AH Laird & JS Morley, « Polypeptides. Part III. The synthesis of the C-terminal tetrapeptide sequence of gastrin, its optical isomers, and acylated derivatives », dans Journal of the Chemical Society C: Organic, 1966, p. 555-566 [résumé lien DOI (pages consultées le 18/09/2008.)]
- ↑ (en) M Goodman & YS Oh, « United States Patent 5298272 - Bridged carboxylic ortho ester sweetener » sur www.freepatentsonline.com, 1992. Consulté le 18/09/2008.
- ↑ JM Schlatter (Searle) Brevet ZA 67 02190, 1968.
- ↑ (en) JM Schlatter (Searle), « United States Patent 3492131 - Peptide sweetening agents » sur www.freepatentsonline.com, 1970. Consulté le 18/09/2008.
- ↑ a , b et c (en) E Metcalfe, B Martini & M Gold, « Sweet Talking - research shows potential health risks of aspartame » sur http://www.findarticles.com, June 2000, The Ecologist, p. 1-6. Consulté le 19/09/2008.
- ↑ (en) A Whitmore, « FDA Statement on Aspartame » sur http://www.fda.gov, 1996, FDA - TALK PAPER, Food and Drug Administration. Consulté le 18/09/2008.
- ↑ (en) Aspartame (WHO Food Additives Series 15), International Programme on Chemical Safety. Consulté le 12 juin 2007
- ↑ Parlement européen & Conseil de l'Europe, « Directive 89/107/CEE du 21 décembre 1988 relative au rapprochement des législations des États membres concernant les additifs pouvant être employés dans les denrées destinées à l’alimentation humaine », dans Journal officiel de l’Union européenne, no L 040, 1989, p. 27-33 [résumé, texte intégral (pages consultées le 08/09/2008.)] [pdf]
- ↑ a et b Parlement européen et Conseil de l'Europe, « La directive 94/35/CE concernant les édulcorants modifiée par la Directive 96/83/CE », dans Journal officiel de l'Union européenne, no L 237, 1994 [résumé, texte intégral (pages consultées le 18/09/2008)] [pdf]
- ↑ Parlement européen et Conseil de l'Europe, « Directive 95/31/CE établissant des critères de pureté spécifiques pour les édulcorants pouvant être utilisés dans les denrées alimentaires modifiée par les directives 98/66/CE et 2000/51/CE. », dans Journal officiel de l'Union européenne, 2000 [résumé, texte intégral (pages consultées le 18/09/2008.)]
- ↑ Parlement européen et Conseil de l'Europe, « Directive 2003/115/CE modifiant la directive 94/35/CE concernant les édulcorants destinés à être employés dans les denrées alimentaires. », dans Journal officiel de l’Union européenne, no L 24, 2003, p. 65-71 [résumé, texte intégral (pages consultées le 18/09/2008.)]
- ↑ (en) C Malo & JX Wilson, « Glucose Modulates Vitamin C Transport in Adult Human Small Intestinal Brush Border Membrane Vesicles », dans Journal of Nutrition, no 130, 2000, p. 63-69 [résumé (page consultée le 18/09/2008.)]
- ↑ (en) Codex Alimentarius Commission, « Updated up to the 31st Session of the Codex Alimentarius Commission for Aspartame (951) » sur http://www.codexalimentarius.net, 2008, GSFA Online, Codex Alimentarius. Consulté le 16/10/2008.
- ↑ Aspartame, Food Standards Australia New Zealand
- ↑ Falsifications and Facts about Aspartame, Food Safety and Technology
- ↑ a et b Aspartame, ministère de la Santé du Canada
- ↑ Aspartame, Autorité européenne de sécurité des aliments
- ↑ Am J Clin Nutr. 1997 Mar ; 6 (3): 737-43
- ↑ (en) KL Teff, J Devine & K Engelman, « Sweet taste: effect on cephalic phase insulin release in men. », dans Physiol Behav., vol. 57, no 6, 1995, p. 1089-1095 [résumé lien DOI (pages consultées le 19/09/2008.)].
- ↑ (en) L Prat-Larquemin, JM Oppert, F Bellisle & B Guy-Grand, « Sweet taste of aspartame and sucrose: effects on diet-induced thermogenesis. », dans Appetite, vol. 34, no 3, 2000, p. 245-251 [résumé lien DOI (pages consultées le 19/09/2008.)].
- ↑ [pdf] les dangers de l'aspartame : rumeurs ou réalité ?, Julien Tap et Gaetane Collard, Rapport bibliographique, IUP SIAL sécurité des aliments, Université de Paris XII - Val de Marne, février 2004.
- ↑ Simon S, Les dangers de l'aspartame, "Sacré Planète", oct-nov. 2008, n° 30
- ↑ (en) M Soffritti, F Belpoggi, D Degli Esposti & L Lambertini, « Aspartame induces lymphomas and leukaemias in rats », dans Eur. J. Oncol., vol. 10, no 2, 2005, p. 107-116 [résumé, texte intégral (pages consultées le 18/09/2008.)] [pdf]
- ↑ (en) EFSA, « Opinion of the Scientific Panel on food additives, flavourings, processing aids and materials in contact with food (AFC) related to a new long-term carcinogenicity study on aspartame. : EFSA-Q-2005-122 », dans The EFSA Journal, no 356, 1996, p. 1-44 [résumé, texte intégral (pages consultées le 18/09/2008.)] [pdf]
- ↑ V Gazin, « Veille toxicologique - l'aspartame », dans Bulletin Vigilances, no 29, Octobre 2005, p. 4 (ISSN 1629-3533) [texte intégral (page consultée le 18/09/2008.)][pdf]
Voir aussi
Articles connexes
Bibliographie
- (en) Aspartame: Physiology and Biochemistry De Lewis D. Stegink, Lloyd J. Filer, Publié par CRC Press, 1984, ISBN 9780824772062, 670 pages.
Liens externes
- (en) Safety data sheet - Aspartame sur la base de donnée de la Direction Européenne de la Qualité du Médicament & Soins de Santé DEQM
- (en) Aspartame, European Food safety agency (avis officiels, législation, etc.)
- Édulcorants autorisés, législation européenne sur les édulcorants, Europa.eu.int.
- (en) Summary of Evaluations Performed by the Joint FAO/WHO Expert Committee on Food Additives (résumé des évaluations faites par le comité d'experts communs sur les additifs alimentaires de l'OMS et de la FAO).
- Portail de la chimie
- Portail de la biochimie
- Portail de l’alimentation et de la gastronomie
Catégories : Édulcorant | Ester carboxylique | Peptide
Wikimedia Foundation. 2010.