- Infarctus Du Myocarde
-
Infarctus du myocarde
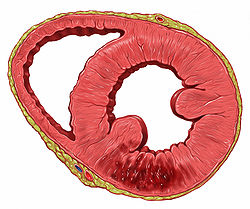
L'infarctus du myocarde (IDM étant une abréviation courante) est une nécrose (mort de cellules) d'une partie du muscle cardiaque. En langage courant, on l'appelle le plus souvent une crise cardiaque. Il se produit quand une ou plusieurs artères coronaires se bouchent, les cellules du myocarde (le muscle constituant le cœur) irriguées par cette (ou ces) artère(s) ne sont alors plus oxygénées, ce qui provoque leur souffrance (douleur ressentie) et peut aboutir à leur mort (cicatrice de l'infarctus qui persistera habituellement). La zone « infarcie » ne se contractera plus correctement.
Sommaire
Épidémiologie
Le nombre d'infarctus du myocarde décroit très sensiblement (près de 60 % en 25 ans), probablement du fait de l'amélioration de la prise en charge des facteurs de risque cardio-vasculaire[1].
Anatomie et terminologie
Il existe deux artères coronaires, la droite et la gauche. Cette dernière est à l'origine de deux grandes branches (inter-ventriculaire antérieure et circonflexe). Elles donnent d'autres branches d'importance inégale. Ces artères irriguent (apportent du sang - de l'oxygène) chacune des différentes zones du cœur. La notion d'infarctus est ainsi variable, en fonction de (ou des) artère(s) touchée(s) et de l'importance de la souffrance du tissu musculaire cardiaque (myocarde).
Suivant la topographie
Suivant l'extension anatomique, on distinguait classiquement les infarctus trans-muraux, c'est-à-dire intéressant la totalité de l'épaisseur du muscle cardiaque (myocarde), des non trans-muraux, ces derniers étant séparés en rudimentaire et en sous-endocardiques (intéressant la partie interne du myocarde, au contact du sang des cavités). Cette distinction a été mis en correspondance avec les différents types de présentation sur l'électrocardiogramme (ECG) :
- l'infarctus transmural correspondant à la présence d'une onde Q large et profonde,
- l'infarctus sous-endocardique correspondant à un sous décalage du segment ST,
- l'infarctus rudimentaire correspondant à une onde T négative.
Cette correspondance anatomo-électrocardiographique, très en vogue dans les années 1970-80, s'est révélé être très souvent erronée et n'est plus utilisée dans les publications internationales.
De même, on distinguait les infarctus antérieur ou antéro-septal, les postéro-diaphragmatique, les inféro-basaux sur des critères uniquement électrocardiographiques en supputant une correspondance bijective avec l'artère lésée. Cette relation est cependant loin d'être absolue et cette terminologie est également progressivement abandonnée.
Actuellement, la classification des infarctus repose uniquement sur des critères électrocardiographiques sans préjuger de l'atteinte réelle anatomique. On distingue ainsi :
- les infarctus avec onde Q ;
- les infarctus sans onde Q.
Le territoire de l'infarctus est nommé suivant la topographie des signes électrocardiographiques : un infarctus antérieur correspond à un infarctus dont l'onde Q est visible dans les dérivations situés « en avant » (V1-V2-V3) et non pas à un infarctus intéressant la partie antérieure du myocarde (même si c'est souvent le cas).
On distingue ainsi :
- les infarctus antérieurs (en V1-V2-V3 sur l'ECG) ;
- les infarctus inférieurs (en D2, D3 et VF) ;
- les infarctus postérieurs (en V7-V8-V9) ;
- les infarctus apicaux (V4, V5 et V6) ;
- les infarctus latéraux (D1, VL).
Suivant le temps
- Un infarctus aigu arrive à l'hôpital avant la douzième heure du début de la douleur : le problème essentiel est alors de déboucher l'artère coronaire pour sauvegarder le maximum de muscle cardiaque.
- Un infarctus sub-aigu ou semi-récent arrive au-delà de la douzième heure. Le problème n'est plus la désobstruction de l'artère responsable, l'essentiel des dégâts étant déjà fait, mais d'éviter les complications.
Suivant le mécanisme ou le mode de présentation
Cette classification est essentiellement un outil de travail à visée épidémiologique. Elle a été définie en 2007 par un panel d'experts internationaux[2]. Elle classe les infarctus en cinq types :
- 1 : infarctus sur lésion d'une ou plusieurs coronaires ;
- 2 : infarctus sur ischémie myocardique sans lésion d'une coronaire (spasme, thrombose...) ;
- 3 : mort subite ;
- 4 : infarctus conséquence d'une complication d'une angioplastie (la thrombose d'un stent étant catégorisée en 4b) ;
- 5 : infarctus conséquence d'une complication d'un pontage aorto-coronarien.
Un type particulier survient lorsqu'une prise en charge médicale rapide permet, d'une manière ou d'une autre, une désobstruction de l'artère coronaire suffisamment rapide pour qu'il n'y aie aucune séquelle, voire, aucune augmentation des enzymes myocardiques signant l'absence, de fait, de nécrose. On parle alors d' infarctus avorté[3].
Mécanismes de l'occlusion
L'oblitération d'une artère coronaire obéit, schématiquement, à deux mécanismes :
- la formation d'un thrombus, la formation d'un "caillot" de sang par les plaquettes qui s'agrègent, libèrent des substances thrombogènes et déclenchent des réactions en chaîne, le plus souvent au niveau de plaque(s) d'athérome préexistante(s) - l'athérome étant un dépôt qui cause l'occlusion de l'artère.
- le spasme coronaire, réduction brutale de la lumière artérielle lié à la vasomotricité des artères, comme dans une crise d'asthme où le calibre des bronches s'auto-réduit spontanément.
Les deux mécanismes s'associent et s'auto-entretiennent - chacun renforçant l'activité de l'autre. Forme la plus habituelle de l'occlusion coronaire.
Mais il existe des formes « pures », spastiques, la plus « classique » étant le Prinzmetal, sus-décalage de ST caractéristique sur l'électro-cardiogramme (ECG), à condition de pouvoir enregistrer l'ECG au bon endroit, au bon moment. L'enregistrement ECG continu (Holter ECG) est ici un précieux outil, toujours à condition que le spasme se produise pendant l'examen.
À côté de cette affection anciennement décrite, existent des infarctus parfaitement authentifiés, ne s'accompagnant pas du sus-décalage bien connu. Infarctus à coronaires normales, saines en coronarographie (radiographies des artères coronaires) ou par endoscopie intracoronaire, technique moins usuelle qui consiste à monter une sorte de caméra — un appareil à ultra-sons micro échographe — à l'intérieur des artères coronaires.
Ces deux formes requièrent des traitements différents (pour ne pas dire opposés).
Dans tous les cas, survient alors une occlusion de l'artère coronaire, plus ou moins complète et, surtout, plus ou moins prolongée, provoquant une ischémie (souffrance cellulaire par défaut d'apport en d'oxygène) du territoire myocardique. Au-delà d'un temps évalué à quatre heures, se produira la mort des cellules musculaires du cœur. Plus l'ischémie persiste, plus la nécrose s'étendra et plus la zone infarcie s'étendra.
Outre la prise en compte du facteur temps dans la gestion de cette urgence médicale, la nécessité absolue d'une analyse minutieuse, pointilleuse de l'examen de référence, l'électrocardiogramme (ECG) comprenant au moins 12 dérivations (12 « angles de vision » de l'activité électrique du cœur), dont l'enregistrement doit être d'excellente qualité (parfois gênée par l'angoisse, bien légitime, d'une personne souffrante), permettra d'affirmer l'ischémie myocardique, si possible avant constitution de la nécrose, et permettra d'en reconnaître le mécanisme dont dépendra l'attitude thérapeutique.
Facteurs de risque et prévention
Article détaillé : facteurs de risque cardio-vasculaire.Facteurs de risque
Les facteurs de risque essentiels aujourd'hui reconnus sont :
- le tabac (ou le tabagisme passif)
- l'excès de cholestérol
- l'âge
- le sexe (masculin)
- le diabète
- l'hypertension artérielle
- l'hérédité (infarctus dans la famille)
- la sédentarité
Prévention
Il s'agit de prévenir un maximum la formation des facteurs de risque indiqués ci-dessus (si possible).
Lutter contre la sédentarité (sport)
Alimentation
Les fruits et légumes protègent le cœur et les vaisseaux sanguins. Grâce à leur richesse en antioxydants et en fibres alimentaires, les fruits et les légumes préviennent l'oxydation du cholestérol afin d'empêcher l'apparition de maladies cardio-vasculaires, premières causes de mortalité dans de nombreux pays développés. Selon l'étude scientifique internationale Interheart publiée le 20 octobre 2008, les personnes ayant une alimentation riche en fruits et en légumes "ont 30% de risque en moins de subir une crise cardiaque que celles en consommant pas ou peu."[4].Aspirine
La prise quotidienne de très petite quantité d'aspirine, qui favorise la fluidité du sang de façon mesurable (action anti-aggrégante plaquettaire -AAP-), réduirait les risques d'infarctus[5][6][7][8].Diagnostic à la phase aiguë
Symptômes
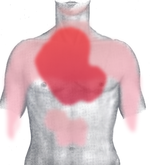
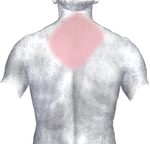
Le symptôme principal est la douleur thoracique. Elle concerne la région rétro-sternale (en arrière du sternum). Elle est violente, habituellement intense (sensation « d'étau broyant la cage thoracique »), prolongée et non (ou peu) sensible à la trinitrine (la trinitrine soulage les douleurs d'angine de poitrine). Elle est dite pan-radiante, irradiant dans le dos, la mâchoire, les épaules, le bras, la main gauche, l'épigastre (estomac). Elle est angoissante, oppressante (difficultés à respirer).
Cette description correspond à la forme typique et caractérisée. En pratique, toutes les variations existent, jusqu’à l'infarctus asymptomatique (sans douleur, sans gêne respiratoire, sans angoisse, ou encore sans malaise), L'infarctus du myocarde étant découvert à l'occasion d'un électrocardiogramme « systématique », par exemple lors d'un bilan de santé.
Sur le plan symptomatique, il existe des formes dites plus trompeuses, douleurs limitées à une (ou à des) irradiation(s), des formes particulières, digestives à type de douleurs épigastriques (région de l'estomac), abdominales hautes, des formes où prédominent telle ou telle manifestation (par exemple vagale, avec sueurs, malaise, sensation de chaleur, éructations), des formes limitées à une oppression angoissante, des formes dominées par une complication ; malaises, mort subite, œdème pulmonaire (essoufflement aigu inexpliqué), choc cardiogénique (pouls et tension imprenables), tamponnade (compression du cœur par un épanchement), troubles du rythme (palpitations, malaise), des formes psychiatriques (brutale désorientation).
Devant toute manifestation dont on ne possède pas la certitude du diagnostic et/ou chez des personnes dont les facteurs de risques sont prédominants, effectuer un électrocardiogramme (ECG) permet de confirmer ou d'infirmer le diagnostic d'infarctus du myocarde.
Signes physiques
L'examen d'un patient présentant un infarctus non compliqué est pauvre en signes cliniques. C'est l'interrogatoire qui fait l'essentiel du diagnostic, l'examen clinique ne permettant que d'éliminer certains diagnostics ou de dépister des complications.
On peut parfois percevoir, à l'auscultation cardiaque, un bruit dit de galop (trouble du remplissage du ventricule), un frottement traduisant un épanchement péricardique (tunique qui entoure le cœur). Mais ce n'est pas une péricardite habituelle (inflammation en règle virale et bénigne du péricarde, structure qui entoure le cœur et lui permet d'avoir des mouvements de contraction).
Signes de gravité
On peut les classer en plusieurs catégories :
Liés au terrain :
- l'âge
- le diabète (risque accru de choc cardiogénique)
- maladie grave associée
Liés à la dysfonction cardiaque :
- infarctus étendu (diagnostic électrique - sur l'électrocardiogramme)
- insuffisance cardiaque
- œdème pulmonaire
- choc cardiogénique
Liés à des complications mécaniques de l'infarctus :
- tamponnade (compression du cœur par un épanchement)
- communication inter ventriculaire
- rupture de paroi (latérale ou autre)
- insuffisance valvulaire aigüe (insuffisance mitrale par dysfonction ou rupture de pilier)
Liés à un trouble du rythme (tachycardie ventriculaire) ou de la conduction (blocs auriculo-ventriculaires.
Il existe des scores prenant compte de plusieurs paramètres et qui sont correlés avec l'évolution de la maladie. L'un des plus utilisés est le score GRACE (Global Registry for Acute Coronary Events : registre global des événements coronariens aigus)[9]. Il prend en compte l'âge du patient, la fréquence cardiaque, la pression artérielle à l'arrivée, la fonction rénale, la présence ou non de signes d'insuffisance cardiaque (classe Killip), ainsi que certaines circonstances péjoratives (arrêt cardiaque).
Examens complémentaires
Électrocardiogramme
 Électrocardiogramme à 12 dérivations montrant des signes d'infarctus du myocarde dans la région inférieure : élévation du segment ST en DII, DIII, et aVF et image en miroir en DI et aVL.
Électrocardiogramme à 12 dérivations montrant des signes d'infarctus du myocarde dans la région inférieure : élévation du segment ST en DII, DIII, et aVF et image en miroir en DI et aVL.
L'interprétation d'un électrocardiogramme (ECG) n'est pas chose aisée. On s'attache à étudier l'ensemble de l'ECG et à rechercher, au sein des 12 dérivations minimales, des signes concordants d'ischémie myocardique.
Concordants veut dire : signes concernant, selon les 12 dérivations minimales - les « angles de vue » du fonctionnement électrique du cœur - un (ou plusieurs) territoire(s) de la même paroi irriguée par une artère coronaire.
L'infarctus ne touche qu'exceptionnellement l'ensemble du cœur (infarctus circonférenciels, d'évolution en règle rapidement fatale).
Les douze dérivations minimales - ces « angles de vue » - explorent des zones du cœur différentes : paroi antérieure, septum interventriculaire, paroi latérale, paroi inférieure (ou inféro-basale), ventricule droit. Ces douze dérivations sont regroupées, plusieurs dérivations (2 ou 3) explorant, de manière un peu différente (l'angle de vue n'est pas tout à fait le même) une paroi du cœur.
Si il y a ischémie, il doit exister une (ou des) zone(s) - topographiques - qui souffrent. L’aspect électrique de ces zones ischémiques contraste avec l'aspect des zones restées saines, non concernées par le processus, car irriguées par une autre artère ou irrigués par des branches de l'artère lésée, ces branches naissant en amont de l'occlusion coronaire. Cette souffrance est concordante, retrouvée dans une partie des douze dérivations.
Le diagnostic de l'ECG permet donc une approche topographique. Il s'agit d'authentifier la zone ischémique mais la correspondance ECG - lésion anatomique est loin d'être constante.
En pratique, il y a un "centre" (zone où l'ischémie est la plus profonde) et des "zones adjacentes d'extension", connues, selon l'anatomie des ventricules (ventricule gauche en règle, le plus important en tant que masse et du point de vue fonctionnel) et l'anatomie des artères coronaires.
Les descriptions électriques "classiques" s'attachent à l'étude :
- des complexes QRS (correspondant à la contraction des ventricules)
- de la repolarisation (correspondant à la relaxation ("repos") des Ventricules, pendant la quelle ils se remplissent "passivement"): segment ST, onde T.
Schématiquement : Les modifications induites par l'ischémie concernent la repolarisation : "troubles de la repolarisation"
- Sus-décalage du segment ST,
- Sous-décalage du segment ST, inversion ou positivation excessive de l'onde T
Les modifications induites par la nécrose concernent les complexes QRS :
- Onde Q (plus grande qu'un tiers d'un autre QRS et qu'1 mm
Attention, l'onde Q peut être le résultat d'un infarctus ancien ou refléter l'activité d'un Septum Inter-Ventriculaire important (ou hypertrophié).
Dosage des enzymes cardiaques
L'augmentation des enzymes cardiaques signe la mort cellulaire conséquence de la nécrose et fait donc partie de la définition d'un infarctus. L'enzyme la plus spécifique et sensible est la troponine (I ou T) dont le dosage tend à supplanter celui des CPK-MB (fraction MB de la Créatine phosphokinase).
L'importance de l'élévation enzymatique est proportionnelle à l'importance de l'infarctus (on parle d'infarctus avec « pic de troponine » à 10, par exemple). La répétition des dosages permet d'en suivre l'évolution.
D'autres enzymes s'élèvent également au cours d'un infarctus mais sont bien moins spécifiques (une augmentation peut se retrouver dans d'autres maladies, cardiaques ou non) et leur utilisation en tant que marqueur tend à être abandonné. Ce sont les SGOT, les SGPT, les LDH.
Prise en charge de l'infarctus
Premiers secours
Le diagnostic d'infarctus du myocarde est d'ordre médical. Celui-ci échappe donc en principe à la compétence du secouriste ou du témoin sauveteur, à qui il apparaîtra soit comme un malaise, soit comme un arrêt cardiaque (mort subite). Dans le cas d'un malaise, il ne faut pas se hasarder à un pseudo-diagnostic : une personne peut avoir un infarctus du myocarde sans ressentir les signes typiques (ni douleur thoracique, ni douleur dans la mâchoire rayonnant dans le bras gauche), et à l'inverse, une personne peut ressentir ces signes sans qu'elle fasse un infarctus du myocarde. Dans tous les cas, tout malaise doit être considéré comme pouvant évoluer vers une urgence vitale et nécessite une prise de contact avec un médecin, qui établira un diagnostic.
Pour un malaise :
- on met la personne au repos dans la position où elle se sent le mieux, on propose dans ce cas la position allongée ;
- on la questionne sur ce qu'elle ressent, les circonstances de survenue du malaise (notamment depuis combien de temps), les antécédents (est-ce la première fois qu'elle ressent ce malaise, prend-elle des médicaments, a-t-elle été hospitalisée)
- on prévient la régulation médicale (« 112 » dans l'Union européenne, le « 15 ou le 18» en France, le « 144 » en Suisse, le « 100 » en Belgique, le « 911 » au Canada, voir Numéro d'appel d'urgence) en transmettant le maximum d'information,
- on revient surveiller la victime et on applique les conseils donnés par la régulation médicale ;
- dans le cadre du prompt secours : mise sous inhalation de dioxygène avec un débit de 9 L/min pour un adulte.
Pour un arrêt cardiaque :
- on protège si nécessaire ;
- on prévient immédiatement les secours (comme ci-dessus) ;
- on pratique la réanimation cardio-pulmonaire en attendant les secours ;
- utilisation d'un défibrillateur automatique si disponible.
Traitement hospitalier
Il s'agit d'une urgence médicale. L'hospitalisation doit être faite en unités spécialisées (en France : USIC ou unités de soins intensifs cardiologiques) disposant de matériels de réanimation et d'une surveillance de paramètres vitaux en continu (électrocardiogramme).
Le patient est mis au repos strict, éventuellement sous oxygène, avec une perfusion veineuse. Un scope de surveillance électrocardiographique est mis en place. Un traitement par antiagrégants plaquettaires (clopidogrel[10] et aspirine) est institué, en plus de la mise sous médicaments anticoagulants (héparine en continu ou en fractionné). La sédation de la douleur peut nécessiter le recours aux morphiniques. La mise sous un dérivé nitré en perfusion est habituelle.
L'attitude vis-à-vis des artères coronaires dépend essentiellement du type de l'infarctus, avec ou sans onde Q sur l'électrocardiogramme.
Infarctus avec onde Q
L'électrocardiogramme est, en règle, typique, et il n'est pas besoin d'attendre les résultats de la biologie (augmentation des enzymes myocardiques) pour en faire le diagnostic.
Outre la prise en charge de la douleur et d'éventuelles complications, le problème crucial est de déboucher le plus rapidement possible (au mieux dans les quatre premières heures) la (ou les) artère(s) coronaire(s) concernée(s). Plus la désobstruction de l'artère coronaire responsable est précoce, moins il y aura de séquelles. Toute suspicion d'infarctus (en pratique douleur thoracique prolongée) doit conduire à l'appel de la régulation médicale (voir Numéro d'appel d'urgence) pour une prise en charge la plus rapide possible.
Deux méthodes sont employées pour désobstruer une artère :
- Soit par un traitement "médical", utilisant des produits qui visent à détruire ("lyser") le thrombus (caillot de sang) obstruant l'artère ; c'est la "thrombolyse/fibrinolyse" (injection par simple voie intra-veineuse - comme lors d'une prise de sang - d'un médicament qui va dissoudre le caillot dans l'artère. Cette thrombolyse peut-être faite sur le lieu même de prise en charge de l'infarctus, c'est-à-dire, bien avant l'arrivée en milieu hospitalier (thrombolyse pré-hospitalière). Le produit fibrinolytique le plus utilisé sont les différentes formes de Tpa (tissue plasminogen activator).
- Soit désobstruction "instrumentale" par angioplastie, en introduisant, au cours d'une coronarographie (radiographies des artères coronaires) un micro cathéter dans l'artère pour dilater la lésion (les lésions) responsable(s). Le geste est le plus souvent associée à la mise en place d'un stent (ressort), dans l'artère. La pratique d'une angioplastie nécessite cependant une hospitalisation dans un centre spécialisé. Le taux de réussite du geste est supérieur à celui de la fibrinolyse[11]. On parle d' angioplastie primaire ce geste fait au décours immédiat d'un infarctus.
Le choix entre ces deux méthodes dépend essentiellement de leur disponibilité (proximité d'un centre pratiquant l'angioplastie). Elles sont complémentaires, une angioplastie en urgence pouvant être proposée en cas d'échec de la fibrinolyse (jugée sur la persistance de la douleur et des anomalies sur l'électrocardiogramme), permettant alors une meilleure chance d'évolution favorable[12]. Par contre, le recours systématique à une angioplastie en urgence, quel que soit le résultat de la fibrinolyse, n'a pas démontré d'intérêt[13].
Une angioplastie secondaire de l'artère responsable, c'est-à-dire faite quelques jours après la survenue de l'infarctus, semble avoir un certain intérêt au niveau pronostic[14]. Par contre, si l'infarctus est vu tardivement et que l'artère est toujours occluse, une désobstruction systématique par angioplastie ne semble pas bénéficiable en l'absence d'ischémie myocardique prouvée[15].
Parfois, ces mesures peuvent s'avérer en effet partiellement voire totalement inefficaces (multiplicité des artères coronaires concernées, étendue des obstructions, obstruction complète infranchissable, siège particulier et/ou caractère anatomique des lésions). Un ou plusieurs pontages aorto-coronariens peuvent être alors proposés, idéalement un peu à distance de l'infarctus.
Infarctus sans onde Q
Les signes électrocardiographiques sont moins typiques et le diagnostic doit être étayé par une augmentation du taux des enzymes myocardiques dans le sang. Il n' y a pas, classiquement, d'indication à une tentative de désobstruction urgente par fibrinolyse ou par angioplastie primaire.
Une angioplastie secondaire systématique semble en améliorer le pronostic[16].
Après l'hospitalisation
Médicaments
La médication prescrite à la sortie du patient peut varier selon la situation clinique. Toutefois, cinq classes de médicaments apparaissent comme des standards dans le traitement post-infarctus.
- Acide acétylsalicylique (Aspirine) : Devrait normalement être prescrit chez tous les patients ayant subi un infarctus, sauf si une contre-indication est présente. La dose est comprise entre 75 et 160 mg, une fois par jour, et sa prescription doit être à vie. Par son effet anti aggrégant plaquettaire, elle réduit le risque d'une nouvelle occlusion d'une artère coronaire. En Amérique du Nord, la dose est généralement de 80 ou 81 mg puisque le médicament est disponible à cette dose. En cas de problème (allergie, rarissime, ou intolérance), il peut être remplacé par le clopidogrel.
- Bêta-bloquants : Cette classe de médicament a été montrée bénéfique quel que soit le type d'infarctus, son ampleur ou les caractéristiques du patient. Ils semblent toutefois encore plus bénéfiques chez les patients ayant fait un infarctus plus grave. Les bêta-bloqueurs vont aider à diminuer la tension artérielle, mais aussi à réduire la poussée adrénergique sur le cœur. Ils réduisent ainsi le risque d'un nouvel infarctus ou l'évolution vers l'insuffisance cardiaque. Il semble peu rationnel d'utiliser un bêta-bloqueur avec une activité sympathomimétique intrinsèque (ASI). Les molécules les plus étudiées et les plus utilisées sont le metoprolol (12,5 à 100 mg 2 fois par jour en forme régulière) le bisoprolol (1,25 à 10 mg 1 fois par jour) et l'aténolol. Cette médication devrait être prise à long terme.
- Inhibiteurs de l'enzyme de conversion de l'angiotensine : Comme les bêta-bloqueurs, ces médicaments vont aider au contrôle de la tension artérielle, mais ils vont également réduire le remodelage cardiaque, qui peut mener à l'insuffisance cardiaque. Également comme les bêta-bloqueurs, ils devraient être prescrits chez un patient post-infarctus, même si ce dernier a une tension artérielle normale. En cas d'intolérance, ils peuvent être remplacés par un antagoniste des récepteurs de l'angiotensine. Parmi les inhibiteurs de l'enzyme de conversion fréquemment prescrits, on peut citer le ramipril (1,25 à 20 mg 1 fois par jour) ou l'énalapril (2,5 à 40 mg 1 fois par jour). Cette médication devrait être prise à long terme.
- Statines : Bien qu'étant données initialement dans le but de faire baisser un niveau de cholestérol sanguin élevé, elles sont efficaces quelle que soit la valeur de celui-ci dans la réduction du risque de survenue d'un nouvel accident cardiaque. Celles qui ont démontré une baisse d'événements cardio-vasculaires sont l'atorvastatine (40 à 80 mg 1 fois par jour au coucher), la simvastatine (40 mg) et la pravastatine (40 mg). Cette médication devrait être prise à long terme.
- Clopidogrel : Ce médicament Antiagrégant plaquettaire va également réduire le risque de thrombose, mais par un mécanisme différent de celui de l'aspirine. Il sera combiné avec ce dernier chez les patients ayant été traités par l'implantation d'un stent. La durée du traitement est variable, mais généralement, le patient va recevoir la combinaison aspirine + clopidogrel durant au moins 1 an, l'aspirine étant laissé seul par la suite.
Autres
La lutte contre les facteurs de risque cardio-vasculaire est indispensable : arrêt du tabagisme, prise en charge d'un diabète, d'une obésité, mise en place d'une activité physique adaptée...
En cas de dysfonction ventriculaire sévère, définie par une fraction d'éjection inférieure à 35%, la pose d'un défibrillateur implantable est recommandée devant le risque important de mort subite[17].
Complications
La mortalité hospitalière est un peu inférieure à 10%. L'insuffisance cardiaque survient dans un peu plus de 10% à la phase aiguë, les chiffres tendant à diminuer actuellement, du fait d'une meilleure prise en charge initiale[18].
La mortalité est essentiellement due à une insuffisance cardiaque, soit secondaire à la taille de l'infarctus, soit, plus rarement, due à une complication mécanique : insuffisance mitrale aiguë par rupture d'un pilier, formation d'une communication entre les cavités droites et gauches cardiaques... A distance de l'épisode aigu, un quart des décès sont consécutifs à une mort subite, même si cette issue tend à devenir moins fréquente[19]. Le risque est d'autant plus important en cas de dysfonction ventriculaire gauche majeure et la pose d'un défibrillateur automatique implantable doit être discutée dans ces cas.
Les troubles du rythme cardiaque sont une complication fréquente.
Notes et références
- ↑ Hardoon SL, Whincup PH, Lennon LT et Als. How much of the recent decline in the incidence of myocardial infarction in british men can be explained by changes in cardiovascular risk factors?: evidence from a prospective population-based study, Circulation, 2008;117:598-604
- ↑ Thygesen K, Alpert JS, White HD, Universal definition of myocardial infarction, Eur Heart J, 2007;28:2525-2538
- ↑ Taher T, Fu Y, Wagner GS et als. Aborted myocardial infarction in patients with ST-segment elevation: insights from the Assessment of the Safety and Efficacy of a New Thrombolytic Regimen-3 Trial Electrocardiographic Substudy, J Am Coll Cardiol, 2004;44:38-43
- ↑ Etude Interheart 20 octobre 2008 (réalisée sur 16.000 personnes), citée dans Le Monde, 23 octobre 2008, page 27.
- ↑ Recommandations de l’Académie nationale de médecine pour la prise en charge des patients après infarctus du myocarde - Rapport de André VACHERON et Jean-Paul BOUNHOURE[1], au nom d’un groupe de travail de la commission IV ( Maladies cardiovasculaires) - Académie nationale de médecine - novembre 2007
- ↑ Antiplatelet Trialists’ Collaboration. Collaborative overview of randomized trials of antiplatelet therapy. I : prevention of death, myocardial infarction, and stroke by prolonged antiplatelet therapy in various categories of patients. Br Med J 1994; 308: 81-106.
- ↑ Coronary Drug Project Research Group.Aspirin in coronary heart disease. J Chron Dis 1976; 29:625-42.
- ↑ Aspirin Myocardial Infarction Study Research Group.A randomized, controlled trial of aspirin in persons recovered from myocardial infarction. JAMA 1980; 243: 661-9.
- ↑ de Araujo Goncalves P, Ferreira J, Aguiar C, Seabra-Gomes R, TIMI, PURSUIT, and GRACE risk scores: sustained prognostic value and interaction with revascularization in NSTE-ACS, Eur Heart J 2005;26:865-872
- ↑ Chen ZM, Jiang LX, Chen YP et als. Addition of clopidogrel to aspirin in 45,852 patients with acute myocardial infarction: randomised placebo-controlled trial, Lancet, 2005;366:1607-1621
- ↑ White HD, Chew DP, [372:570-584 Acute myocardial infarction], Lancet, 2008;372:570-584
- ↑ Wijeysundera HC, Vijayaraghavan R, Nallamothu BK et als. Rescue angioplasty or repeat fibrinolysis after failed fibrinolytic therapy for ST-segment myocardial infarction: a meta-analysis of randomized trials, J Am Coll Cardiol, 2007;49:422-430
- ↑ Keeley EC, Boura JA, Grines CL, Comparison of primary and facilitated percutaneous coronary interventions for ST-elevation myocardial infarction: quantitative review of randomised trials, Lancet, 2006;367:579-588
- ↑ Collet JP, Montalescot G, Le May M et als. Percutaneous coronary intervention after fibrinolysis: a multiple meta-analyses approach according to the type of strategy, J Am Coll Cardiol, 2006;48:1326-1335
- ↑ Hochman JS, Lamas GA, Buller CE et als. Coronary intervention for persistent occlusion after myocardial infarction, N Engl J Med, 2006;355:2395-2407
- ↑ Bavry AA, Kumbhani DJ, Rassi AN et als. Benefit of early invasive therapy in acute coronary syndromes: a meta-analysis of contemporary randomized clinical trials, J Am Coll Cardiol, 2006;48:1319-1325
- ↑ Moss AJ, Zareba W, Hall WJ et als. Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction, N Engl J Med, 2002;346:877-883
- ↑ Fox KA, Steg PG, Eagle KA et als. Decline in rates of death and heart failure in acute coronary syndromes, 1999–2006, JAMA, 2007;297:1892-1900
- ↑ Selcuk Adabag A, Therneau TM, Gersh BJ, Weston SA, Roger VL, Sudden death after myocardial infarction, JAMA, 2008;300:2022-2029
Annexes
Bibliographie
- Antman EM, Anbe DT, Armstrong PW et coll. ACC/AHA Guidelines for the Management of Patients With ST-Elevation Myocardial Infarction. Circulation 2004.110:82-292.
Liens externes
- Prise en charge de l’infarctus du myocarde à la phase aiguë en dehors des services de cardiologie - Conférence de consensus - 23 novembre 2006
- Portail de la médecine
Catégories : Urgence médicale | Maladie cardio-vasculaire
Wikimedia Foundation. 2010.