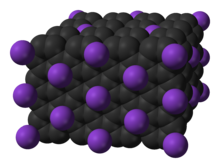
- Composé d'insertion du graphite
-
Les composés d'insertion du graphite, appelés aussi composés d'intercalation du graphite sont des matériaux complexes qui ont une formule général X-Cy où X est un élément chimique ou une molécule inséré, intercalé entre les couches de graphène, constitutif du graphite, un allotrope du carbone[1],[2],[3],[4]. Dans ce type de composés, les couches du graphite restent intactes et les atomes ou molécules hôtes restent localisés entre elles. Quand la matrice (graphite) et l'hôte X interagissent par transfert de charge, généralement, la conductivité électrique dans les plans augmentent. Quand l'hôte forme des liaisons covalentes avec les plans du graphite comme pour les fluorures ou les oxydes, le conductivité décroît comme la conjugaison du système pi du graphène s'effondre.
Sommaire
Structure générale
Dans un composé d'insertion du graphite, chaque espace intercouche n'est pas nécessairement occupée par l'hôte. Dans les composés appelés stage 1, les couches de graphite et les couches d'hôtes intercalés alternent et dans les composés stage 2, deux couches de graphite sans hôte alternent avec une couche d'hôtes. Ces compositions idéales peuvent variées et donc ces composés sont un exemple de composés non-stoechiométriques. il est habituel de spécifier la composition avec le stage.
En stage 1, les composés d'intercalation binaires métal-graphite ont la stœchiométrie X-C8 pour les métaux avec les plus grands rayons atomiques (X = K, Rb et Cs) et X-C6 pour les plus petits (X = Li, Sr, Ba, Eu, Yb and Ca)[2].
Calcium-graphite
De grosses quantités de calcium-graphite Ca-C6 sont obtenues par immersion de graphite pyrolytique(en) très orienté, dans un alliage Li-Ca bien choisi fondu pendant un long moment (10 jours à 350 °C). La structure cristalline de Ca-C6 correspond au groupe d'espace R¯3m. La distance entre couches de graphite augmente de 335 pm à 452,4 pm et la distance carbone-carbone augmente de 142 à 144,4 pm. Parmi les composés d'insertion supraconducteurs, Ca-C6 a la plus haute température critique, Tc = 11.5 K, qui augmente quand une pression est appliquée, 15.1 K à 8 GPa[2].
Potassium-graphite
La forme K-C8 du potassium-graphite est l'un des plus forts agents réducteurs connus. Il est préparé sous atmosphère inerte en fondant du potassium sur une poudre de graphite. Le potassium est absorbé par le graphite et la couleur change du noir aux teintes bronze. Le solide obtenu peut s'enflammer spontanément lorsqu'il est exposé à l'air. Structurellement, la composition peut s'expliquer en considérant que la distance potassium-potassium est le double de la distance entre les centres des hexagones dans les couches du graphite. La liaison entre le graphite et le potassium est ionique et le composé est un conducteur électrique[5]. K-C8 est un supraconducteur avec une température critique très basse, Tc =0.14 K[2]. Il a été aussi utilisé comme catalyseur de polymérisations et comme un réactif pour réaction de couplage d'halogénures d'aryl en bisphényl[6]. Dans une étude[6], du K-C8 fraichement préparé, est traité du 1-iodododécane (CH3-(CH2)8-CH2I) et forme des plaquettes de taille micrométrique de carbone entourées de longues chaînes alkyl qui permettent de rendre ces plaquettes solubles dans le chloroforme. Un autre composé potassium-graphite, le K-C24 a été utilisé comme monochromateur de neutron.
Fluorures de carbone
Le monofluorure de carbone est noté (CF)x et est utilisé comme cathode dans un type de batteries lithium. il est préparé par réaction entre du fluor gazeux et du graphite à 215-230 °C. Sa couleur est gris, blanc ou jaune. Les liaisons entre le carbone et le fluor sont covalentes. Ce composé est un isolant électrique.
Le monofluorure de tétracarbone (C4F ou F-C4) est préparé par réaction entre le fluor gazeux mélangé de fluorure d'hydrogène, HF, avec du graphite à température ambiante. Ce composé a une couleur bleu-noir.
Autres composés d'insertion
D'autres composés d'intercalation du graphite sont le bisulfate-graphite et l'oxyde de graphite. Des exemples de composés d'insertion du graphite avec des complexes sont ceux avec comme hôtes du baryum et de l'ammoniac (Ba(NH3)2.5-C10.9(st.1)) ou ceux avec du césium, de l'hydrogène et du potassium (Cs-C8.K2H4/3-C8(st.1)).
Notes
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Graphite intercalation compound » (voir la liste des auteurs)
- M.S. Dresselhaus and G. Dresselhaus, Review: Intercalation compounds of graphite, Advances in Physics, 1981, 30, p 139 (187 pages)
- N. Emery et al., Review: Synthesis and superconducting properties of CaC6, Sci. Technol. Adv. Mater., 2008, 9, 044102. article
- H-P Boehm et al., Nomenclature and terminology of graphite intercalation compounds, Pure & Appl. Chem., 1994, 66, p. 1893. article .pdf
- D. Savoia et al., Applications of potassium-graphite and metals dispersed on graphite in organic synthesis, Pure & Appl. Chem., 1985, 57, p. 1887. article .pdf
- (en) NIST Ionizing Radiation Division 2001 - Technical Highlights
- S. Chakraborty et al., Functionalization of Potassium Graphite", Angew. Chem. Int. Ed., 2007, 46, p. 4486. DOI 10.1002/anie.200605175
Liens externes
Voir aussi
Catégorie :- Composé du carbone
Wikimedia Foundation. 2010.