- Acide méthacrylique
-
Acide méthacrylique 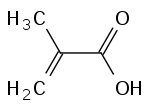
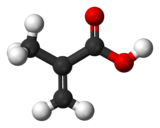
Général Nom IUPAC acide 2-méthyl-2-propénoïque Synonymes acide méthylacrylique
acide méthacryliqueNo CAS No EINECS ChEBI SMILES InChI Apparence liquide incolore d'odeur âcre. Propriétés chimiques Formule brute C4H6O2 [Isomères] Masse molaire[1] 86,0892 ± 0,0042 g·mol-1
C 55,81 %, H 7,02 %, O 37,17 %,Propriétés physiques T° fusion 14,85 °C [2] T° ébullition 162,55 °C [2] Solubilité dans l'eau : miscible, Masse volumique 1,00913 g·cm-3 (liquide,25 °C)[3] T° d'auto-inflammation 385 °C [4] Point d’éclair 68 °C [4] Limites d’explosivité dans l’air 2,1–8,7 %vol à 25 °C [4] Pression de vapeur saturante 0,87 mbar à 20 °C
1,9 mbar à 30 °C
8 mbar à 50 °C [4]Viscosité dynamique 1,38 mPas à 24 °C [5] Thermochimie ΔfH0gaz -367,3 kJ·mol-1 [2] ΔfH0liquide -414,8 kJ·mol-1 [2] ΔfusH° 8,0625 kJ·mol-1 à 287,5 K [2] ΔvapH° 47,5 kJ·mol-1 [2] Cp 159,7 J·K-1·mol-1 (liquide,298,15 K) PCI -2 016,7 kJ·mol-1 (liquide) [2] Propriétés optiques Indice de réfraction  [7]
[7]Précautions Directive 67/548/EEC[8] 
CPhrases R : 21/22, 35, Phrases S : 1/2, 26, 36/37/39, 45, Transport[4] 89 2531 NFPA 704[9] SIMDUT[10] 



Écotoxicologie LogP 0,93 [4] Unités du SI & CNTP, sauf indication contraire. L'acide méthacrylique ou acide méthylacrylique est un acide carboxylique de formule brute C4H6O2.
Historique
L'histoire de l'acide méthacrylique commence en 1865, année où il est synthétisé pour la première fois à partir du méthacrylate d'éthyle[5]. Il faut toutefois attendre les travaux de Otto Röhm sur la polymérisation pour que l'intérêt devienne commercial en 1901. Ce dernier fonda une compagnie et après la Première Guerre mondiale, développa une voie de synthèse à partir de la cyanohydrine d'éthylène (2-cyanoéthanol), puis plus tard en compagnie de Walter Bauer, il utilisa la cyanohydrine d'acétone (2-cyano-2-propanol). En 1931, il obtint un polymère solide transparent qui est considéré comme un de premier verre organique.
Propriétés physico-chimiques
L'acide méthacrylique est très réactif avec les groupes carboxyles, vinyles et esters[5].
Les principales réactions sont[5]:
- Addition sur la double liaison carbone-carbone
- Addition de groupes cyanures, halogénures, alcools, de sulfures ou d'amines conduit à des dérivés de l'acide 2-méthylpropanoïque
- Réaction avec des diènes selon le schéma de la réaction de Diels-Alder.
- Polymérisation
- L'acide polymérise facilement en présence d'initiateurs radicalaires (peroxydes, UV). L'absence d'oxygène est nécessaire sous peine de former des radicaux hydroperoxydes. Les monomères peuvent être récupérés après polymérisation par chauffage à des températures de plus de 300 °C.
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) « 2-Propenoic acid, 2-methyl- » sur NIST/WebBook, consulté le
- (en) Jaime Wisniak, Gladis Cortez, René D. Peralta, Ramiro Infante et Luis E. Elizalde, « Some Thermodynamic Properties of the Binary Systems of Toluene with Butyl Methacrylate, Allyl Methacrylate, Methacrylic Acid », dans Journal of Solution Chemistry, vol. 36, no 8, aouût 2007, p. 997-1022 [lien DOI (page consultée le 25 janvier 2010)]
- Entrée de « Methacrylic acid » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 25 janvier 2010 (JavaScript nécessaire)
- (en) William Jr.1 Bauer, Methacrylic Acid and Derivatives, Wiley-VCH Verlag GmbH & Co., coll. « Ullmann's Encyclopedia of Industrial Chemistry », 15 juin 2000
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, Huston, Texas, Gulf Pub. Co. (ISBN 0-88415-857-8)
- (en) V. N. Verezhnikov et I. N. Pshenichnaya, « Heterocoagulation of anionic and cationic latexes with particles bearing intrinsic charge », dans Russ. J. Appl. Chem., vol. 79, no 7, juillet 2007, p. 1158-1161 [lien DOI (page consultée le 25 janvier 2010)]
- « acide méthacrylique » sur ESIS, consulté le
- UCB Université du Colorado
- « Acide méthacrylique » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 janvier 2010
Wikimedia Foundation. 2010.





