- Pet scan
-
Tomographie par émission de positons
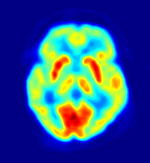
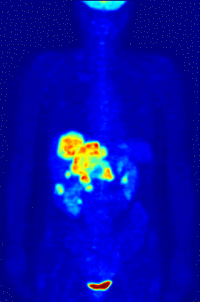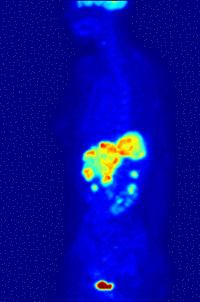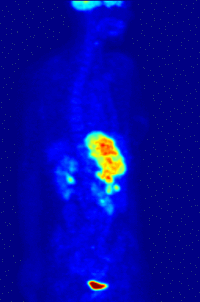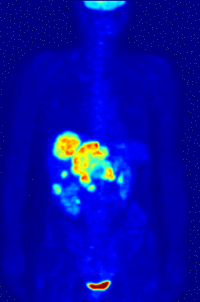 Reconstruction tridimensionnelle de la distribution de glucose marqué au fluor 18 telle que mesurée par tomographie d'émission de positons
Reconstruction tridimensionnelle de la distribution de glucose marqué au fluor 18 telle que mesurée par tomographie d'émission de positons
La tomographie par émission de positons (TEP) est une méthode d'imagerie médicale pratiquée par les spécialistes en Médecine nucléaire qui permet de mesurer en trois dimensions l'activité métabolique d'un organe grâce aux émissions produites par les positons issus de la désintégration d'un produit radioactif injecté au préalable. (terminologie anglo-saxonne : « positron emission tomography » - PET ou PETscan-)
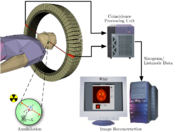
La TEP repose sur le principe général de la scintigraphie qui consiste à injecter un traceur dont on connaît le comportement et les propriétés biologiques pour obtenir une image du fonctionnement d'un organe. Ce traceur est marqué par un atome radioactif (carbone, fluor, azote, oxygène...) qui émet des positons dont l'annihilation produit elle-même deux photons. La détection de la trajectoire de ces photons par le collimateur de la caméra TEP permet de localiser le lieu de leur émission et donc la concentration du traceur en chaque point de l'organe. C'est cette information quantitative que l'on représente sous la forme d'une image faisant apparaître en couleurs les zones de forte concentration du traceur.
Ainsi la TEP permet de visualiser les activités du métabolisme des cellules : on parle d'imagerie fonctionnelle par opposition aux techniques d'imagerie dite structurelle comme celles basées sur les rayons X (radiologie ou CT-scan) qui réalisent des images de l'anatomie. Par conséquent, la tomographie par émission de positons est un outil diagnostique qui permet de déceler certaines pathologies qui se traduisent par une altération de la physiologie normale comme les cancers. La TEP est aussi utilisée en recherche biomédicale, par exemple en imagerie cérébrale où elle permet de révéler les régions actives du cerveau lors de telle ou telle activité cognitive de manière analogue à ce qui se fait avec l'imagerie par résonance magnétique fonctionnelle.
Sommaire
Historique
La technique a été développée pour la première fois en 1975[1].
Qu’est-ce qu’une TEP ?
Une tomographie par émission de positons (TEP) est un examen d’imagerie médicale par scintigraphie réalisé dans le service de médecine nucléaire d'un hôpital ou d'une clinique.
La scintigraphie en TEP est obtenue par injection d’un traceur faiblement radioactif par voie intraveineuse. Ce traceur est le plus souvent le fluor (18F) incorporé dans une molécule de glucose formant le 18F-flurodéoxyglucose (en abrégé 18F-FDG). Ce traceur est semblable au glucose : il se fixe au niveau des tissus qui consomment de grandes quantités de ce sucre comme les tissus cancéreux, le muscle cardiaque ou encore le cerveau. Le fluor 18, dont la demi-vie est inférieure à deux heures, émet ensuite de façon temporaire des rayonnements que l’on peut suivre dans l’organisme du patient grâce à une caméra spéciale, une caméra TEP. Le fluor 18 ainsi que les autres isotopes pouvant être utilisés (oxygène (15O), azote (13N), carbone (11C)) ont une courte demi-vie, jusqu’à 110 minutes pour le fluor. Ces isotopes de courte durée nécessitent pour leur production un cyclotron.
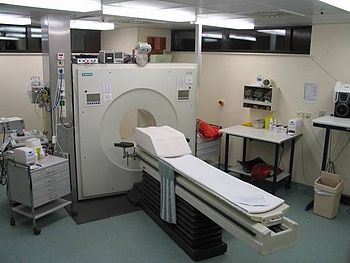
Une caméra TEP est un appareil qui a l’aspect d’un scanner mais son principe de fonctionnement est différent.
En effet, l'atome radioactif (par exemple, le fluor 18) se désintègre en émettant un positon. Celui-ci va s'annihiler avec un électron du milieu, après un très court parcours (en général inférieur à 1 mm). Cette annihilation produit deux photons gamma de 511 keV qui partent sur une même direction mais dans un sens opposé, ce qui rend possible le traitement tomographique des données. En effet, les capteurs situés tout autour du patient détectent les photons d'annihilation en coïncidence (c’est-à-dire ceux qui arrivent en même temps), ce qui permet d'identifier la ligne sur laquelle se trouve l'émission des photons. Un système informatique reconstitue ensuite à l'aide d'un algorithme de reconstruction les images de la répartition du traceur au niveau d’une partie ou de la totalité du corps sous la forme d'une image 2D ou d'un objet 3D. Les images ainsi obtenues sont dites "d’émission" (la radioactivité provient du traceur injecté au patient). La résolution spatiale de l'image ainsi obtenue est comprise entre 4 et 7 mm[2].
Il est possible d’améliorer la qualité des images en utilisant le principe de correction d’atténuation. Lors de la traversée du corps, de nombreux photons gamma subissent une atténuation liée aux structures traversées.
En effet, il est aisé de comprendre qu'un foyer hyperfixant situé en profondeur, tel qu'un ganglion lombo-aortique, devra traverser beaucoup plus de matières qu'un foyer de surface tel qu'un mélanome.
Pour effectuer cette correction, on utilisait initialement des images de transmission obtenues grâce à une source radioactive qui tourne rapidement autour du patient ; mais aujourd'hui, la plupart des caméras TEP sont couplées à un tomodensitomètre à rayons X (système TEP/TDM ou PET/CT en anglais), ce qui permet de superposer l'image fonctionnelle (Image TEP) à sa localisation anatomique précise dans le corps (Image CT).
La correction d’atténuation ainsi réalisée permet de réaliser l'examen beaucoup plus rapidement et permet d'obtenir des images de meilleure qualité.Exposition aux radiations et radioprotection
Au cours d'une tomographie par émission de positons, le patient reçoit une dose d'environ 10 mSv ce qui correspond à la dose reçue au cours d'un scanner thoraco-abdominal. On injecte en général au patient de l'ordre de 3 à 5 MBq/kg (5 millions de désintégrations par seconde) soit de 5 à 10 mCi pour un adulte pour le FDG. L’activité injectée varie en fonction du poids et de l’âge du patient. La période radioactive (la période où l'activité du produit se divise par 2) du produit le plus utilisé en TEP (le 18F) est de l'ordre de 110 minutes, donc en 12 heures la quasi-totalité de la radioactivité a disparu. En réalité, la radioactivité disparait encore plus rapidement car le FDG est naturellement éliminé avec les urines.
L'examen lui-même dure en général près d'une demi-heure.
La réalisation de cet examen ne présente pas de danger pour les patients ni pour leur entourage. Cependant quelques précautions sont à prendre pour éviter une exposition inutile aux radiations.
En raison de l’activité des radionucléides injectés (même s’ils ont une durée de vie courte), cet examen est contre-indiqué aux femmes enceintes, comme tous les examens utilisant des radiations ionisantes. Les mères allaitant devront suspendre l’allaitement durant dix à douze heures après l’injection car une partie du traceur radioactif peut se retrouver dans le lait maternel. Les contacts avec les jeunes enfants et les femmes enceintes sont à éviter la journée suivant l’examen. De légères précautions de bon sens sont donc à prendre vis-à-vis du milieu familial, professionnel ou hospitalier pendant environ 12 heures, temps moyen pour que la plus grande partie de la radioactivité ait disparu.
De plus, des précautions supplémentaires sont à prendre pour les patients incontinents ou porteurs d’une sonde urinaire du fait de l’élimination du traceur par les urines.
Principaux traceurs utilisés
Le 18F FDG
Le 18F-FDG (Fluorodeoxyglucose marqué au Fluor 18) est un sucre semblable au glucose, rendu radioactif. C’est la radioactivité de ce fluor particulier rajouté au glucose qui permet sa détection par la caméra TEP. Pour vivre, fonctionner et se reproduire, les cellules ont besoin d’énergie sous forme de glucose, sucre assimilable par l’organisme. Cette source énergétique est essentielle aux nombreuses cellules de l’organisme et elle se trouve naturellement dans le sang. Plus l’activité des cellules est importante, plus leur consommation de glucose augmente.
Les cellules cancéreuses se multiplient sans cesse. Ces nombreuses multiplications nécessitent beaucoup d’énergie. Elles ont donc une consommation anormalement élevée de glucose par rapport aux cellules normales. C’est grâce à cette consommation excessive de glucose que l’on peut repérer le tissu cancéreux avec la caméra TEP.
Le 18F-FDG se comporte comme le glucose, mais contrairement à celui-ci, il n’est pas une source d’énergie utilisable par la cellule cancéreuse. Il s’accumule alors dans la cellule qui devient radioactive, de plus la molécule 18F- FDG est phosphorylée par la cellule qui "tente" de l'assimiler dans son métabolisme, ce qui l'empêche de ressortir de la cellule et le 18F-FDG-6P s'y accumule.
En devenant radioactive, elle émet des rayonnements qui peuvent être détectés par la caméra TEP. Le tissu cancéreux est ainsi repéré grâce à l’accumulation du produit radioactif sous la forme d’une image d’hyperfixation.
Toutes les informations recueillies par la caméra TEP reposent sur la radioactivité repérée dans les tissus après l'injection du 18F-FDG au patient. Le système informatique relié à la caméra TEP produit des coupes et des images en trois dimensions des endroits du corps où le 18F-FDG s'est accumulé.
Comment se déroule l’examen TEP ?
Pour que l’examen se déroule dans des conditions optimales, il convient de respecter certaines indications. Une éventuelle grossesse est à préciser, tout retard de règles sera donc signalé. Il faut rester à jeun 6 à 8 heures avant l’examen. Evitez tout exercice physique depuis la veille de l’examen (par exemple un marathon la veille) ceci inclut la conduite automobile le jour-même de l’examen pour ne pas stimuler la consommation de glucose par les fibres musculaires. Dans la plupart des cas, il n’est pas nécessaire d’arrêter ou de modifier son traitement médical. Dans certaines situations, il est demandé que la prise de médicament soit effectuée au plus tard 6 heures avant l’examen ou 6 heures après. De plus, il convient de respecter un certain délai après une chimiothérapie (3 semaines), une radiothérapie (4 mois), une chirurgie (2 mois) et après l’injection de facteurs de croissance hématopoïétiques (1 semaine) avant l’examen TEP. En effet, ces traitements peuvent modifier la répartition du traceur au sein du corps. Le diabète qui entraine une augmentation de la concentration de glucose dans le sang peut modifier les résultats de la TEP, c’est pourquoi le patient doit signaler son diabète au praticien pour qu’il prenne les dispositions adéquates.
L’examen se déroule en deux temps. À son arrivée, le patient est installé sur un lit et doit se reposer. Un technicien spécialement formé injecte dans une veine du bras ou dans une perfusion posée au préalable, une dose de traceur radioactif (par exemple, le 18F-FDG) diluée dans une solution salée (du sérum physiologique). Le patient reste au repos une heure au moins. Ce temps permet au produit de bien se répartir dans l’organisme et d’être capté par les tissus (comme les tumeurs).
Il est installé au calme dans une pièce sombre. À partir de l’injection, toutes les activités qui peuvent perturber la diffusion du traceur sont à éviter. Il faut rester le plus immobile possible (en évitant de bouger, de parler ou de mâcher un chewing-gum) afin de ne pas stimuler les muscles, de même il est déconseillé de lire car cela fait travailler le cerveau et donc augmente la consommation de glucose, ce qui risque de modifier les résultats de l’examen.
Avant de s’installer sur le lit d’examen de la machine TEP, le patient se rend aux toilettes afin de vider au maximum la vessie (voie d'élimination du produit non fixé). Lors de l’examen, le patient est allongé sur un lit qui se déplace à l’intérieur d’un anneau détecteur. Seule une partie du corps se trouve à l’intérieur de l’appareil. De ce fait, les patients claustrophobes ne ressentent en général aucune gêne particulière au cours de l'examen. De plus, la machine est silencieuse, contrairement à l'IRM.
L’enregistrement des images dure de 20 à 40 minutes selon les machines ou l'indication de l'examen. Au total, le patient doit prévoir de rester dans le service environ 2 à 3 heures pour l’ensemble de la procédure. Un premier avis peut être donné par l’équipe médicale sur place mais le compte rendu détaillé de l’examen nécessite un délai de plusieurs heures voire d’une journée ou deux. Après l’examen, il est recommandé de bien boire afin d’éliminer le plus rapidement possible le traceur et ne pas se retenir avant d’uriner.
Le diagnostic
Lors du diagnostic, une TEP peut être réalisée pour tenter d’identifier la maladie à l’origine des signes ou des symptômes ressentis ou observés par le patient ou d’une anomalie décelée lors d’une radiographie ou d’une échographie. Elle peut aider à déterminer si une anomalie est en fait bénigne ou maligne. Les avantages de cette méthode sont nombreux. En effet, la TEP peut permettre de détecter la présence d’anomalies métaboliques évoquant la présence d’une maladie avant même que les changements anatomiques soient visibles par les autres techniques d’imagerie. De plus, l’existence de plusieurs traceurs permet de se focaliser sur le métabolisme que l’on désire étudier (par exemple l’oxygène pour le cerveau ou le glucose pour les tumeurs).
Applications
Historiquement, la TEP était destinée à la neurologie. Dans les faits, la TEP s’est essentiellement développée pour l’oncologie et la cardiologie.
Cancérologie
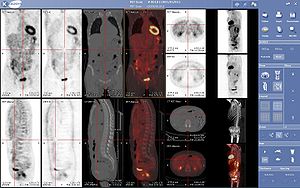
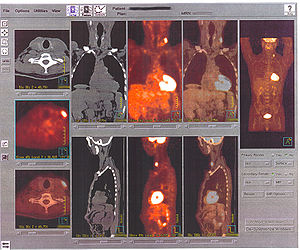 L'appareil TEP peut être couplé avec un scanner (ou CT-scan en anglais) pour obtenir une meilleure localisation anatomique des structures tumorales : ici, un ganglion cervical sus-claviculaire gauche est le siège d'une hyperfixation du FDG. Le scanner couplé permet aussi un gain de temps indéniable pour les calculs d'atténuation nécessaires à une image par TEP de qualité.
L'appareil TEP peut être couplé avec un scanner (ou CT-scan en anglais) pour obtenir une meilleure localisation anatomique des structures tumorales : ici, un ganglion cervical sus-claviculaire gauche est le siège d'une hyperfixation du FDG. Le scanner couplé permet aussi un gain de temps indéniable pour les calculs d'atténuation nécessaires à une image par TEP de qualité.
La TEP associée avec l'injection d'un traceur, ici (18F) le fluorodésoxyglucose (FDG, FDG-PET), est utilisée en cancérologie. Ce traceur est très proche chimiquement du glucose et va donc aller se fixer sur les tissus possédant un métabolisme élevé. Notamment : le cœur, le cerveau et les cellules tumorales. Les cellules tumorales malignes présentent un hypermétabolisme glucidique et une surexpression des transporteurs de glucose (GLUT-1). Le traceur (glucose transformé) ne peut pas subir d’hydrolyse (glycolyse) et il s’accumule donc dans les cellules décrites ci-dessus. C’est pour cela que la TEP est particulièrement bien indiquée dans la recherche des tumeurs malignes.
Cet examen se révèle utile à différentes étapes d’un cancer :
- lors du diagnostic pour l’identification d’une anomalie détectée lors d’un précédent examen (échographie, radiographie) et pour la précision de sa nature (tumeur maligne ou bénigne).
- lors du bilan d’extension pour la précision et la recherche de l’étendue du cancer et d’éventuelles métastases.
- lors du traitement, il permet de juger de l’efficacité d’une thérapie.
- lors de la surveillance pour la détection d’une éventuelle récidive.
Les appareils les plus performants permettent actuellement de détecter des structures tumorales de très petites tailles de l’ordre de 5 mm. La TEP est un outil puissant en oncologie, surpassant en sensibilité et en spécificité (toutes deux supérieures à 90%) les examens de radiologie conventionnels (IRM, scanner X, échographie) dans de nombreux cancers.
On peut citer par exemple, de façon non exhaustive, les lymphomes, les cancers et les nodules pulmonaires, les tumeurs des voies aérodigestives supérieures (bouche, larynx, pharynx), les localisations hépatiques des cancers digestifs, les mélanomes, les cancers du sein (en récidive) ou les cancers gynécologiques comme les principales indications aujourd'hui de la TEP au FDG.
Il est à noter que, du fait de la fixation physiologique du FDG sur le tissu cérébral, la TEP au FDG ne permet en général pas de rechercher les métastases cérébrales.
Imagerie cérébrale et neurologie
Le principe de l'utilisation de la TEP en imagerie cérébrale (neurologie et neurosciences cognitives) repose sur le lien entre activité des neurones dans une région donnée et la mesure de la radioactivité. Ce lien est assez indirect puisqu'au travers de la TEP on mesure l'accumulation d'un radiotraceur. Le radiotraceur le plus couramment utilisé est l'oxygène 15 dont l'accumulation est due à la réponse hémodynamique, c'est-à-dire une augmentation locale du débit sanguin cérébral qui se produit lorsqu'une région du cerveau voit son activité augmenter. L'imagerie cérébrale TEP reflète donc l'apport d'énergie plutôt que l'activité cérébrale proprement dite.
L'avantage de la TEP en imagerie cérébrale tient au fait qu'il est possible d'utiliser des radioligands (traceurs radioactifs) spécifiques de certains neurorécepteurs afin d'étudier des mécanismes très spécifiques de l'activité cérébrale. Ainsi, le radiotraceur raclopride marqué au carbone 11 permet de visualiser l'activité synaptique liée au récepteur D2 de la dopamine. Cette méthodologie fait l'objet de nombreux développements dans le domaine de la neuropsychiatrie.
La TEP est toujours utilisée dans la recherche du fonctionnement des maladies cérébrales dégénératives comme Alzheimer et Parkinson. De récentes études ont tenté de montrer l’intérêt de l’utilisation de la TEP pour un diagnostic précoce de la maladie d’Alzheimer. Il a été observé une réduction du métabolisme au niveau du gyrus cingulaire postérieur que l’on ne retrouve pas dans le vieillissement normal. Cependant, il est nécessaire d’associer à ce résultat d’autres examens (par exemple une IRM pour monter une atrophie de l’hippocampe).
Cardiologie
En cardiologie, la principale indication de la TEP au FDG est la recherche de viabilité du muscle cardiaque après un infarctus[3] : on parle alors de myocarde "hibernant". Cet examen permet de déterminer si les zones du cœur qui souffrent d’une diminution de leur fonction après un infarctus sont viables ou nécrotiques. Une diminution du métabolisme au FDG confirme que le tissu myocardique est non viable alors qu’un métabolisme normal indique sa viabilité et que la fonction cardiaque pourra être améliorée par le rétablissement d’un flux sanguin adéquat grâce à une intervention (pontage coronarien ou angioplastie).
Il existe d'autres traceurs utilisables en cardiologie, notamment le rubidium (82 Rb) (et le 13NH3). Le Rb se comporte comme un analogue du potassium et permet d'étudier la perfusion myocardique avec une efficacité supérieure à celle de la technique "classique" qu'est la scintigraphie myocardique de perfusion. Le couplage de la TEP avec un scanner X (tomodensitométrie) permet une amélioration de la qualité des images par rapport à la scintigraphie (correction d'atténuation voire parfois quantification absolue de la perfusion). De plus, cela laisse entrevoir la possibilité de coupler deux techniques en une : l'angioscanner des coronaires et la TEP de perfusion en un seul examen de moins de 30 minutes. Il est probable que, dans quelques années, ce traceur sera utilisé à côté des techniques de scintigraphie dites "classiques".
Limites
La principale contrainte d’utilisation de la TEP est due à la courte demi-vie des isotopes radioactifs qui nécessitent donc la présence d’un Cyclotron à proximité du centre d’examen. Il existe un certain nombre de causes de faux positifs et de faux négatifs qui peuvent conduire à une mauvaise interprétation de l’examen.
Les faux positifs (examen positif alors qu’absence d’anomalie) sont essentiellement dus à des causes d’inflammation (granulome, anthracose, chirurgie et radiothérapie récentes, fracture récente…) ou d’infection (pneumopathie, tuberculose, ostéomyélite…)
Les faux négatifs (examen négatif alors que présence d’anomalies) sont essentiellement liés à la taille de la lésion (trop petite pour être détectée), à la localisation (proximité d’une région de fixation naturelle : cerveau, cœur, vessie…), à la nature de l’anomalie (certaines tumeurs présentent moins d’avidité au traceur : tumeur mucineuse…), à une glycémie élevée, ou à une chimiothérapie récente de moins de 15 jours.
Avenir de la TEP
L’évolution actuelle de la TEP est le couplage de cette technique d’imagerie fonctionnelle avec le scanner à rayons X (TEP/TDM, PET/CT en anglais) dans le but de permettre un repérage anatomique précis des anomalies métaboliques révélées par la TEP. L’imagerie multimodale est très performante dans la pratique clinique mais tous les services de médecine nucléaire n’en sont pas encore dotés. Cependant, les principaux constructeurs d’équipement médical cherchent d’ores et déjà à développer de nouveaux types d’appareils combinant l’examen IRM et la TEP.
Articles connexes
- Positron
- Imagerie cérébrale
- Tomographie d'émission monophotonique (Single Photon Emission Computed Tomography)
- Imagerie moléculaire
- Master Européen en Imagerie Moléculaire
Notes et références
- ↑ Ter-Pogossian MM, Phelps ME, Hoffman EJ, Mullani NA, A positron-emission transaxial tomograph for nuclear imaging (PETT), Radiology, 1975;114:89–98
- ↑ Pichler PJ, Wehrl HF, Judenhofer MS, Latest advances in molecular imaging instrumentation, J Nucl Med, 2008;49(Suppl 2):5S–23S
- ↑ Bengel FM, Higuchi T, Javadi MS, Lautamäki R, Cardiac positron emission tomography, J Am Coll Cardiol, 2009;54:1-15
Liens externes
- (fr) FAQ petscanonline.
- (en) What is PET?.
- Portail de la médecine
Catégories : Imagerie médicale | Médecine nucléaire | Imagerie en cancérologie | Imagerie cérébrale - lors du diagnostic pour l’identification d’une anomalie détectée lors d’un précédent examen (échographie, radiographie) et pour la précision de sa nature (tumeur maligne ou bénigne).
Wikimedia Foundation. 2010.