- Méthylpropène
-
Isobutène 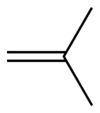
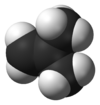
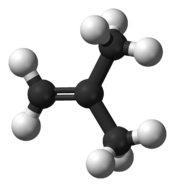
Structure de l'isobutèneGénéral Nom IUPAC 2-méthylpropène Synonymes Isobutène, isobutylène. No CAS No EINECS PubChem SMILES InChI Apparence Gaz incolore Propriétés chimiques Formule brute H2C=C(CH3)2 Masse molaire[1] 56,1063 ± 0,0038 g·mol-1
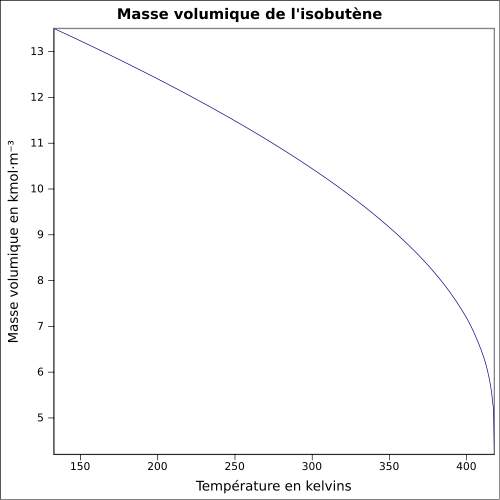
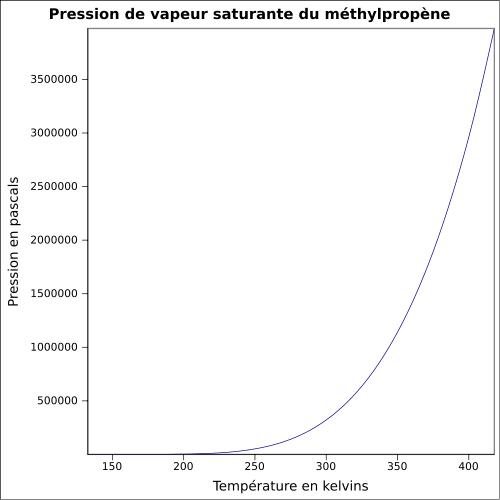
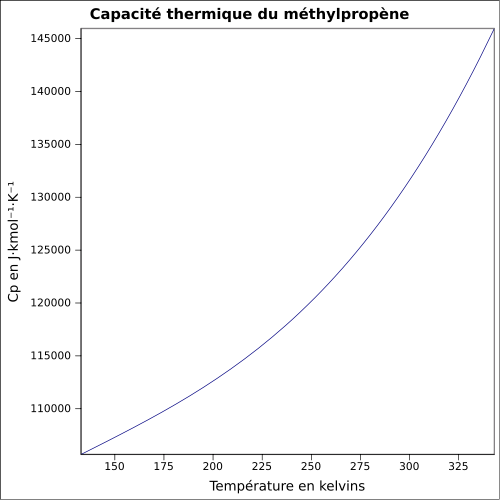
C 85,63 %, H 14,37 %,Propriétés physiques T° ébullition -6,93 °C [2] Masse volumique 626,2 kg·m-3 (liquide) T° d'auto-inflammation 465 °C Point d’éclair Inférieur à -10 °C Pression de vapeur saturante Point critique 4 002 kPa [4], 144,75 °C [2] Thermochimie Cp Unités du SI & CNTP, sauf indication contraire. L'isobutène, également appelé isobutylène (ou 2-méthylpropène selon sa dénomination UICPA), est le composé chimique de formule H2C=C(CH3)2. Il s'agit d'un alcène ramifié à quatre atomes de carbone qui se présente sous forme d'un gaz incolore inflammable aux conditions normales de température et de pression.
Sommaire
Production
L'isobutène peut être isolé à partir de produits de raffinage du pétrole à l'aide d'acide sulfurique H2SO4, mais la principale méthode de production industrielle reste la déshydrogénation catalytique de l'isobutane[5]. La production d'isobutène s'est fortement accrue dans les années 1990 avec l'augmentation de la demande en méthyl tert-butyl éther H3C–O–C(CH3)3 (MTBE).
Une entreprise française implantée dans le Génopole d'Évry (Essonne) a annoncé le 6 octobre 2010 avoir fabriqué des OGM capables de synthétiser de l'isobutène à partir de glucose[6]. Il s'agirait, selon les responsables de cette société, de bactéries équipées d'un matériel enzymatique artificiel développé par génie génétique. Encore au stade de prototype, ce mode de production pourrait s'avérer prometteur s'il venait à être industrialisé.
Applications
L'isobutène est un intermédiaire de synthèse intervenant dans un grand nombre de produits. Il polymérise pour donner du polyisobutène, utilisé notamment comme élastomère et comme additif de lubrifiants. L'hydroxytoluène butylé (BHT) et l'hydroxyanisole butylé (BHA) sont des antioxydants fabriqués à partir d'isobutène par réaction de Friedel-Crafts avec des phénols.
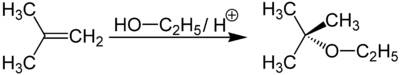
L'isobutène est également à la base de la fabrication des carburants oxygénés avec le méthanol CH3OH et l'éthanol C2H5OH en donnant l'éther méthyle-tertiobutyle H3C–O–C(CH3)3 (MTBE) et l'éther éthyle-tertiobutyle H3C–CH2–O–C(CH3)3 (ETBE) respectivement :
L'alkylation avec le butane donne de l'isooctane, autre additif pour les carburants.
L'isobutène intervient en outre dans la production de méthacroléine H2C=C(CHO)–CH3.
Sécurité
L'isobutène est un gaz hautement inflammable et présente des risques d'explosion. Il est généralement stocké sous forme de gaz comprimé, le risque étant, outre les explosions, qu'il produise une atmosphère asphyxiante s'il est libéré de façon incontrôlée par simple appauvrissement en oxygène.
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) Iwona Owczarek et Krystyna Blazej, « Recommended Critical Temperatures. Part I. Aliphatic Hydrocarbons », dans J. Phys. Chem. Ref. Data, vol. 32, no 4, 4 août 2003, p. 1411 [lien DOI]
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, 1997, 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- (en) Iwona Owczarek et Krystyna Blazej, « Recommended Critical Pressures. Part I. Aliphatic Hydrocarbons », dans J. Phys. Chem. Ref. Data, vol. 35, no 4, 18 septembre 2006, p. 1461 [lien DOI]
- Hydrocarbon Chemistry, George A. Olah et Árpád Molnár, Wiley-Interscience, ISBN 978-0471417828
- (en) DownstreamToday.com – 7 octobre 2010 « French Firm Prototypes Process for Producing Isobutene from Glucose. »
Article lié
- Butène C4H8, dont le méthylpropène est l'un des quatre isomères.
Liens externes
- Encyclopédie Air Liquide : Isobutène
Wikimedia Foundation. 2010.