- 153-94-6
-
Tryptophane
Tryptophane 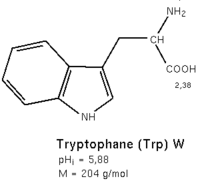
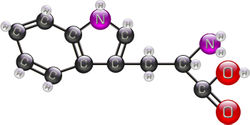
Structure du L-tryptophane Général Nom IUPAC acide (S)-2-amino-3-(1H-indol-3-yl)propanoïque Synonymes W, Trp No CAS (L)
(D)No EINECS (L) Code ATC N06 SMILES InChI Propriétés chimiques Formule brute C11H12N2O2 [Isomères] Masse molaire 204,2252 g∙mol-1
C 64,69 %, H 5,92 %, N 13,72 %, O 15,67 %,Propriétés physiques T° fusion 290,5 °C (décomposition) Propriétés biochimiques Codons UGG Acide aminé essentiel oui Unités du SI & CNTP, sauf indication contraire. Le tryptophane est un acide aminé, qui dans sa configuration lévogyre (L-tryptophane) est l'un des 20 acides aminés constituant des protéines. Dans le code génétique, il est codé par le codon UGG. Il s'agit d'un acide aminé essentiel pour l'homme, c'est-à-dire qu'il doit être apporté par l'alimentation.
Il est aromatique, apolaire et hydrophobe (comme la phénylalanine). Très fragile, il est détruit par les acides minéraux, et ne peut être isolé dans les hydrolysats acides des protéines. C'est un acide aminé contenant un hétérocycle indole qui lui confère de propriétés spectroscopiques d'absorption et de fluorescence dans l'UV. En dehors de son utilisation dans la biosynthèse des protéines, c'est le précurseur d'autres composés importants comme la sérotonine, la mélatonine, la bufoténine, etc.
Dans l'organisme humain, le tryptophane est indispensable et représente environ 1 % des acides aminés présents dans les protéines (le plus rare des 20 acides aminés). Le tryptophane est le précurseur de l’hormone du sommeil, la mélatonine. Certains constituants alimentaires facilitent dans notre organisme la synthèse de sérotonine, neuromédiateur qui régule notre humeur, notre comportement alimentaire et nous prépare au sommeil. Certaines situations physiologiques comme un régime hypocalorique par exemple, peuvent entraîner une baisse de sécrétion de la sérotonine, souvent responsable de stress, de fatigue psychique, de troubles du sommeil. Certains aliments sont riches en tryptophane : œufs, noix de coco, lactosérum ; d'autres en sont pauvres : maïs, carottes, chou.
Dans le cerveau, le tryptophane est hydroxylé par une enzyme et transformé en 5-hydroxytryptophane. Ce 5-HTP est décarboxylé (en présence de vitamine B6) pour donner la sérotonine. Des suppléments de tryptophane et de son métabolite le 5-hydroxytryptophane ou 5-HTP favorisent la sécrétion de sérotonine. Plusieurs études ont établi leur intérêt dans le traitement de la dépression.
En 1989, la compagnie japonaise Showa Denko commercialisa aux États-Unis du tryptophane comme supplément alimentaire produit par manipulation génétique d'une bactérie. On assista alors à une épidémie d’une nouvelle et mystérieuse maladie, le syndrôme éosinophilie-myalgie (EMS, eosinophilia-myalgia syndrome) qui causait des douleurs musculaires[1]. Par la suite, on relia cette maladie à la consommation du tryptophane transgénique, imputable à une mauvaise filtration qui laissait passer un contaminant [2]. Ce tryptophane tua 37 personnes et en rendit 1,500 autres infirmes. Il s'agit d'une véritable catastrophe industrielle liée au premier produit obtenu par manipulation génétique commercialisé .
Sommaire
Voir aussi
Articles connexes
Liens externes
- (fr) Le tryptophane, sur le site du CHU de la Pitié-Salpêtrière
- (en) Tryptophan, sur le site de l'Institut de chimie et biochimie de Berlin
Bibliographie
Notes et références
- ↑ L-tryptophan implicated in human eosinophilia-myalgia syndrome causes fasciitis and perimyositis in the Lewis rat., L J Crofford et al.; J Clin Invest., 1990 , Vol. 86(5), pp. 1757–1763. DOI:10.1172/JCI114902.
- ↑ An Investigation of the Cause of the Eosinophilia-Myalgia Syndrome Associated with Tryptophan Use, Belongia et al.; The New England Journal of Medicine, 1990, Vol. 323(6), pp. 357-365)
Ala | Arg | Asn | Asp | Cys | Glu | Gln | Gly | His | Ile | Leu | Lys | Met | Phe | Pro | Ser | Thr | Trp | Tyr | Val Acide aminé essentiel | Protéine | Peptide | Code génétique - Portail de la biochimie
- Portail de la chimie
Catégories : Acide aminé essentiel | Dérivé de la tryptamine | Composé indolé
Wikimedia Foundation. 2010.