- Glycols
-
Polyol
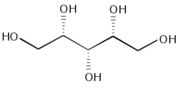 Structure du xylitol, un polyol au goût sucré.
Structure du xylitol, un polyol au goût sucré.
Un polyol ou polyalcool ou glycol est un composé chimique organique caractérisé par un certain nombre de groupes -OH (groupes hydroxyles).
De formule chimique générale ; CnH2n+2On, ils possèdent au moins deux groupements alcool[1].
Sommaire
Toxicologie
Pas d'effet toxique connu pour les polyols. Certains éthers de glycol sont particulièrement toxiques, de même que certaines de leurs métabolites. Ils provoquent cependant des gaz, douleurs abdominales, et ont un effet laxatif lorsqu'ils sont ingérés en trop grande quantité.
Écotoxicologie
Exemples
- Le glycol le plus simple est l'éthylène glycol, de formule chimique CH2OH-CH2OH (c'est un diol).
- Le glycérol ou glycérine (triol).
- L'érythritol (tétraol)
- Le propylène glycol.
- le mannitol
- le sorbitol
- le xylitol
- le maltitol
- le lactitol
- le volemitol (heptol)
(Le maltitol et le lactitol ne sont pas complètement hydrogénés ; il s'agit de monosaccharides combinés à un alcool polyhydrique.)
Le terme est cependant également utilisé pour un certain nombre de polymères que l'on obtient par addition d'oxydes d'alcènes à un sucre par exemple mais aussi du glycérol. Des exemples-type sont l'oxyde de polyéthylène ou polyéthylène glycol (PEG), le polypropylène glycol (PPG) et le polytétraméthylène glycol (PTMG).
Mousses de polyuréthane
Les polyols (notamment le sorbitol) sont utilisés comme base dans l'industrie pour la réalisation des mousses de polyuréthane en y ajoutant de l'isocyanate pour la polymérisation.
Le polyol sert de chaîne de base au polymère, dont les propriété varient selon la longueur de chaîne.
Polyols en tant qu'additifs alimentaires
Nom Pouvoir édulcorant
(saccharose = 1,0)Contenu calorique
(kcal / g)Érythritol 0,7 [1] 0,2 [1] Glycérol 0,6 [3] 4,3 [3] HSH 0,4–0,9 [1] 3,0 [1] Isomalt 0,5 [1] 2,0 [1] Lactitol 0,4 [1] 2,0 [1] Maltitol 0,9 [1] 2,1 [1] Mannitol 0,5 [2] 1,6 [1] Sorbitol 0,6 [1] 2,6 [1] Xylitol 1,0 [2] 2,4 [1] Sources:
[1] (en) Calorie Control Council
[2] (en) Antonio Zamora, "Carbohydrates"
[3] (en) Jeremy Keough, "Glycerol"
Le principal intérêt des polyols pour l'industrie alimentaire réside dans leur utilisation en tant qu'édulcorant de charge à faible valeur calorique. Certains d'entre-eux possèdent une chaleur de dissolution négative, produisant une sensation de froid recherchée dans certaines applications (notamment de confiserie).À l'exception de l'érythritol, au schéma métabolique particulier, la plupart des polyols sont absorbés partiellement au niveau intestinal et influencent donc peu ou pas la glycémie post-prandiale. Le glycérol peut entrer directement dans la voie de la glycolyse via le glycéraldéhyde-3-Phosphate. Ceci explique sa valeur calorique plus élevée.
Le second intérêt des polyols en application alimentaire réside dans leur capacité de liaison de l'eau, permettant un abaissement significatif de l'activité de l'eau. Le glycérol reste le composé le plus efficace du groupe pour cet usage mais, sa chaleur de dissolution positive et son arrière-goût marqué, limite son usage.
Polyols chez les végétaux
Les végétaux ont la faculté de synthétiser leur biomasse à partir des molécules minérales simples (eau, sels minéraux du sol et dioxyde de carbone). Cette autotrophie repose sur un pigment localisé dans le chloroplaste, la chlorophylle qui utilise la lumière comme source d'énergie et la transforme en énergie chimique via la chaîne de la photosynthèse. Lors de la photosynthèse, le dioxyde de carbone atmosphérique absorbé par les stomates des feuilles est combiné à l'hydrogène provenant de la photolyse de l'eau. Cette réaction conduit à un dégagement d'oxygène et à la réduction du gaz carbonique qui se traduit par la formation de trioses phosphates précurseurs du cycle de Calvin dans le chloroplaste. Les trioses phosphates sont transformés en amidon transitoire ou exportés dans le cytosol pour donner le saccharose, forme principale de transport à longue distance du carbone. La nuit, l'amidon est évacué vers le cytoplasme sous forme de glucose pouvant être dégradé par la glycolyse pour fournir de l'énergie à la cellule, ou synthétisé en saccharose. Chez certains végétaux, le rôle de transport à longue distance du carbone est assuré, parallèlement au saccharose, par des tridiholosides dérivant du saccharose par addition d'une ou deux molécules de galactose ou par des polyols comme le mannitol et le sorbitol.
Nature biochimique des polyols
Les polyols sont considérés comme des dérivés d’oses et sont obtenus par la réduction du groupement aldéhyde ou cétone d’un glucide. Les polyols peuvent être classés en deux groupes :
- les alditols ou polyols aliphatiques qui ont une chaîne linéaire d’atomes de carbone
- les cyclitols ou polyols cycliques qui sont des dérivés du cyclohexane.
Suivant la longueur de leur chaîne carbonée, les alditols sont désignés sous le nom de pentitols, hexitols, heptitols, etc. Les alditols les plus courants chez les plantes sont les hexitols (chaîne à six atomes de carbone). Chaque aldose produit un seul alditol dont le nom dérive de cet ose, par exemple mannose donne le mannitol.
Il a été estimé qu’environ 30% de la production primaire de carbone sur terre passait par la synthèse de polyols chez les plantes et chez les algues (Bieleski, 1982). Les polyols sont présents dans l’ensemble du monde végétal et mycélien. Ainsi, chez les champignons, les lichens et beaucoup d’algues marines, les polyols constituent souvent le principal assimilat. Chez les plantes supérieures, 17 alditols ont été identifiés dont 13 chez les angiospermes (LEWIS, 1984). Les plus fréquemment rencontrés sont :
- le galactitol (ou dulcitol), surtout présent chez les Célastracées (fusain)[2], les Scrofulariacées (muflier, digitale) et les Orobanchacées (orobanche)
- le sorbitol, principal produit photosynthétique chez plusieurs espèces de Rosacées ligneuses comme le pommier (Malus), le poirier (Pyrus), le prunier (Prunus)[3].
- le mannitol, présent dans une centaine d’espèces de végétaux supérieurs dont les Rubiacées (caféier), les Oléacées (troène, frêne, olivier) et les Apiacées (céleri, carotte, persil).
Rôles des polyols
Chez les plantes, les rôles physiologiques proposés pour les polyols sont multiples : intervention dans la tolérance aux stress abiotiques et biotiques et forme de transport et de stockage de squelettes carbonés.
Tolérance au stress salin:
Beaucoup de stress environnementaux auxquels les plantes sont soumises semblent conduire à une diminution du potentiel hydrique. Selon les espèces végétales, la sensibilité des plantes et leur réponse aux changements de potentiel hydrique dus à la sécheresse, aux faibles températures ou à une salinité élevée, varient. Cependant, l’un des moyens utilisé par des organismes tels que les champignons, les algues, les végétaux supérieurs pour tolérer ces stress est la synthèse et l’accumulation de composés solubles de faibles poids moléculaires pour augmenter le potentiel osmotique des cellules et maintenir la turgescence. Ces composés sont appelés des solutés compatibles. Ils sont osmotiquement actifs et ils peuvent s’accumuler à de très hautes concentrations dans le cytosol sans pour autant interférer avec le métabolisme cellulaire. Parmi ces composés se trouve le mannitol (polyol acyclique), ainsi que d’autres substances inorganiques (ions) ou organiques (hexoses et certains acides aminés) pouvant également intervenir dans l’ajustement osmotique.
Notes et références de l'article
- ↑ Oilfield Glossary: Term 'glycol'
- ↑ (en) (en) Peter M. Collins, Dictionary of carbohydrates, CRC Press, 2005, 1282 p. (ISBN 0849338298), p. 480-481
- ↑ Escobar Gutiérrez A.J. 1995. Photosynthèse, partition du carbone et métabolisme du sorbitol dans les feuilles adultes de pêcher (Prunus persica (L.) Batsch). Thèse de Doctorat de l'Université de Poitiers, France.
Bibliographie
- BIELESKI R.L., 1982. Sugar alcohols. In Loewus F., Tanner W., Eds. Encyclopedia of Plant Physiology, Vol. 13. Berlin, Springer-Verlag. Pp 158–192.
- LEWIS D.H., 1984. Physiology and metabolism of alditols. In Lewis D.H., ed. Storage Carbohydrates in Vascular Plants. Cambridge, UK, Cambridge University Press. pp 157–179.
Voir aussi
Articles connexes
Liens et documents externes
- Portail de la chimie
Catégories : Édulcorant | Polyol
Wikimedia Foundation. 2010.
