- C5H12N2O2
-
Ornithine
Ornithine 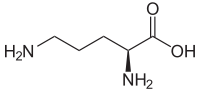
Formule topologique de l'ornithine. Général No CAS No EINECS SMILES InChI Propriétés chimiques Formule brute C5H12N2O2 [Isomères] Masse molaire 132,161 g∙mol-1
C 45,44 %, H 9,15 %, N 21,2 %, O 24,21 %,pKa 1.94 (25 °C) [1] Propriétés physiques T° fusion 140 °C [1] Propriétés biochimiques Acide aminé essentiel dans certains cas Précautions SIMDUT[2] Produit non contrôlé Unités du SI & CNTP, sauf indication contraire. L'ornithine (acide 2,5-diaminopentanoïque) est un acide aminé. Cet acide aminé n'est pas codé par le code génétique. À ce titre, il n'entre pas dans la composition des protéines. C'est l'un des produits de l'action de l'arginase dihydrolase sur la L-arginine pour former l'urée (voir l'article à propos du cycle de l'urée).
L'ornithine peut également avoir un intérêt en microbiologie et en bactériologie. En effet, cette molécule n'est pas un acide aminé, donc n'entre pas dans la constitution d'holoprotéines (qui ne sont constituées que de résidus d'acide aminé). Cela dit, cette molécule peut être dégradée par des bactéries de façon à être utilisée par ces dernières. L'enzyme nécessaire à sa dégradation est l'ornithine décarboxylase donnant la putrescine plus du C02 (acide volatile moins acide que le groupement COOH, aussi appelé groupement carboxylique) ce qui provoque donc une alcalinisation du milieu.
Sachant que, comme dit plus haut, l'ornithine elle-même est synthétisée par l'arginine grâce à l'enzyme argine dihydrolase qui donnent de la putrescine plus du CO2, ce procédé est un peu complexe et emprunte deux voies possibles :
Dans tous les cas l'arginine est hydrolysée une première fois, donnant de la citrulline plus de l'ammoniac (NH3).
Ensuite :
- soit la citrulline est à son tour hydrolysée et donne de l'ornithine, du CO2 et du NH3 ;
- soit il y a action du phosphate inorganique (Pi) qui forme alors de l'ornithine et du carbamyl-phosphate, qui a son tour subit l'action de l'ADP et forme de l'ATP plus du CO2 et du NH3.
Notes et références
- ↑ a et b (en) « Ornithine » sur ChemIDplus, consulté le 11 février 2009
- ↑ « Ornithine (l-) » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
Ala | Arg | Asn | Asp | Cys | Glu | Gln | Gly | His | Ile | Leu | Lys | Met | Phe | Pro | Ser | Thr | Trp | Tyr | Val Acide aminé essentiel | Protéine | Peptide | Code génétique - Portail de la biochimie
- Portail de la chimie
Catégorie : Acide aminé
Wikimedia Foundation. 2010.
