- Bisphénol A
-
Bisphénol A 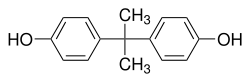
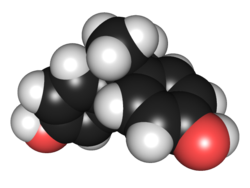
Structure du bisphénol A Général Nom IUPAC 4,4'-dihydroxy-2,2-diphénylpropane No CAS No EINECS SMILES InChI Apparence cristaux blancs[1]. Propriétés chimiques Formule brute C15H16O2 [Isomères] Masse molaire[2] 228,2863 ± 0,0137 g·mol-1
C 78,92 %, H 7,06 %, O 14,02 %,Propriétés physiques T° fusion 152 à 153 °C[1] T° ébullition 360 °C [3] ;
250 à 252 °C (1,7 kPa)[1]Solubilité 300 mg·l-1 (eau) [3] Masse volumique 1,2 g·cm-3[1] T° d'auto-inflammation 600 °C[1] Point d’éclair 207 °C (coupelle ouverte)[1] Pression de vapeur saturante à 190 °C : 87 Pa[1] Thermochimie Cp Précautions Directive 67/548/EEC 
XnPhrases R : 37, 41, 43, 62, Phrases S : (2), 26, 36/37, 39, 46, SIMDUT[5] 
SGH[6] 

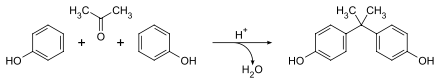
DangerÉcotoxicologie LogP 3,32[1] Unités du SI & CNTP, sauf indication contraire. Le bisphénol A (BPA) est un composé chimique issu de la réaction entre deux équivalents de phénol et un équivalent d'acétone, dont la toxicité sur le corps humain est en débat.
La molécule contient deux groupements fonctionnels phénols et fait partie des composés organiques aromatiques. Ses autres noms sont aussi 4,4'-(propan-2-ylidène)diphénol ou p, p'-isopropylidènebisphénol.
Comme le nonylphénol, le bisphénol A est un perturbateur endocrinien œstrogéno-mimétique[7] capable de se lier au récepteur α des œstrogènes. Son action serait environ 1 000 fois inférieure à celle de l’œstradiol, mais il est très présent dans notre environnement (environ trois millions de tonnes de BPA sont produites chaque année dans le monde[8]) et dans le corps humain.
Le bisphénol est surtout utilisé pour tapisser l'intérieur de certaines boîtes de conserve, de canettes (principales sources d'exposition pour l'homme).
En tant que révélateur de la coloration à l’impression, le Bisphénol A est présent sous forme libre dans un grand nombre de tickets de caisse ou des reçus de cartes de crédit (papier thermique).
Le bisphénol était utilisé pour la fabrication des biberons, ce qui a été interdit pour des raisons sanitaires au Canada et le 23 juin 2010 en France (après proposition du Sénat en mars 2010, dans le cadre du projet de loi Grenelle 2)[9].
En Belgique une proposition de loi (19 mai 2011) a été déposée au Sénat de Belgique visant à interdire le bisphénol A dans les tickets de caisse et reçus de carte de crédit.
Sommaire
Histoire
La première synthèse chimique du bisphénol A est due à A. P. Dianin en 1891. Il a été très étudié dans les années 1930 au cours de la recherche d'œstrogènes de synthèse. Il ne fut jamais utilisé comme œstrogène de synthèse du fait de la découverte à la même époque d'un autre composé de synthèse, le diéthylstilbestrol, dont les propriétés se révélèrent plus intéressantes.
Utilisations
Le bisphénol A est utilisé à l'heure actuelle comme monomère pour la fabrication industrielle par polymérisation de plastiques de type polycarbonate et de résines époxy.
Il est également utilisé comme antioxydant dans les plastifiants et le PVC, et comme inhibiteur de polymérisation dans le PVC.
Le Bisphénol A est présent sous forme libre dans un grand nombre de tickets de caisse (papier thermique).
Les polycarbonates sont très largement utilisés dans des produits de consommation courants depuis les lunettes de soleil et les CD jusqu'aux récipients pour l'eau et la nourriture. En France en 2008, ils sont présents dans 90 % des biberons[10]. On considère qu'ils sont potentiellement responsables de la précocité de l'apparition de la puberté et l'on soupçonne un fort effet sur le développement.
Certains de ces plastiques peuvent être repérés par le chiffre 3 (PVC), 7 (other) ou PC (polycarbonate) au centre ou en dessous du symbole de recyclage (voir Code d'identification des résines).
On note notamment que :
- Certains monomères entrant dans la composition des résines composites d'obturation utilisés pour les soins dentaires sont partiellement constitués de bisphénol A : il s'agit du Bis-GMA (diméthacrylate glycidique de bisphénol A), du Bis-EMA (diméthacrylate d'oxyde éthylène de bisphénol A) et du Bis-DMA (diméthacrylate de bisphénol A)[11]. De par ses liaisons esters, le Bis-GMA n'est pas hydrolysé et ne libère donc pas de bisphénol A, ni le Bis-EMA. Ces deux monomères sont les plus fréquemment utilisés. Seul le Bis-DMA montre des signes d'hydrolysation et de libération de bisphénol A. En revanche, aucune résine composite ne contient directement de bisphénol A.
- Les résines contenant du bisphénol A sont très utilisées comme revêtement intérieur des boîtes de conserves[12].
Environnement et santé
Le bisphénol A est connu pour s'extraire des plastiques spontanément à très faible dose [réf. souhaitée] et plus significativement s'il est nettoyé avec des détergents puissants ou utilisé pour contenir des acides, ou des liquides à hautes températures.
95 % des échantillons d’urine collectés auprès d'adultes américains contenaient des niveaux quantifiables de BPA[13].
Il peut être accumulé dans les tissus gras. La contamination humaine se fait essentiellement par ingestion mais un passage par les voies respiratoires ou la peau est possible.
Selon les récents travaux de "l'Institut National de la Recherche Agronomique (INRA)", le bisphénol A, présent sous forme libre dans un grand nombre de tickets de caisse (papier thermique), pénetre l'organisme humain par la peau. Plusieurs équipes de recherche ont rapporté que les taux résiduels de BPA étaient plus importants dans l'organisme d'hôte(sse)s de caisse[14]. (octobre 2010).
Effets connus ou supposés sur l'environnement
Le Bisphénol A est largement disséminé ; constitutif de nombreux récipients alimentaires en plastique est un xénoestrogène stable et résistant. Or le BPA est un leurre hormonal, capable de « mimer » l’effet des hormones sexuelles féminines qui ont un rôle dans la fonction de reproduction, mais aussi le développement d’organes comme le cerveau ou le système cardio-vasculaire [15].
Massivement produit et dispersé dans l'environnement depuis quelques décennies, il est couramment retrouvé dans l’organisme d’une large majorité de la population, quel que soit l’âge, et notamment chez les enfants[16]. On en trouve maintenant dans presque tous les organismes vivants, ainsi, Park et Choi ont établi le EC50 du BPA à 0,2 mg⋅l−1 et à 3,3 mg⋅l−1 le LC50 pour les larves aquatiques Chironomus tentans[17].
La prévalence du toxique est reconnue importante chez l'homme selon diverses études (93% des urines contiennent du BPA à faible niveau, mais aussi bien davantage de glucuronide, qui est le sous produit de métabolisation, excrété en quelques jours). Le risque d'effets est controversé, car les concentrations corporelles (33-80ng/kg) sont 1 000 fois inférieures à la réglementation EPA/US, mais produisent des effets avérés chez les rongeurs. Or, les rongeurs semblent métaboliser moins le BPA et y être plus sensibles, 10 fois en ordre de grandeur[18]. Les nourrissons sont les plus à risque (leur exposition pouvant être douze fois plus élevée que celle des adultes[réf. nécessaire]).- Données écotoxicologiques consensuelles[19] ; Le bisphénol A est écotoxique[19] (au delà de certaines doses qui varient selon les groupes et les espèces, et par des mécanismes qui pourraient être différents de ceux des autres xéno-oestrogènes[19]). Des études notamment faites sous l'égide de l'Union européenne de 2003 à 2008 dont porté sur les effets du BPA sur divers taxons aquatiques (poissons et mollusques, les plus étudiés), semi-aquatiques (amphibiens) et terrestres (reptiles, crustacés, insectes, vers de terre, oiseaux et plantes[19]). Les animaux les plus étudiés sont les poissons pour lesquels les valeurs de toxicité aiguë vont de 1 à 20 mg/L de BPA chez les vertébrés et invertébrés. Chez les poissons, les concentrations létales 50 mesurées entre 48 et 96 heures sont comprises entre 4,6 et 17,9 mg/L [20].
Effets sanitaires connus ou suspectés
Le degré de toxicité et d'écotoxicité du Bisphénol A, et secondairement la « dose journalière admissible » sont encore discutés[21], et ont surtout été étudiés chez le rat de laboratoire, pour ses effets sur le cerveau[22], sur la reproduction des mâles[23] mais plusieurs indices laissent penser que ce produit pourrait aussi toucher l'organisme humain :
- La Food and drug administration (FDA) qui avait initialement déclaré le BPA sans danger en 2008, est revenu sur son avis, sur la base de nouvelles études concluant à « des effets potentiels sur le cerveau et sur la prostate des bébés et des fœtus ». La FDA a ensuite encouragé l'initiative des industriels américains de ne plus utiliser de BPA dans les contenants d'aliments pour bébés et souhaite que le BPA ne soit plus utilisé dans les revêtements intérieurs de boîtes de conserves[24].
- le 5 février 2010, l'Agence Française de Sécurité Sanitaire des Aliments (Afssa) a rendu un avis sur le bisphénol A[25]. L'Afssa dit constater des « effets subtils » sur le comportement de jeunes rats exposés in utero, ce qui l'incite à « poursuivre son travail d'expertise pour comprendre ces signaux d'alertes ».
Un avis qui ne satisfait absolument pas l'Association Santé Environnement France qui y voient là un symbole du grand écart entre les préoccupations quotidiennes des gens et les abstraites recommandations des agences de l'État Voir leur positionnement de médecins de terrain. - En avril 2010, l'AFSSA a estimé qu'il n'y a « pas de raison de modifier les habitudes alimentaires », mais que « la protection des consommateurs doit être renforcée, et le niveau d'exposition de la population réduit ». L'AFSSA se fonde sur 769 échantillons d'aliments et sodas analysés, ayant montré des teneurs variables, inférieures au seuil de détection jusqu'à 17 microgrammes par kilogramme (µg/kg) d'aliment voire atteignant 128 µg/kg dans les conserves de légumes, poissons et plats cuisinés[26]. Suite à ce travail, l'agence en appelle à une mobilisation de l'industrie (…) pour mettre au point des substituts du BPA pour les usages alimentaires et à une réévaluation des limites de migration spécifique du BPA.
En attendant, l'AFSSA recommande un étiquetage systématique des produits contenant du BPA pour que les consommateurs ne chauffent pas ces produits trop longtemps. La présence de BPA dans les aliments est principalement due à sa migration à partir des matériaux au contact, ce phénomène étant accentué par le chauffage.
- Un avis et un rapport de l'Agence européenne de la sécurité alimentaire (EFSA) sont attendus en mai 2010.
- Des études ont montré (sans que d'éventuels liens de causalité directe soient déjà identifiés et compris) qu'un taux urinaire élevé de ce produit était corrélé avec un risque plus élevé
-
- - de diabète (sur ce point, cela reste discuté[27]),
- - de maladies cardiovasculaires[28]
- - d'anomalies du bilan hépatique[29].
- - de moindre efficacité de chimiothérapies chez les patients cancéreux[réf. nécessaire].
- Parmi les effets attendus et mieux compris ; en tant que perturbateur hormonal[30], il s'est montré capable d'affecter la reproduction d'animaux de laboratoire et il pourrait être un des nombreux facteurs de délétion de la spermatogenèse chez l'homme.
- Chez le lapin, à faible dose (1 picogramme), il peut inhiber l'érection du pénis suite à des modifications des tissus du corps caverneux. Plus la dose de BPA est importante, plus les tissus sont dégradés par augmentation de collagène fibreux, dépôts de graisse, hyperplasie et fibrose[31].
- La souris de laboratoire CD1, exposée in utero à de faibles doses de BPA, accouche de mâles présentant une prostate plus lourde et un épididyme diminué, alors que les femelles présenteront des altérations du développement des glandes mammaires[32].
- 10 μg/kg/jour (taux proches des valeurs d’exposition actuelles d'une femme enceinte) suffisent pour induire chez la souris des anomalies de développement de la prostate fœtale (ce qui rend plausible un risque accru de cancer ultérieur[33].)
- Effets sur le système reproducteur mâle ; Selon l'ANSES[19] les conclusions épidémiologiques diffèrent (mais sur la base d'études ayant porté sur des échantillonnages différentes (hommes féconds et inféconds). Par contre, le BA est facteur reconnu de délétion de la spermatogenèse après 5 semaines d'exposition au BPA chez l'animal selon deux études aux résultats convergents[34],[35]. L'impact d'une exposition prénatale, néonatale et post-natale (lactation) sont encore controversés chez l'animal. Pour la période pubertaire, on suspecte une moindre production de testostérone et modification de l’activité sexuelle[19].
- Effets du BPA sur le système reproducteur féminin(dont sur l'endomètre, les ovaires polykystiques ou comme facteur de fausse-couches et prématurité) Peu d’études sont disponibles et sont selon l'Ansees[19] méthodologiquement limitées (faible échantillonnage au sein de la population, participants choisis, manque d'analyse statistique fine,…dans un contexte de confusions possibles. Les données disponibles ne permettent pas de conclure avec certitude d'un impacts chez la femme), mais le BPA semble affecter la maturation ovocytaire dans la procréation médicalement assistée selon une étude[36] de bonne qualité et une autre étude[37] présentant des limites méthodologiques « non majeures ». Plusieurs impacts sont par contre « avérés chez l’animal » en exposition prénatale, comme post-natale :
- Augmentation de la survenue de kyste des ovaires [19];
- Modifications hyperplasiques de l'endomètre ;
- puberté avancée (pour une exposition pré et post-natales précoce) ;
Plusieurs études d'exposition in utero ou post-natale précoce ont montré (effet avéré) une perturbation hormonale hypothalamo-hypophysaire gonadotrope avec variations des taux d’hormones sexuelles, perturbation de l'expression des récepteurs des hormones sexuelles.
Chez l’animal adulte, des effets sont observés (dont remaniement histologique de la paroi utérine, changement morphologique du tractus génital), mais à des doses bien supérieures au NOAEL retenue par l'EFSA[19].
- Effets sur le cerveau et le comportement ; on suspecte des effets sur la neurogenèse, le « dimorphisme sexuel comportemental », l'anxiété et le comportement exploratoire et (chez l'animal) sur une altération du comportement maternel. Ils ne peuvent être démontré chez l'être humain faute de données, mais plusieurs études sur l'animal ont montré un effet sur le développement neurologique en cas d'exposition in utéro ou périnatale. Des anomalies de neurodifférenciation et des systèmes aminergique et glutamatergique NMDA sont observées[19]. Le BPA affecte aussi dans ce cas les récepteurs oestrogènes (ERα et ERß), et le nombre de neurones sensibles à l'ocytocine et à la sérotonine. Dans le cerveau, l'hypothalamus (et en son sein des régions impliquées dans le dimorphisme sexuel) semble le plus affecté. Dans l'hippocampe (lié aux activités cognitives et à l'anxiété), les zones associées aux récepteurs NMDA sont également modifiées. Ces résultats sont néanmoins controversé car des études faite avec des niveaux d'exposition différents, concluant selon les cas, à un non-effet[38]., un effet anxiogène[39] ., 2010; Poimenova et al., 2010) ou à un effet anxiolytique[40].
- Effets sur le métabolisme lipidique, glucidique et le système cardio-vasculaire ; ils sont suspectés chez l'Homme suite à une étude transversale (Melzer et al., 2010) ayant mis en évidence une corrélation entre problèmes cardiovasculaires (corronariens et diabète) et teneurs urinaires en BPA[19].
L'exposition de rongeurs au BPA (in utero ou chez l'adulte) affecte le métabolisme du foie, des tissus adipeux et du pancréas, avec selon certains auteurs des « changements dans l'expression des gènes codant pour des protéines intervenant dans les voies de signalisation cellulaire impliquées dans la lipogenèse et le métabolisme glucidique »[19]. In vivo, la lipogenèse semble affectée, de même qu' in vitro. Des effets sur le métabolisme des glucide ont été signalés suite à exposition prénatale et périnatale au BPA, mais avec une mauvaise répétabilité des expériences (cet effet reste donc controversé). Par contre, chez l'animal toujours, le BPA, in vivo et in vitro augmente - de manière avérée - la lipémie et le risque de surcharge pondérale en activant la lipogenèse, avec un effet avéré de l'exposition prénatale et périnatale ou chez l’adulte[19]. - Effets thyroïdiens ; Chez les amphibiens, in vitro, la métamorphose se montre affecté - de manière avérée - selon l'Anses par le BPA qui est alors antagoniste des hormones thyroïdiennes, probablement en augmentant le recrutement de corépresseurs des récepteurs des HT, mais les autres données disponibles en 2010 ne permettent ni de confirmer ni d'infirmer un tel rôle chez l'Homme ou les mammifères (aux doses auxquelles nous sommes exposés)[19].
Les rongeurs, en laboratoire présentent un effet du BPA sur le fonctionnement thyroïdien quand l'exposition se fait durant la maturation finale de l'axe hypothalamo-hypophyso-thyroïdien[19]. - Effets sur le système immunitaire Le BPA est un sensibilisant cutané de catégorie B[41],[19], associé à une production d'anticorps anti-cytomégalovirus, mais sans que l'on puisse à ce jour évaluer l'importance de cette réaction ou ses conséquences immunitaires. Le BPA suscite chez l'animal une production de lymphocytes T et une surproduction avérée de cytokines, avec un déplacement de la réponse immunitaire observée en faveur des Th2, sans que l'on puisse extrapoler de conséquences pour l'Homme[19].
- Effets sur l'intestin ; En 2010, il ne semblaient pas avoir jamais été étudiés chez l'être humain, mais l'animal adulte exposé à de fortes doses de BPA y réagit comme avec l'oestradiol, probablement via une action sur les récepteurs aux estrogènes[19]. Le BPA a eu chez des animaux nés de mères traitées, un effet pro-inflammatoire dans la descendance femelle (évoquant un manque de maturation du système immunitaire). Le BPA pourrait avoir un effet d'inflammation de l'intestin et modifier la perméabilité intestinale (effet suspecté, sur la base d'une seule étude chez l’animal)[19].
- Effets sur la prostate (développement et cancérogénicité) ; il n'a pas été épidémiologiquement étudié chez l'Homme. Chez les murins, même sur plusieurs générations (de souris et rats), le poids la prostate ne semble pas affecté[42],[43] par le BPA chez l'adulte, mais augmente en poids (avec hyperplasie dans les cas où des coupes histologiques ont été faites) (Chitra et al., 2003; Herath et al., 2004) s'il y a eu exposition prénatale chez la souris (Nagel et al., 1997 ) . L'exposition néonatale (rongeurs) a produit des lésions de type PIN, mais pas d'adénocarcinome de la prostate[19]. Les effets sur la prostate, suspectés chez l'animal, restent donc controversés chez l'homme[19].
- Effets sur le sein : cancérogénicité ; Les données disponibles sont récentes (post-2000) et en évolution, avec une seule étude épidémiologique chez l'homme, qui comprend des limites méthodologiques selon l'Ances. Par contre chez l'animal, un effet avéré est une accélération de la maturation de la glande mammaire à l'âge adulte après exposition prénatale ou périnatale au BPA[19]. On observe aussi des lésions hyperplasiques intracanalaires (si exposition périnatale ou prénatale), des lésions de type néoplasique dites CIS ou carcinomes intracanalaires (si exposition périnatale au BPA) chez des animaux exposés au BPA. Un risque accru de développer ultérieurement des tumeurs mammaires est suspecté en cas de co-expositions avec un agent cancérogène) s'il y a eu exposition prénatale ou périnatale au BPA[19]
Risque In utero
Le placenta ne protège pas l'embryon de l'exposition au bisphénol A.
- Un passage transplacentaire significatif du BPA (4 % d’une dose de 20 μg/kg donnée à la mère) est avéré chez la souris[44]. Chez l'humain, il augmente le poids du bébé à la naissance[45]. L'inserm a publié en 2010 une expertise collective sur ses effets[46]. Il n'aurait pas d'effets neurologiques sur le développement[47]
Historique de la connaissance
Les premières études sur l'action œstrogénique du bisphénol A datent des années 1930 où il fut administré à des rates ayant subi une ablation des ovaires. Une action en tant qu'androgène fut rapidement fortement suspectée[48]. Ces effets pourraient entraîner des problèmes de santé chez l'homme, tels qu'une diminution du taux ou de la qualité des spermatozoïdes. Le bisphénol A peut causer des anomalies de fonctionnement d'autres organes, comme le pancréas[49] ou la thyroïde[50].
L'industrie du plastique a longtemps affirmé que le bisphénol A était sans danger pour l'homme, minimisant ou réfutant les tests donnant des résultats contraires. Onze études effectuées par des industriels ne mettaient aucun risque en évidence tandis que, d'après un rapport de Frederick vom Saal et Claude Hughes, 90 % des 104 études indépendantes montrent un risque possible[51]. Un rapport précédent rendu public par le Centre pour l'analyse des risques de l'Université Harvard[réf. nécessaire] et financé par le Groupement américain du plastique qualifiait le risque de « faible » et « non significatif ». Claude Hughes considère dans le rapport de 2004 que cette publication du Centre pour l'analyse des risques n'est pas fiable parce qu'elle ne prend en compte que peu de travaux publiés depuis 2001 sur l'effet des faibles doses de BPA sur la santé.
En 2005, l'équipe de S.M Belcher démontrait que de faibles taux de bisphénol-A peuvent entraîner une altération du développement du fœtus chez le rat[52].
En 2006, vom Saal et Welshons[53] ont publié une analyse détaillée expliquant pourquoi certaines études, principalement menées par des laboratoires financés par l'industrie, n'obtenaient pas des résultats reproductibles sur les effets à faible dose du bisphénol-A. Un comité scientifique indépendant a réanalysé les données du rapport pour le compte d'une agence du gouvernement américain et a montré qu'en réalité un effet existe en dépit des conclusions opposées du rapport originel[réf. nécessaire].
En décembre 2009, une étude française réalisée par des chercheurs de l'INRA conclut pour la première fois que l’exposition au Bisphénol A (BPA) a des conséquences sur la fonction intestinale chez le rat. L'étude démontre que l’appareil digestif du rat est très sensible aux faibles doses de BPA, affectant la perméabilité intestinale, la douleur viscérale et la réponse immunitaire à l’inflammation digestive. Les effets du BPA sur l’intestin s'observent dès une dose dix fois inférieure à la dose journalière admissible pourtant considérée comme très sécuritaire pour l’homme. Cette étude montre également que l’exposition pré- et post-natale de ces animaux peut fragiliser la fonction de « barrière intestinale » à l’âge adulte[54].
La position des organismes officiels de sécurité sanitaire
En 2007, l'Autorité européenne de sécurité des aliments (EFSA) notait en conclusion de son rapport sur le Bisphénol A, sa présence dans les canalisations de transport de l'eau potable et les conteneurs. Elle préconisait que des études soient menées sur la possible propagation de cette substance dans l'eau. L’EFSA fixa alors la dose journalière admissible (DJA) à 0,05 milligramme/kg (= 50µg/kg) de poids corporel pour cette substance[55], taux retenu par l'Agence française de sécurité sanitaire de l'alimentation, de l'environnement et du travail (Anses).
Une enquête récente a détecté des traces de bisphénol A dans les urines de 91% des Canadiens, à raison en moyenne de 1,16 μg par litre d'urine, soit un taux proche de ceux relevés (concentrations moyennes ou médianes) ailleurs allant de 1 à 3 μg·l-1. Au Canada toujours, les 12-19 ans sont plus touchés (1,5 μg en moy.), alors que les taux les plus faibles sont détectés chez les plus de 60 ans (0,9 μg en moye). Selon l'Agence française de sécurité sanitaire de l'alimentation, de l'environnement et du travail (Anses) il serait en France d'environ 1 μg·l-1.
Depuis le 18 avril 2008, Santé Canada, l'office public de santé du Canada, a classé le bisphénol A au rang de substance dangereuse[56]. Le Canada a été ainsi le premier pays à classer au rang des toxiques cette substance, ce qui doit amener États-Unis et Union européenne à se prononcer. Le produit a ainsi été interdit dans certains États américains (Chicago, Minnesota, Connecticut et Suffolk County[57]), tandis que les sénateurs Dianne Feinstein (dém., Calif.), Charles E. Schumer (dém., N.Y.) et Edward J. Markey (rép.) ont déposé une proposition de loi visant à son interdiction pour tout contenant de boisson[57].Le 15 août 2008, un rapport de la Food and Drug Administration (FDA) aux États-Unis concluait que ce produit ne posait pas de problème de santé humaine aux niveaux d'exposition habituels pour l'homme; ce constat n'est pas partagé par de nombreux scientifiques, y compris au sein d'un groupe consultatif de la FDA qui accuse l'agence de ne retenir que les arguments avancés par les études financées par l'industrie du plastique et d'ignorer une centaine d'études [57], créant « un faux sentiment de sécurité », alors que d'autres rapports ou études alertent sur les risques liés à ce produit. L'agence s'est engagée à réétudier la question[58], ce qui l'a amené à renverser partiellement sa position: si elle n'a pas interdit le Bisphénol A, ni contraint les producteurs à afficher la présence de Bisphénol sur les étiquettes (ce dernier étant classé « additif alimentaire ») faute, dit-elle, de preuves suffisantes, elle conseille le public de minimiser son exposition à ce produit[57]. Ayant lancé une enquête dotée d'un budget de 30 millions de dollars sur deux ans pour étudier le Bisphénol[57], elle souligne que 90% de la population américaine présente des traces de bisphénol dans son urine[57] et se déclare particulièrement soucieuse des effets du Bisphénol sur les fœtus, les bébés et les jeunes enfants[57]. L'industrie du bisphénol produit plus de 6 millions de tonnes par an de ce produit[57].
Le 30 septembre 2010, l'Agence européenne de sécurité des aliments rend un avis concluant qu'il n'existe aucune nouvelle preuve les amenant à reconsidérer la DJA fixée à 0,05 mg/kg de poids corporel et considère qu'il n'est pas dangereux pour la santé[59], mais l'ANSES (Agence nationale de sécurité sanitaire alimentation, environnement, travail) en France considère que cette référence n'est plus fiable[60].
En 2011, l'Anses a publié deux rapports ; le premier sur les effets sanitaires du bisphénol A, et le second sur ses usages[61], avant de lancer un appel à contributions, pour recueillir des commentaires sur le contenu et les pistes de ses travaux et pour recevoir toute donnée scientifique concernant, notamment, les produits de substitution disponibles ou des données relatives à leur innocuité et efficacité[62].
Bisphénol A et biberons
En 2008, le bisphénol A était très présent dans les plastiques alimentaires et notamment dans les polycarbonate s, dans 90 % des biberons qui peuvent en relarguer des quantités significatives dans les aliments ainsi donnés aux bébés[63],[64]. Face aux risques médiatisés cette année, certains fabricants de biberons (Dodie ; Avent du groupe Philips) ont décidé la même année de fabriquer des biberons sans BPA mais commercialisés plus chers[65]. Ceux-ci ont également publié des questions/réponses sur leurs sites Internet pour rassurer les clients et leur donner leurs avis sur le bisphénol A et leurs recommandations d'utilisation des biberons actuels (notamment la « chauffe »[66].)
Le 17 octobre 2008, le Canada est devenu le premier pays dans le monde à interdire les biberons contenant du bisphénol A[67]. La France les a interdit deux ans après, en 2010 dans le cadre du projet de loi Grenelle 2.
En France, dans un communiqué du 13 novembre 2008, l'Agence française de sécurité sanitaire des aliments (Afssa) s'est alignée sur les conclusions de l'Autorité européenne de sécurité des aliments (AESA) selon lesquelles l'exposition des nourrissons au bisphénol A est largement inférieure à la dose journalière tolérable (DJT) et ce, même en cas de chauffage au micro-ondes[68]. Quelques jours plus tard, le Canard enchaîné dénonçait un conflit d'intérêt en faisant remarquer que de nombreux membres du comité d'experts de l'Afssa étaient également employés par l'industrie du plastique[69].
Début 2009, la polémique enfle. En France, le Réseau environnement santé (RES), qui regroupe associations, ONG et scientifiques, demande aussi « l'interdiction du BPA dans les plastiques alimentaires ». Aux États-Unis comme en France, un certain nombre de fabricants annoncent qu'ils proposent ou vont proposer des biberons « garantis sans bisphénol A[70]. »
Les endocrinologues constatent une augmentation des problèmes testiculaires chez les garçons, de l'obésité précoce et une avancée de l'âge de puberté des filles (par exemple, selon une étude publiée en 2010, ayant porté sur 1239 jeunes filles de 3 régions des États-Unis, 15 % d'entre elles ont entamé leur puberté vers 7 ans, et 20 % avaient de premiers poils pubiens dès 8 ans, ce qui confirme des résultats danois montrant que la formation des seins est de plus en plus précoce chez les jeunes européennes[71]. Des variations ethniques ou régionales sont constatées, qui pourraient être liées à l'alimentation et éventuellement à l'exposition au Bisphénol A ou à d'autres facteurs environnementaux[72].
Lors de son colloque annuel (10 juin 2009), la Société internationale d'endocrinologie a de nouveau alerté sur cette question (effet perturbateur endocrinien sur la reproduction, implications dans les cancers du sein et de la prostate, dans certaines pathologies cardiovasculaires, de la thyroïde et l’obésité). Elle a appelé à réduire l’exposition de la population à ces molécules, au nom du principe de précaution. Elle a publié une « déclaration scientifique » [73],[74] dans la revue Endocrine Reviews. La déclaration juge le problème préoccupant, et appelle à renforcer la recherche.Le 5 février 2010, l'Agence française de sécurité sanitaire des aliments a rendu son avis sur le bisphénol A[25]. L'Afssa dit « constater des « effets subtils » sur de jeunes rats, ce qui l'incite à poursuivre son travail d'expertise pour comprendre ces signaux d'alertes ». Elle conseille donc de ne pas « chauffer trop fort » les aliments ou biberons au micro-ondes. Une recommandation qui ne satisfait pas du tous les médecins de l'Association Santé Environnement France, qui disent ne pas savoir ce que « chauffer trop fort veut dire »[75]. Dans le doute, les médecins de l'association appellent à prendre quelques précautions simples, notamment préférer l'utilisation de biberons en verre incassable ou en plastique sans BPA.
Le 23 juin 2010, le Parlement interdit la fabrication et la commercialisation de biberons contenant du bisphénol A[76].
Méthodes analytiques
Plusieurs méthodes de dosage de BPA dans l’eau existent.
Parmi ces méthodes, l’une des plus utilisées est la SPE/GC, SPE/LC avec différents types de détection comme l’UV, la fluorescence, etc. Bien que donnant une bonne limite de détection, les désavantages de cette technique, tels que sa lenteur et sa grande consommation de solvant, ont entraîné la mise au point de plusieurs autres techniques.
La technique de la SPME espace tête pour détecter le BPA dans l'eau est la plus utilisée actuellement. Elle se déroule comme suit: 5 ml d’échantillon sont prélevés et filtrés avec un filtre fibre de verre de 0,45 μm de diamètre. Cet échantillon est introduit dans une fiole de 20 ml contenant 20 du NaCl 20 % (poids/volume). On ajoute ensuite 50µL de méthanol contenant 4 mg·l-1 de BPA d4 comme étalon interne. On ajoute ensuite 200 µl d’anhydride acétique puis la fiole est immédiatement scellée. Après 5 minutes de dérivatisation, 100 μm d’une fibre de type PDMS sont introduits dans l’espace tête pendant 30 minutes et à 100 °C avec une agitation de 500 tours par minute. Cette fibre adsorbe les analytes d’intérêt dans la phase gazeuse située au-dessus de la matrice. Ces analytes concentrés sont par la suite désorbés dans l’injecteur d'un chromatogramme en phase gazeuse à 280 °C pendant 5 minutes[77].
La SPME espace tête/LC/MS/MS a été appliquée par Santé Canada pour détecter le BPA dans l’eau embouteillée.
Notes et références
- BISPHENOL A, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Entrée de « 4,4'-Isopropylidenediphenol » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 4 juillet 2009 (JavaScript nécessaire)
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 3, Huston, Texas, Gulf Pub. Co. (ISBN 0-88415-859-4)
- « Bisphénol A » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- Le Bisphénol A (BPA) et les biberons ?, article scientifique École Normale Supérieure - DGESCO.
- « Le concept de perturbation endocrinienne et la santé humaine », Médecine/sciences ; février 2007 ; volume 23 ; n° 2 ; Voir.
- Le Parlement interdit l'utilisation des biberons au bisphénol A, Le Monde. Mis en ligne le 23 juin 2010, consulté le 23 juin 2010
- Le Nouvel Observateur, 25 septembre 2008.
- Polydorou O, König A, Hellwig E, Kümmerer K. Long-term release of monomers from modern dental-composite materials. Eur J Oral Sci. 2009 Feb;117(1):68-75.
- http://www.afssa.fr/Documents/MCDA2007sa0312.pdf : Avis de l’Agence française de sécurité sanitaire des aliments relatifs à l’inertie et à l’innocuité chimique des Matériaux aux Contacts des Denrées Alimentaires (MCDA) issus des résines (exemple n°1)
- Calafat AM, Kuklenyik Z, Reidy JA, et al. Urinary concentrations of bisphenol A and 4-nonylphenol in a human reference population. Environ Health Perspect 2005 ; 113 : 391-5.
- Le Bisphénol A pénétrerait l’organisme par la peau.
- Impact of oral Bisphenol A at reference doses on intestinal barrier function and sex differences after perinatal exposure in rats. Braniste V., Jouault A., Gaultier E., Polizzi A., Buisson-Brenac C., Leveque M., Martin P.G., Theodorou V., Fioramonti J., Houdeau E. PNAS. 2010 Jan 107:1 448-453. (publiée en ligne le 14 décembre 2009)
- Becker K., Göen T., Seiwert M., Conrad A., Pick-Fuß H., Müller J., Wittassek M., Schulz C., Kolossa-Gehring M.(2009). GerES IV:Phthalate metabolites and bisphenol A in urine of German children, Int. J. Hyg. Environ. Health 212: 685–692.
- Sun Young Park and Jinhee Choi, Cytotoxicity, genotoxicity and ecotoxicity assay using human cell and environmental species for the screening of the risk from pollutant exposure Environment International volume 33, Issue 6, 2007 {{{1}}}817-822.
- http://www.scientificamerican.com/article.cfm?id=plastic-not-fantastic-with-bisphenol-a Article Scientific America, 2008
- Anses, Rapport d’expertise collective Saisines « 2009-SA-0331 » et « 2010-SA-0197 » : Effets sanitaires du BPA, 2011
- Voir Tableau XVI de l'étude Anses 2011 citée en notes de bas de page
- Beronius A., Ruden C., Hakansson H., Hanberg A., (2009). Risk to all or none? A comparative analysis in the health risk assessment of bisphenol A, Reprod. Toxicol., accepted manuscript, doi:10.1016/j.reprotox.2009.11.007.
- American Chemistry Council (2009). DNT study: A dietary developmental neurotoxicity study of bisphenol in rats, WIL- 186056, September 2009, 4796p.
- Aydogan M., Korkmaz A., Barlas N., Kolankaya D., (2009) Pro-oxidant effect of vitamin C coadministration with bisphenol A, nonylphenol, and octylphenol on the reproductive tract of male rats. Drug Chem Toxicol. 1-11. doi: 10.3109/01480540903286468
- Bisphénol A: l'agence sanitaire admet pour la 1ère fois des « signaux d'alerte » (Dépêche AFP du 5 février 2010)
- http://www.afssa.fr/Documents/MCDA2009sa0270.pdf
- Source : Marc Mortureux, directeur général de l'Afssa), lors d'un point sur l'évaluation en cours de l'exposition des consommateurs au Bisphénol A.
- Ning G, Bi Y, Wang T et al. Relationship of urinary bisphenol A concentration to risk for prevalent type 2 diabetes in chinese adults: A cross-sectional analysis, Ann Intern Med, 2011:155:368-374
- Melzer D, Rice NE, Lewis C, Henley WE, Galloway TS, 2010 Association of Urinary Bisphenol A Concentration with Heart Disease: Evidence from NHANES 2003/06. PLoS ONE 5(1): e8673. doi:10.1371/journal.pone.0008673 Résumé de l'étude et sources
- Lang IA, Galloway TS, Scarlett A et Als. Association of urinary bisphenol A concentration with medical disorders and laboratory abnormalities in adults, JAMA, 2008;300:1303-1310.
- Beronius A., Ruden C., Hanberg A., Hakansson H., (2009). Health risk assessment procedures of endocrine disrupting compounds within different regulatory frameworks in the European Union. Regul Toxicol Pharmacol. 55(2):111-22.
- DG Moon, HS Park, JB Choi, YS Kim, JJ Kim, Bisphenol a inhibits penile erection via alteration of penile histology in the rabbit Department of Urology, Korea University, Seoul, Korea ([PDF]Résumé / Voir page 33/39 paragraphe P5/6 – 128) 3 groupes de lapins de laboratoire mâles (un 4e groupe servant de témoin) ont été exposés durant 8 semaines à 3 doses différentes de Bisphénol A (BPA) ; 1 µg/kg, 1 nanogramme/kg, et 1 picogramme/kg. Les échantillons de tissu caverneux du pénis ont été récoltés pour les études pharmacologiques et histologiques. Dans tous les groupes traités, le tissu caverneux ne réagissait pas normalement aux tests par rapport aux témoins (p <0,01) et ce d'une manière dépendante de la dose. Le BPA a entraîné la dysfonction érectile par altération du pénis, même à une dose de l'ordre du picogramme.
- Markey CM, Luque EH, Munoz de Toro MM, et al. « In utero exposure to bisphenol A alters the development and tissue organization of the mouse mammary gland ». Biol Reprod 2001 ; 65 : 1215-23.
- Timms BG, Howdeshell KL, Barton L, et al. « Œstrogenic chemicals in plastic and oral contraceptives disrupt development of the fetal mouse prostate and urethra ». Proc Natl Acad Sci États-Unis 2005 ; 102 : 7014-9.
- Chitra KC, Latchoumycandane C, Mathur PP. Induction of oxidative stress by bisphenol A in the epididymal sperm of rats. Toxicology. 2003 Mar 14;185(1-2):119-127
- Herath CB, Jin W, Watanabe G, Arai K, Suzuki AK, Taya K. Adverse effects of environmental toxicants, octylphenol and bisphenol A, on male reproductive functions in pubertal rats. Endocrine 2004 Nov;25(2):163- 172.
- Mok-Lin E, Ehrlich S, Williams P., Petrozza J, Wright DL, Calafat AM, Ye X, Hauser R. Urinary bisphenol A concentrations and ovarian response among women undergoing IVF. Int J Andro. 2010 Apr; 33(2):385-393
- Fujimoto VY, Kim D, vom Saal FS, Lamb JD, Taylor JA, Bloom MS. Serum unconjugated bisphenol A concentrations in women may adversely influence oocyte quality during in vitro fertilization Fertil Steril. 2011 Apr;95(5):1816-9.
- Stump DG, Beck MJ, Radovsky A, Garman RH, Freshwater LL, Sheets LP, Marty MS, Waechter JM, Jr.,Dimond SS, Van Miller JP, Shiotsuka RN, Beyer D, Chappelle AH, Hentges SG (2010) Developmentalneurotoxicity study of dietary bisphenol A in Sprague-Dawley rats. Toxicological Sciences 115, 167-182
- Cox KH, Gatewood JD, Howeth C, Rissman EF (2010) Gestational exposure to bisphenol A and crossfostering affect behaviors in juvenile mice. Hormones and Behavior 58, 754-761
- Tian YH, Baek JH, Lee SY, Jang CG (2010) Prenatal and postnatal exposure to bisphenol a induces anxiolytic behaviors and cognitive deficits in mice. Synapse 64, 432-439
- catégorie B : solid-based indication for contact allergenic effects because of less frequency proven contact allergenic effet in humans taking into account existing positive animal data) (Schlede et al., 2003).
- Tyl RW, Myers CB, Marr MC, Thomas BF, Keimowitz AR, Brine DR, Veselica MM, Fail PA, Chang TY, Seely JC, Joiner RL, Butala JH, Dimond SS, Cagen SZ, Shiotsuka RN, Stropp GD, Waechter JM (2002) Threegeneration reproductive toxicity study of dietary bisphenol A in CD Sprague-Dawley rats. Toxicological Sciences 68, 121-146.
- Tyl RW, Myers CB, Marr MC, Sloan CS, Castillo NP, Veselica MM, Seely JC, Dimond SS, Van Miller JP, Shiotsuka RN, Beyer D, Hentges SG, Waechter JM (2008) Two-generation reproductive toxicity study of dietary bisphenol a in CD-1 (Swiss) mice. Toxicological Sciences 104, 362-384.
- Zalko D, Soto AM, Dolo L, et al. « Biotransformations of bisphenol A in a mammalian model: answers and new questions raised by low-dose metabolic fate studies in pregnant CD1 mice ». Environ Health Perspect 2003 ; 111 : 309-19.
- Article intitulé Lebisphénol A augmente le poids de naissance des bébés LE FIGARO 12/09/11
- INSERM >BisphénolA : Effets sur la reproduction - Une expertise collective del’Inserm, 03/06/10
- BFR 29/07/10 BisphenolA : Studies ( Stump et al. (2010) and Ryan et al. (2010)) provideno indications fo r adverse effects on neurological development and behaviour (BfR Opinion Nr. 035/2010 of 2010-07-29)
- Takeuchi T, Tsutsumi O, Ikezuki Y, Takai Y, Taketani Y, Positive relationship between androgen and the endocrine disruptor, bisphenol A, in normal women and women with ovarian dysfunction, Endocr J, 2004;51:165-169.
- Ropero AB, Alonso-Magdalena P, Garcia-Garcia E, Ripoll C, Fuentes E, Nadal A, Bisphenol-A disruption of the endocrine pancreas and blood glucose homeostasis, Int J Androl, 2008;31(2):194-200.
- Moriyama K, Tagami T, Akamizu T et als. Thyroid hormone action is disrupted by bisphenol A as an antagonist, J Clin Endocrinol Metab, 2002;87:5185-5190.
- vom Saal FS, Hughes C. An extensive new literature concerning low-dose effects of bisphenol A shows the need for a new risk assessment, Environ Health Perspect, 2005;113:926-33.
- Le HH, Carlson EM, Chua JP, Belcher SM. Bisphenol A is released from polycarbonate drinking bottles and mimics the neurotoxic actions of estrogen in developing cerebellar neurons. Toxicol Lett. 2008 Jan 30;176(2):149-56.
- vom Saal FS, Welshons W, Large effects from small exposures. II. The importance of positive controls in low-dose research on bisphenol A, Environmental Research, 2006 Jan, 100: 50-76.
- (en) V. Branistea et al., « Impact of oral Bisphenol A at reference doses on intestinal barrier function and sex differences after perinatal exposure in rats », dans PNAS, vol. 106, no 50, 2009 [résumé (page consultée le 16 décembre 2009)].
- point sur le bisphénol A, voir aussi le dossier sur le BPA.
- (en) Page d'information sur le bisphénol A du gouvernement du Canada.
- Lyndsey Layton, Reversing itself, FDA expresses concerns over health risks from BPA, Washington Post, 16 janvier 2010
- A false sense of security, Chicago Tribune, 24 janvier 2009
- Le bisphénol A n'est pas dangereux pour la santé, selon l'Agence européenne, le Monde. Mis en ligne le 30 septembre 2010, consulté le 30 septembre 2010
- Rapport de l'ANSES Effets sanitaires du bisphénol A et connaissances relatives aux usages du bisphénol A.
- Anses, Effets sanitaires du bisphénol A Rapport d’expertise collective Connaissances relatives aux usages du bisphénol A Rapport d’étude Ed scientifiques, Sept 2011
- Voir § Appel à projet ; "Rapports relatifs aux effets sanitaires et aux usages du bisphénol A"
- Biedermann-Brem S., Grob K., Fjeldal P., (2008). Release of bisphenol A from polycarbonate baby bottles: mechanisms of formation and investigation of worst case scenarios. Eur. Food Res. Technol. 227: 1053-1060
- Biedermann-Brem S. and Grob K., (2009). Release of bisphenol A from polycarbonate baby bottles: water hardness as the most relevant factor Eur. Food Res. Technol. 228: 679-684.
- « Allo, maman bobo ! », dans Le Nouvel Observateur, 25 septembre 2008 et Nouvel Observateur Magazine digital - nouvelobs.com.
- Q/A Dodie et Q/A Avent.
- « Seul le Canada s'inquiète des biberons au bisphénol A », dans Le Monde du 22 octobre 2008 Le Monde.fr : Archives.
- « Biberon chauffé au micro-ondes : pas de danger, assure l'Afssa », dans Le Monde du 16 novembre 2008 Le Monde.fr : Archives.
- « Un biberon pour la route », dans Le Canard enchaîné du 19 novembre 2008.
- « Les biberons seront bientôt garantis sans bisphénol A » 10 mars 2009, Le Monde.
- Lise Aksglaede, Kaspar Sørensen, Jørgen H. Petersen, Niels E. Skakkebæk, and Anders Juul Recent Decline in Age at Breast Development: The Copenhagen Puberty Study Pediatrics, May 2009; 123: e932 - e939 (résumé)
- Germaine M. Buck Louis, L. Earl Gray, Jr, Michele Marcus, Sergio R. Ojeda, Ora H. Pescovitz, Selma Feldman Witchel, Wolfgang Sippell, David H. Abbott, Ana Soto, Rochelle W. Tyl, Jean-Pierre Bourguignon, Niels E. Skakkebaek, Shanna H. Swan, Mari S. Golub, Martin Wabitsch, Jorma Toppari, and Susan Y. Euling Environmental Factors and Puberty Timing: Expert Panel Research Needs Pediatrics, Feb 2008; 121: S192 - S207. (Résumé)
- (en)Diamanti-Kandarakis et al. ; « Endocrine-Disrupting Chemicals: An Endocrine Society Scientific Statement » ; Endocrine Reviews vol. 30, n°4, p. 293-342 (juin 2009) ([PDF]Déclaration, en anglais, 56 pages, consulté le 17 juin 2009)
- (en)Résumé de l'étude EDRV
- http://www.lepost.fr/article/2010/02/05/1925498_l-avis-des-medecins-de-terrain-sur-l-avis-de-l-ultra-theorique-afssa-sur-le-bisphenol-a.html
- « Le Parlement interdit l'utilisation des biberons au bisphénol A », LeMonde.Fr avec l'AFP et Reuters, 24 juin 2010.
- 2 Intissar Limam; Ang line Guenne; Mohamed Ridha Driss and Laurent Mazeas Simultaneous determination of phenol, methylphenols, chlorophenols and bisphenol-A by headspace solid-phase microextraction-gas chromatography-mass spectrometry in water samples and industrial effluents’ journal of analytical chemistry,Volume 90, Issue 3 - 6 January 2010, pages 230 - 244.
Voir aussi
Bibliographie
- Dianin, Zhurnal russkogo fiziko-khimicheskogo obshchestva, 23 (1891), p. 492 ff.
- Th. Zincke, Mittheilungen aus dem chemischen Laboratorium der Universität Marburg, Justus Liebigs Annalen der Chemie, 343 (1905), p. 75-131.
- (en) Handbook of Chemistry and Physics, CRC Press, 76th edition (1995-1996).
- (en) E. C. Dodds and Wilfrid Lawson, « Synthetic strogenic Agents without the Phenanthrene Nucleus », Nature, vol. 137, p. 996 (1936).
- (en) E. C. Dodds and W. Lawson, « Molecular Structure in Relation to Oestrogenic Activity. Compounds without a Phenanthrene Nucleus », Proceedings of the Royal Society of London, Series B, Biological Sciences, vol. 125, pp. 222-232 (1938).
- (en) Attila Zsarnovszky, Hoa H. Le, Hong-Sheng Wang et Scott M. Belcher, « Ontogeny of Rapid Estrogen-Mediated Extracellular Signal-Regulated Kinase Signaling in the Rat Cerebellar Cortex: Potent Nongenomic Agonist and Endocrine Disrupting Activity of the Xenoestrogen Bisphenol A », Endocrinology, n° 146, pp. 5388-5396 (2005).
- Jean-Yves Nau, « Alerte sanitaire sur les plastiques alimentaires », Le Monde, 14 mai 2008.
- Stéphane Foucart, « Bisphénol A, les dessous d'un scandale sanitaire », Le Monde, samedi 29 octobre 2011, pp. 6-7.
Articles connexes
- Canalisation, epoxy
- Biberon, jouets, plastiques
- Perturbateur endocrinien
- Délétion de la spermatogenèse
- Syndrome de dysgénésie testiculaire
Liens externes
- Anti-BPA
Informations, sources, études sur le Bisphenol A
- Pro-BPA
- (fr) Site d'information de l'industrie européenne du plastique sur le bisphénol A
- (en) Site d'information de l'industrie du plastique sur le bisphénol A
- Dossiers à vocation scientifique
Catégories :- Produit chimique nocif
- Bisphénol
- Polluant
- Perturbateur endocrinien
- Plastifiant
Wikimedia Foundation. 2010.