- Hydrogénopersulfate de potassium
-
Hydrogénopersulfate de potassium 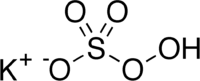
Général Nom IUPAC hydrogénopersulfate de potassium Synonymes peroxymonosulfate de potassium
monopersulfate de potassium
MPS
Caroat
OxoneNo CAS
et (sel triple - voir le texte)PubChem SMILES InChI Propriétés chimiques Formule brute KHSO5 Masse molaire[1] 152,168 ± 0,007 g·mol-1
H 0,66 %, K 25,69 %, O 52,57 %, S 21,07 %,Précautions Directive 67/548/EEC[2] 
C
OPhrases R : 8, 34, 37, Phrases S : 17, 36/37/39, Transport - 3260 Unités du SI & CNTP, sauf indication contraire. L'hydrogénopersulfate de potassium ou peroxymososulfate de potassium (aussi connue sous l'abréviation MPS et les noms de marque Caroat® et Oxone®) est le sel de potassium de l'acide persulfurique. Il est largement utilisé comme agent d'oxydation en chimie organique[3].
Ce sel est commercialisé par deux compagnies : Evonik (auparavant Degussa) sous le nom de marque Caroat® et DuPont sous le nom d'Oxone®, nom de marque qui maintenant est devenu un mot commun dans le vocabulaire de la chimie. Ces produits sont, de fait, le sel triple de formule 2KHSO5·KHSO4·K2SO4, MM = 614.76 g/mol[4],[5]. Le potentiel standard (E0) pour ce sel triple est de 1,85 V[6] pour la demi-réaction qui génère l'ion hydrogénosulfate :
- HSO5– + 2 H+ + 2 e– → HSO4– + H2O E0 = 1,85 V
Réactions
L'oxone est un oxydant versatile[3]. Il oxyde les aldéhydes en acides carboxyliques, en présence de solvants alcooliques, les esters peuvent être obtenus. Les alcènes internes peuvent être clivés pour donner deux acides carboxyliques tandis que les alcènes terminaux sont époxydés. Les thioéthers donnent des sulfones, les amines tertiaires des amine oxyde et les phosphines des phosphine oxydes (en)[7].
Une illustration du pouvoir oxydant de ce sel est la conversion d'un dérivé de l'acridine en l'acridine-N-oxyde correspondant[8]:
Il oxyde aussi un thioéther en sulfone avec deux équivalents[9] et avec un seul équivalent, la réaction s'arrête au stade sulfoxyde car la réaction qui convertit le sulfure en sulfoxyde est beaucoup plus rapide que la réaction qui convertit le sulfoxyde en sulfone. Il est ainsi possible d'arrêter facilement la réaction au stade désiré :
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Potassium peroxymonosulfate » (voir la liste des auteurs)
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- http://www.tcieurope.eu/fr/catalog/O0310.html
- http://www.organic-chemistry.org/chemicals/oxidations/oxone-potassiumperoxomonosulfate.shtm
- [PDF] Oxone sur dupont.com
- Oxone. Spectral Database for Organic Compounds (SDBS), National Institute of Advanced Industrial Science and Technology (AIST).
- in le document .pdf de DuPont cité ci-dessus
- Benjamin R. Travis, Meenakshi Sivakumar, G. Olatunji Hollist, and Babak Borhan, « Facile Oxidation of Aldehydes to Acids and Esters with Oxone », dans Organic Letters, vol. 5, no 7, 2003, p. 1031 [lien PMID, lien DOI]
- Thomas W. Bell, Young-Moon Cho, Albert Firestone, Karin Healy, Jia Liu, Richard Ludwig, and Scott D. Rothenberger (1993). "9-n-Butyl-1,2,3,4,5,6,7,8-Octahydroacridin-4-ol". Org. Synth.; Coll. Vol. 8: 87.
- James R. McCarthy, Donald P. Matthews, and John P. Paolini (1998). "Reaction of Sulfoxides with Diethylaminosulfur Trifluoride". Org. Synth.; Coll. Vol. 9: 446.
Liens externes
- Utilisations
- (en) DuPont Oxone Monopersulfate Compound Applications
- (en) Potassium Monopersulfate – Article on precious metal extraction from distributor Green
- Données



