- 1,2-dibromoéthane
-
1,2-dibromoéthane 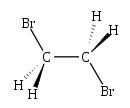
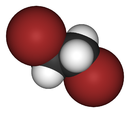
Général Nom IUPAC 1,2-dibromoéthane Synonymes dibronure d'éthylène
bromure d'éthylène
EDB
bromure de glycol
Bromofume (nom de marque),
Dowfume (nom de marque)No CAS No EINECS No RTECS PubChem ChEBI SMILES InChI Apparence liquide incolore Propriétés chimiques Formule brute C2H4Br2 [Isomères] Masse molaire[1] 187,861 ± 0,004 g·mol-1
C 12,79 %, H 2,15 %, Br 85,07 %,Propriétés physiques T° fusion 8-11 °C[2],[3] T° ébullition 131-132 °C[2],[3] Masse volumique 2,18 g·cm-3 à 25 °C[2] Pression de vapeur saturante 11,7 mmHg à 25 °C[2] Propriétés optiques Indice de réfraction  = 1,539[2]
= 1,539[2]Précautions Directive 67/548/EEC[4] 
T
NPhrases R : 23/24/25, 36/37/38, 45, 51/53, Phrases S : 45, 53, 61, Transport[5] 66 1605 NFPA 704 SGH[5] 


Unités du SI & CNTP, sauf indication contraire. Le 1,2-dibromoéthane ou sym-dibromoéthane est un composé organique de formule semi-développée BrCH2CH2Br. Ce liquide incolore avec une odeur sucrée, détectable dès 10 ppm, est un fumigant largement utilisé et parfois controversé. Bien qu'il apparaisse naturellement sous forme de traces dans les océans où il est probablement formé par des algues et le kelp, il est principalement produit synthétiquement.
Sommaire
Préparation
Le 1,2-dibromoéthane est produit par la réaction de l'éthène avec le brome, dans une réaction d'addition d'halogène (en) classique:
- CH2=CH2 + Br2 → BrCH2CH2Br
Utilisation
L'utilisation autrefois dominante du 1,2-dibromoéthane, en 2010 disparue, était comme additif dans l'essence au plomb. Celui-ci réagit avec les résidus de composés du plomb pour générer des bromures de plomb volatils. Il a aussi été utilisé comme pesticide dans les sols et sur différentes cultures après que le 1,2-dibromo-3-chloropropane (DBCP) soit interdit. Mais en raison de sa toxicité, la plupart de ses utilisations sont, en 2010, quasiment arrêtées. Il continue cependant à être utilisé pour la fumigation des grumes contre les termites et coléoptères, pour le contrôle des papillons hétérocères dans les ruches et comme réactif chimique dans la préparation de teintures et de cires[6].
Le 1,2-dibromoéthane est utilisé en synthèse organique comme une source de brome, par exemple pour bromer des carbanions et pour activer le magnésium pour la synthèse de certains réactifs de Grignard. Dans ce dernier cas, le 1,2-dibromoéthane est converti en bromure d'éthénylmagnésium, ce qui dégage une partie fraichement décapée sur la magnésium, mieux à même de réagir avec le substrat[7].
Effets médicaux
Les effets sur les êtres humains de la respiration de 1,2-dibromoéthane à des niveaux élevés ne sont pas connus, mais des études animales ont montré que l'exposition à court terme et à des niveaux élevés causent lipothymie et dépression, indiquant des effets sur le cerveau[8].
Rougeurs et l'inflammations, y compris la formation de phlyctènes (cloques) sur la peau et d'ulcères dans la bouche et l'estomac, peuvent se produire si de grandes quantités sont ingérées. Une ingestion accidentelle a ainsi causé la mort d'une femme de Molokai, à Hawaii[6]. Il est très improbable qu'il y ait un risque de mort pour les personnes exposées à de faibles niveaux.
Bien que très peu soit connu sur les effets de la respiration de 1,2-dibromoéthane sur le long terme, il semble que certains travailleurs exposés ressentent des effets sur leur reproduction incluant un dégradation de la qualité de leur sperme.
Chez le rat, la mort intervient par respiration de niveaux élevés sur de courtes périodes. Des niveaux plus faibles causent des dommages sur leur foie et leurs reins. Quand des rats respirent de l'air ou mangent de la nourriture contenant du 1,2-dibromoéthane sur de courtes ou de longues périodes, ils sont moins fertiles et leur sperme présente des anomalies.
Des changements dans le cerveau et dans le comportement ont été aussi observés chez de jeunes rats dont les parents avaient respirés du 1,2-dibromoéthane et des maladies congénitales ont été relevés chez des jeunes dont les mères avaient été exposées pendant leur grossesse[8].
Le 1,2-dibromoéthane est un cancérigène connu, classé en haut des substances cancérogènes de l'index HERP[9].
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « 1,2-Dibromoethane » (voir la liste des auteurs)
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- 1,2-Dibromoethane chez Sigma-Aldrich.
- NIST : Ethane, 1,2-dibromo-.
- « 1,2-dibromoethane » sur ESIS, consulté le 26 octobre 2010
- Entrée de « 1,2-Dibromoethane » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 26 octobre 2010 (JavaScript nécessaire)
- Toxicalogical Profile for 1,2-Dibromoethane
- Maynard, G. D. 1,2-Dibromoethane' in Encyclopedia of Reagents for Organic Synthesis,Ed: L. Paquette, 2004, J. Wiley & Sons, New York. {{DOI:10.1002/047084289}}.
- ToxFAQs for 1,2-Dibromoethane
- Ranking Possible Cancer Hazards on the HERP Index
Catégories :- Produit chimique toxique
- Produit chimique dangereux pour l'environnement
- Cancérogène chimique
- Bromoalcane
- Insecticide
- Cancérogène du groupe 2A du CIRC
Wikimedia Foundation. 2010.


