- 1,1-dichloroéthène
-
1,1-dichloroéthène 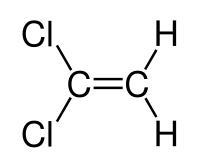
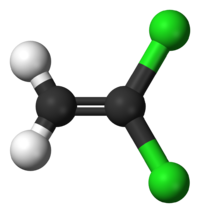
Général Nom IUPAC 1,1-dichloroéthène Synonymes 1,1-dichloroéthylène
1,1-DCE
chlorure de vinyldiène
dichlorure de vinyldièneNo CAS No EINECS PubChem SMILES InChI Apparence Liquide incolore à jaunâtre à l'odeur douce[1] Propriétés chimiques Formule brute C2H2Cl2 [Isomères] Masse molaire[2] 96,943 ± 0,006 g·mol-1
C 24,78 %, H 2,08 %, Cl 73,14 %,Propriétés physiques T° fusion -122 °C[1] T° ébullition 32 °C[1] Solubilité 2,5 g·l-1 (eau, 20 °C) Masse volumique 1, 25 g·cm-3[1] T° d'auto-inflammation 530 °C[1] Point d’éclair 25 °C, coupelle fermée[1] Limites d’explosivité dans l’air 6,5 Vol.-% 260 g·m-3
15 Vol.-% 600 g·m-3Pression de vapeur saturante 660 mbar à 20 °C
954 mbar à 30 °C
1 900 mbar à 50 °CPrécautions Directive 67/548/EEC[1] 
Xn
F+Phrases R : 12, 20, 40, Phrases S : (2), 7, 16, 29, 36/37, 46, Transport 339 1303 Écotoxicologie DL50 194 mg·kg-1 (souris, oral)[3] LogP 2,13[1] Unités du SI & CNTP, sauf indication contraire. Le 1,1-dichloroéthène, appelé couramment 1,1-dichloroéthylène ou 1,1-DCE est un composé organo-chloré de formule C2H2Cl2 qui réagit violemment en diverses circonstances.
Il est la matière première de la fabrication du polychlorure de vinylidène (PVDC) ou Saran.
Sommaire
Propriétés[1]
Le 1,1-dichloroéthène se présente sous la forme d'un liquide incolore à jaunâtre, très volatil, à l'odeur douce. Plus lourd que l'eau, il y est peu soluble, mais est très soluble dans les solvants organiques (éthanol, éther diéthylique, acétone, benzène, chloroforme). Il est extrêmement inflammable, et forme avec l'air un mélange explosif. Il se décompose lorsqu'il est chauffé, et dégage alors notamment du chlorure d'hydrogène et du phosgène. Il tend aussi à se polymériser spontanément. Non stabilisé, il peut se polymériser spontanément dans une réaction violente avec risque d'explosion. Les polymères formées (contenant par exemple des fonctions de peroxydes) peuvent exploser lors d'un impact. Le 1,1-dichloroéthène peut exploser s'il rentre en contact avec le chlorotrifluoroéthylène à chaud, l'ozone, les peroxydes, les hydroxydes de métaux alcalins en présence d'oxygène. Il réagit de façon dangereuse avec les métaux alcalins, l'hydroxyde de potassium, l'air (formation de peroxydes), les agents oxydants, les amides, l'acide chlorosulfurique et l'acide sulfurique fumant.
Synthèse
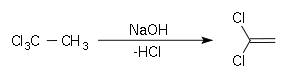
Le 1,1-dichloroéthène peut être produit par déhydrochloration du 1,1,1-trichloroéthane ou du 1,1,2-trichloroéthane, par action de l'hydroxyde de potassium :
On préfèrera en général utiliser le second, qui est un sous-produit non voulu de la synthèse de 1,1,1-trichloroéthane ou du 1,2-dichloroéthane.
Utilisation
Le 1,1-dichloroéthène est principalement utilisé comme co-monomère dans la polymérisation du chlorure de vinyle, de l'acrylonitrile et des acrylates. Il est aussi utilisé dans l'industrie des semi-conducteurs pour faire croitre des couches minces de dioxyde de silicium de haute pureté.
Chlorure de polyvinylidène
Article principal : chlorure de polyvinylidène.Comme de nombreux autres alcènes, le 1,1-dichloroéthène peut être polymérisé pour former du chlorure de polyvinylidène. Un produit très utilisé, un film plastique, le Saran est fait à partir de ce polymère. Au cours des années 1990, des recherches auraient suggéré que, comme de nombreux composé carbonés chlorés, le Saran pouvait être un danger pour la santé, en particulier via la nourriture chauffée à son contact dans les fours à micro-ondes. Depuis 2004, les films plastiques alimentaires on changé de composé et utilisent désormais un dérivé du polyéthylène.
Notes et références
- Entrée de « 1,1-Dichloroethylene » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 13/11/2010 (JavaScript nécessaire)
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- British Journal of Cancer. Vol. 37, Pg. 411, 1978. PMID
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « 1,1-Dichloroethene » (voir la liste des auteurs)
Voir aussi
Catégories :- Produit chimique nocif
- Produit chimique extrêmement inflammable
- Chloroalcène
Wikimedia Foundation. 2010.